
• Claudio Mongardini1
• Andrea Pilloni1
1Sapienza, Università di Roma - Corso di laurea magistrale in Odontoiatria e Protesi dentaria Cattedra di Parodontologia (Titolare: Prof. Andrea Pilloni)
Riassunto
La parodontite è una malattia infiammatoria che colpisce le strutture di sostegno dei denti dovuta alla presenza di una flora batterica patogena nella placca dentale in individui predisposti. Il fondamento della terapia parodontale si basa sull’eliminazione, attraverso la strumentazione radicolare, degli agenti eziologici della malattia. La decontaminazione dei tessuti parodontali è però molto difficile, se non impossibile, per questo sono state proposte varie terapie antimicrobiche aggiuntive a quella meccanica. Le ben note problematiche legate all’uso eccessivo degli antibiotici sistemici hanno indotto la ricerca verso strategie di disinfezione alternative.
La terapia fotodinamica (PDT) o disinfezione attivata dalla luce (LAD) è stata sperimentata per la prima volta da Oscar Raab, chimico tedesco, agli inizi del ‘900. Abbandonata per l’avvento degli antibiotici ha ritrovato nuovo fulgore negli ultimi decenni sia in campo medico che in Odontoiatria, proprio per le problematiche legate all’abuso di antibiotici. Le reazioni fotodinamiche si avvalgono dell’utilizzo di un fotosensibilizzante (PS) e di una sorgente luminosa tarata su specifiche lunghezze d’onda in presenza di ossigeno.
La peculiarità di alcuni PS permette loro di agire specificatamente contro i microrganismi sia Gram+ che Gram- senza provocare alcun danno alle cellule ospiti. Molto efficace è il blu di toluidina, attivo nei confronti di numerosi batteri tra i quali quelli implicati nella malattia parodontale.
Recentemente numerose pubblicazioni hanno messo in evidenza risultati interessanti sia dal punto di vista clinico che microbiologico quando questa tecnica di disinfezione aggiuntiva viene utilizzata in terapia parodontale.
Parole chiave: parodontite, terapia parodontale non-chirurgica, terapia fotodinamica, antimicrobici, LAD, PDT
Summary
Periodontitis is an inflammatory disease that affects the supporting structures of teeth due to the presence of a pathogenic flora in the dental plaque biofilm in susceptible subjects.
The objective of periodontal therapy is the elimination of the causative agents of the disease, through the instrumentation of the dental root surface. The complete decontamination of the periodontal tissues is very difficult, if not impossible, therefore many antimicrobial therapies were proposed with time as adjunctive to mechanical therapy.
The well-known problems relating to the excessive use of systemic antibiotics have stimulated the search for alternative disinfection strategies.
Photodynamic therapy (PDT) or light activated disinfection (LAD) has been described scientifically for the first time by Oscar Raab, a german chemist, at the beginning of ‘900. Abandoned due to the discovery of antibiotics, PDT has found new luster in recent decades both in the medical field and in dentistry, due to the well-known problems related to the abuse of antibiotics. Photodynamic reactions involve the use of a photosensitizer (PS) and
a light source calibrated on a specific wavelength, in the presence of oxygen.
The characteristics of some PS allow them to be specifically active against both Gram+ and Gram- microrganisms without causing any damage to the host cells. Very effective is toluidine blue, active against many bacteria, including those involved in periodontal disease.
Recently many publications have shown interesting clinical and microbiological results, when this adjunctive disinfection technique is used in periodontal therapy.
Key words: periodontitis, non-surgical periodontal treatment, photodynamic therapy, antimicrobical treatment, LAD, PDT
La parodontite è una malattia che colpisce le strutture di sostegno dei denti a patogenesi infiammatoria, indotta dalla presenza di una flora batterica patogena nella placca dentale. La formazione della placca batterica è dunque una condizione necessaria affinché si verifichino quei processi infiammatori causa di gengiviti prima e parodontiti poi, ma non sufficiente, poiché tali processi sono fortemente influenzati dalla suscettibilità individuale1. Dal punto di vista microbiologico, la cavità orale può essere considerata come un ecosistema caratterizzato da complesse interrelazioni tra la componente microbica residente e l’ambiente del cavo orale. Tale ambiente non è costituito da un singolo habitat uniforme ma, al contrario, comprende un certo numero di distinte nicchie ecologiche, ciascuna con una propria composizione microbiologica. Infatti, la topografia della cavità orale presenta distretti molto diversi tra loro: denti, solchi e tasche gengivali, fornici buccali, pavimento, labbra e lingua. Nella cavità orale sono presenti, inoltre, diversi fattori che predispongono alla selezione di determinati microrganismi. L’intero ecosistema orale è la somma di entità topografiche e di microrganismi a esse associate che caratterizzano un particolare tipo di microbioma2. La placca dentale è un deposito soffice che si accumula sui denti non adeguatamente puliti3. Può essere definita come una complessa comunità microbica (biofilm orale), prevalentemente composta da microrganismi batterici inglobati all’interno di una matrice intercellulare, nella quale sono state identificate a oggi circa 700 specie batteriche differenti4.
Sono stati trovati anche microrganismi non batterici della specie mycoplasma, lieviti, protozoi e virus5 oltre a un piccolo numero di cellule epiteliali, di leucociti e di macrofagi. All’interno del biofilm le svariate specie batteriche sono in grado di interagire tra loro, comunicare attraverso l’emissione di segnali chimici6 e scambiare tratti genetici. Il risultato di quest’interazione permette un’aumentata sopravvivenza microbica e una maggiore resistenza alle difese immunitarie dell’organismo ospite o alle sostanze antimicrobiche quali gli antibiotici. Il fondamento della terapia parodontale si basa sull’eliminazione meccanica della placca batterica con l’obiettivo di ridurre o eliminare gli agenti patogeni (soprattutto batteri Gram- anaerobi) che iniziano e sono alla base della progressione della parodontite. Non essendo, ovviamente, possibile la “sterilizzazione” del cavo orale, la terapia parodontale mira, dal punto di vista microbiologico, a rimuovere e scompaginare il biofilm batterico dalle superfici dentali e rallentare la ricolonizzazione dei microrganismi patogeni7-9. Occorre ricordare che la flora microbica sottogengivale ha origini sopragengivali; difatti la quantità, la composizione e la percentuale di ricolonizzazione della placca sottogengivale dipendono dall’accumulo di placca sopragengivale. Di conseguenza, il controllo efficace della placca sopragengivale, combinato con una frequente terapia di igiene professionale sottogengivale, è determinante nel controllo a lungo termine della parodontite. Attualmente il trattamento più ampiamente usato per raggiungere questo obiettivo è la strumentazione manuale o con strumenti “power-driven” della superficie radicolare10.

La terapia meccanica superficiale (scaling e root planing: SRP) e la rimozione del biofilm sopra e sottogengivale sono considerati il gold standard per il trattamento delle malattie parodontali infiammatorie. Scaling e root planing (SRP) consistono nella rimozione meccanica del biofilm e del tartaro spesso eseguiti insieme con l’uso aggiuntivo di diversi tipi di antimicrobici. Nonostante i miglioramenti clinici, l’auspicato risultato dopo SRP - cioè l’eradicazione completa degli agenti patogeni parodontali - è molto difficile o impossibile da raggiungere7 soprattutto perché le procedure di “sbrigliamento” da sole non possono essere sempre efficaci a causa della presenza di tasche profonde o di lesioni in zone difficilmente raggiungibili come quelle delle forcazioni11, o anche perché alcuni patogeni sono in grado di invadere i tessuti molli della tasca parodontale o, ancora, perché si verifica la ricolonizzazione dei siti trattati nel caso in cui altre zone intra-orali o nicchie rimangano non trattate12.

Le procedure sottogengivali (scaling e root planing) possono essere realizzate tramite una tecnica chiusa e una aperta. La prima prevede una strumentazione sottogengivale senza dislocazione intenzionale della gengiva; la seconda implica l’esplorazione della superficie radicolare con tecniche chirurgiche che dislocano il tessuto gengivale. Con la tecnica non chirurgica l’impossibilità di prendere visione diretta della superficie radicolare può essere superata dall’abilità dell’operatore, e le difficoltà dell’accesso si riducono gradualmente, così come i risultati legati alla presenza di recessioni in risposta alla strumentazione sottogengivale.
Lindhe e Nyman nel 198713 sostenevano, infatti, che il fattore critico della terapia parodontale non fosse solamente la scelta della modalità di trattamento, ma anche l’accuratezza del debridement radicolare e il livello di igiene orale del paziente. Studi molto accurati effettuati per valutare l’efficacia dell’intervento sul tartaro, in seguito a scaling e root planing, hanno dimostrato come la rimozione completa del tartaro dalle superfici radicolari sia raramente ottenuta, sia con accesso chirurgico, sia conservativo. Analizzando i risultati riportati dalla revisione effettuata dal workshop dell’Accademia Americana di Parodontologia, si evidenzia che la percentuale di superfici radicolari esibenti tartaro residuo, dopo scaling e root planing senza accesso chirurgico, varia tra il 17% e il 69%. Con accesso chirurgico la percentuale varia tra il 14% e il 24%. Fleischer et al.14, ad esempio, hanno evidenziato che gli operatori pur con esperienza decennale ottenevano forcazioni prive di tartaro solo il 68% delle volte. Gli effetti dello scaling e del root planing sui livelli di attacco clinico sono in genere rapportati alle profondità di tasca iniziali.
I benefici clinici si traducono in una riduzione del livello di attacco clinico nelle tasche parodontali più profonde15. In particolare è stato rilevato un più evidente miglioramento del livello di attacco clinico nelle tasche con profondità maggiore di 6 mm, uno meno evidente nelle tasche di 4-6 mm e uno scarso, se non nullo, in quelle che inizialmente avevano una profondità minore di 4 mm7. La maggior parte dei lavori sperimentali pubblicati in letteratura è concorde con gli studi eseguiti da Waerhaug16, Rabbani et al.17, Stambaugh et al.18, i quali affermano che all’aumentare della profondità di tasca crescono anche le difficoltà a levigare le radici in modo accurato. D’altra parte Badersten et al. hanno pubblicato una serie di lavori in cui hanno dimostrato l’efficacia delle procedure di scaling e root planing (SRP) in soggetti con parodontite moderatamente avanzata e avanzata, affermando che non esiste una misura iniziale della profondità di tasca per stabilire se la terapia non chirurgica possa essere efficace o meno19. Inoltre, anche in pazienti estremamente controllati pur avendo mantenuto la stabilità parodontale per un lungo periodo possono essere presenti o manifestarsi nuovamente delle cosiddette “residual pockets”20,21.
Gli episodi di ulteriore perdita di attacco e, alla lunga, di elementi dentari si possono quantificare in circa il 40% per alcuni Autori20 fino a un quinto della popolazione trattata per altri21. In alcuni casi per ridurre i patogeni oltre alla pulizia accurata delle superfici dei denti si raccomanda l’uso degli antibiotici22,23. Tuttavia, la terapia non chirurgica viene effettuata senza dover ricorrere ad antibiotici aggiuntivi, preferendo usarli solo laddove il trattamento abbia fallito, così che gli antibiotici vengono visti come un ritrattamento e non come parte della terapia iniziale24. In uno studio riguardante il successo degli antibiotici in pazienti che li hanno ricevuti in terapia causale rispetto ad altri ai quali sono stati somministrati solo 6 mesi dopo SRP durante il follow-up (gruppo placebo) è stato riscontrato che i pazienti che hanno ricevuto il trattamento antibiotico iniziale avevano valori statistici significativamente migliori rispetto al gruppo di controllo25. A causa dei numerosi effetti collaterali (soprattutto gastrointestinali) dovuti alla somministrazione sistemica di antibiotici e del rischio di sviluppare ceppi resistenti per l’uso improprio degli stessi, si assiste negli ultimi tempi all’aumento della domanda di antibatterici alternativi. Così, la sfida consiste nel valutare nuove alternative di trattamento in grado di provocare minori effetti collaterali, eliminando efficacemente la flora patogena parodontale.
La terapia fotodinamica
La Terapia fotodinamica (PDT, acronimo del termine inglese “Photo Dynamic Therapy”), talvolta chiamata “fotochemioterapia”, è una forma di fototerapiache utilizza composti sensibili alla luce non tossici. Questi una volta esposti alla stessa fonte luminosa in modo selettivo diventano tossici nei confronti di particolari tipologie cellulari. Il potere terapeutico della luce solare era noto sin dall’antichità: Ippocrate, il padre della medicina, prescriveva ai propri pazienti bagni di sole per curare i propri mali, ma solo recentemente la luce ha rappresentato una nuova frontiera per la cura di numerose patologie in diverse branche della medicina, quali l’oftalmologia, l’oncologia e la dermatologia. La PDT ha oramai ottenuto l’approvazione per il trattamento di alcune neoplasie in molti paesi, anche se il numero totale di indicazioni cliniche è ancora limitato26,27. In dermatologia, ad esempio, viene comunemente usata nel trattamento dell’acne28, mentre in oculistica è impiegata per trattare una vasta gamma di condizioni mediche, tra cui la degenerazione maculare legata all’età ed è riconosciuta come una strategia di trattamento minimamente invasivo e minimamente tossico29. Questo sviluppo rappresenta il punto di arrivo di diversi decenni di indagini intensive, che hanno fornito una serie di informazioni riguardo la correlazione tra la struttura chimica degli agenti fotosensibilizzanti e le loro proprietà farmaco-cinetiche, nonché sul loro modo di azione a livello cellulare e tissutale30,31. L’uso della PDT come modalità terapeutica per il trattamento di infezioni microbiche localizzate (aPDT o “antimicrobial Photo Dynamic Therapy”) rappresenta un nuovo campo di applicazione emergente. In realtà le prime osservazioni dei processi fotodinamici registrati in medicina si riferiscono all’inattivazione dei microrganismi. Raab32, un chimico tedesco, notò che l’interazione tra l’acridina arancio (un colorante), e una fonte luminosa portava a distruzione di colonie di Paramecia caudatum; la reazione tra luce visibile e ossigeno fu dimostrata qualche anno più tardi da von Tappeiner che per primo coniò il termine “fotodinamico”. Tali studi vennero accantonati per decenni per due ragioni:
- alcuni batteri, soprattutto gram negativi, rispondevano scarsamente alla terapia fotodinamica con i fotosensibilizzanti conosciuti all’epoca;
- la scoperta degli antibiotici, che fece ipotizzare alla comunità scientifica internazionale di avere un’arma infallibile nel debellare le malattie infettive batteriche.
Ad oggi un’urgente necessità dello sviluppo di approcci innovativi ed efficaci per la lotta contro le infezioni microbiche è stata determinata da alcuni fattori sociali, come l’inadeguata o eccessiva prescrizione di antibiotici, la diffusa aggiunta di antibiotici nei mangimi animali, la sempre più frequente trasmissione di microrganismi causata dai viaggi, l’espansione della povertà nelle popolazioni dei paesi del Terzo mondo, come pure la grande varietà di meccanismi adottati dalle cellule microbiche per aumentare la loro resistenza agli insulti esterni (quali l’ispessimento della parete esterna, la codifica di nuove proteine che impediscono la penetrazione di farmaci ecc.)33. Recenti risultati sostengono l’ipotesi che la PDT possa rappresentare una valida alternativa in quanto le modalità d’azione dei sensibilizzanti fotodinamici sulle cellule microbiche sono nettamente diverse da quelle tipiche della maggior parte dei farmaci antibiotici34.
Meccanismo d’azione
La aPDT si basa sull’impiego di una fonte luminosa di particolare lunghezza d’onda coerente (laser) o non (lampade a LED), un colorante (fotosensibilizzante) e la concomitante presenza di ossigeno. La combinazione di questi elementi determina la trasformazione degli atomi di ossigeno, che normalmente si trovano nello stato elettronico tripletto, in radicali liberi dell’ossigeno (ossigeno singoletto)35 (Figura 1). L’utilizzo della terapia fotodinamica come terapia antimicrobica prevede 3 fasi distinte, che qui di seguito riportiamo.
- Fase 1: colorazione dei microrganismi. Nella fase 1 il fotosensibilizzante si diffonde in maniera selettiva nelle cellule da trattare in modo da generare una differenza di concentrazione rispetto ai tessuti sani circostanti. Le membrane batteriche, cariche negativamente, e il fotosensibilizzante, carico positivamente, reagiscono attraverso un legame covalente polare.
- Fase 2: esposizione e attivazione del fotosensibilizzante. Una volta somministrato il fotosensibilizzante, questo viene esposto a una fascio di luce prodotto da un laser o da una lampada a LED di adeguata lunghezza d’onda in funzione del fotosensibilizzante che verrà utilizzato. L’assorbimento dell’energia prodotta dalle radiazioni luminose stimola quindi il fotosensibilizzante che si attiva.
- Fase 3: uccisione dei microrganismi. In quest’ultima fase avviene una delle reazioni chimiche possibili, attraverso la quale l’energia, assorbita dall’esposizione al fascio di luce, reagisce con l’ossigeno nello stato fondamentale di tripletto presente nella sostanza fotosensibile diventando 0- (ioni di ossigeno) o O° (radicali reattivi); tale reazione viene comunemente chiamata ROS (Reactive Oxygen Specimen-specie reattive dell’ossigeno) ed è dotata di un forte potere ossidante. Il ROS, reattivo, agisce distruggendo istantaneamente le pareti delle cellule microbiche per ossidazione dei lipidi di membrana e degli enzimi.
Agenti fotosensibilizzanti
I fotosensibilizzanti (PS) sono molecole fotosensibili che possiedono la caratteristica di dar luogo a reazioni chimiche dopo avere assorbito la luce, provocando la distruzione anche di molecole di per se stesse non fotosensibili. Un ideale fotosensibilizzante in grado di promuovere l’azione fotodinamica dovrebbe possedere alcune importanti proprietà:
- elevato livello di purezza;
- alto coefficiente di assorbimento molare e assorbimento nella regione rossa dello spettro;
- alta resa quantica di formazione dello stato di tripletto con tempo di vita relativamente lungo (μs) in modo da garantire un’efficiente formazione di ROS;
- assenza di tossicità al buio;
- notevole selettività di accumulo in una determinata cellula o tessuto onde orientare il foto-processo verso siti predeterminati.
Attualmente nessuna delle molecole fotosensibilizzanti studiate in vitro e/o in vivo soddisfa completamente queste caratteristiche, motivo per il quale la ricerca è particolarmente attiva nel sintetizzare un PS che si avvicini il più possibile a quello ideale. Particolarmente utilizzati in applicazioni odontoiatriche sono due fotosensibilizzanti organici cationici, classificabili tra le Fenotiazine: il blu di metilene (MB) e il blu di toluidina (TBO). Questi sono due composti di colore blu derivati dei coloranti triciclici. Queste due sostanze hanno mostrato, allo stesso tempo, di avere un’azione antimicrobica a largo spettro senza determinare citotossicità sulle cellule dell’uomo, a dosi terapeutiche36, e quindi rappresentano di fatto degli ottimi fotosensibilizzanti in medicina e, in particolare, per le applicazioni odontoiatriche. Molto probabilmente le molecole di PS cationiche vengono assorbite dalle cellule dei mammiferi molto più lentamente rispetto alle cellule batteriche37. L’attivazione del fotosensibilizzante dopo pochi minuti dalla sua somministrazione impedirebbe il danneggiamento delle cellule ospiti. Utilizzando varie concentrazioni di toluidina blu e differenti dosi di energia luminosa, Kömerick et al.38 hanno potuto dimostrare, su modello animale, che una concentrazione di 0.1 mg/ml di questo PS, una volta esposto alla luce di corretta lunghezza d’onda, è in grado di determinare una riduzione del 99% delle cellule batteriche di P. gingivalis. Inoltre, a queste concentrazioni sia il fotosensibilizzante che la fonte luminosa, se utilizzati non in associazione ma singolarmente, non hanno alcun effetto battericida.
Fonti luminose
L’energia luminosa necessaria affinché i processi fotofisici e fotochimici avvengano nella reazione fotodinamica può essere generata principalmente da 2 tipi di sistemi: il laser e le lampade a LED.
I laser
La parola laser è l’acronimo di “Light Amplification by Stimulated Emission of Radiation” e ha come caratteristica principale quella di generare un raggio luce perfettamente monocromatico in fase coerente, poiché prodotto dall’emissione stimolata di atomi tutti assolutamente uguali, e perfettamente rettilineo. Questo permette di ottenere una potenza superiore rispetto alle altre sorgenti luminose. I dispositivi laser vengono classificati in base alla potenza del raggio di emissione sprigionato dalle varie sostanze in due tipi fondamentali:
- i laser duri o power laser (oltre i 50 mW);
- i laser morbidi o soft laser (fino a 25 mW).
I primi, sfruttando un’azione di taglio dei tessuti, vengono ampiamente utilizzati in odontostomatologia in campo conservativo, per l’utilizzo sui tessuti duri dentali, ma soprattutto in campo chirurgico. Il laser a CO2, il laser Neodimio-YAG, il laser ad Argon, il laser Er-Yag e il laser a diodi (usato a potenze elevate) sono alcuni esempi di laser duri. I secondi sono rappresentati dai laser Elio-Neon e quello a diodo semiconduttore (utilizzati a bassa potenza). Questi non hanno effetti di taglio ma esplicano un’azione terapeutica biostimolante favorente i processi vitali e di guarigione con riduzione delle manifestazioni infiammatorie. Inoltre possono essere sfruttati gli effetti fotobiologici e risultano efficaci per l’esposizione e attivazione dei fotosensibilizzanti. In terapia fotodinamica quelli maggiormente utilizzati sono i laser a diodi il cui componente attivo è un semiconduttore simile a quelli impiegati nella produzione di LED (Light Emitting Diode). A secondo dei materiali utilizzati nella costruzione dei semiconduttori, il laser emetterà determinate lunghezze d’onda. I laser maggiormente utilizzati in PDT sono quelli a diodi con mezzo attivo composto da arseniuro fosfuro di gallio (GaAsP). Il fascio di luce emesso, della frequenza di 650 nm, è in grado di attivare quei fotosensibilizzanti maggiormente utilizzati nella terapia fotodinamica antimicrobica.
Le lampade LED
Il termine LED è l’acronimo di Light Emitting Diode (diodo a emissione luminosa), sviluppato nel 1962 da Nick Holonyak JR, ingegnere elettrico statunitense, che è un particolare tipo di diodo capace di emettere una piccola quantità di luce se attraversato da una corrente elettrica. L’uso in campo medico dei LED è stato reso possibile solo alla fine degli anni Novanta grazie alla nascita di LED superpotenti e quasi monocromatici da parte del dottor Whelan e del suo gruppo di ricercatori della NASA. Partendo da questa innovazione tecnologica, la ricerca è stata in grado di sviluppare LED con differenti lunghezze d’onda e con una densità di fotoni clinicamente utili per il trattamento di un’area estesa del tessuto target, caratterizzati inoltre da elevata affidabilità, lunga durata, elevata efficienza e basso consumo. L’uso dei LED con luce rossa a 633 nm (la stessa lunghezza d’onda del ben documentato laser HeNe e del laser a diodi) è capace di attivare l’acido aminolevulenico, che viene applicato topicamente per il trattamento, per esempio, dei tumori cutanei, ma anche quei fotosensibilizzanti, menzionati in precedenza, utilizzati in Odontoiatria nella PDT. Oggi la tecnologia ci ha portato ad avere lampade LED sempre più performanti e di ridotte dimensioni con puntali studiati appositamente per lavorare in ambienti limitati come quelli all’interno del cavo orale (Figura 2).
Applicazioni della aPDT in Odontoiatria
Diverse sono le possibilità di utilizzo della terapia fotodinamica in campo odontoiatrico, sfruttando sia le potenzialità antimicrobiche sia le proprietà riparative e antinfiammatorie proprie della luce nella lunghezza d’onda del rosso. Per brevità abbiamo riassunto le possibili applicazioni nella Figura 3, accennando brevemente all’applicazione endodontica e soffermandoci più dettagliatamente alle applicazioni parodontali.
Endodonzia
Il trattamento dell’infezione pulpare prevede una combinazione di pulizia chimica che include l’irrigazione con un agente disinfettante, come l’ipoclorito di sodio o il perossido di idrogeno, e il trattamento e la sagomatura del canale endodontico con strumentazione meccanica. Le principali cause di fallimento di questa procedura sono la permanenza di microrganismi e la persistente ricontaminazione del canale a causa di un’insufficiente tenuta. Negli ultimi anni sono stati proposti nuovi approcci antimicrobici per la disinfezione dei canali radicolari, che comprendono l’uso di laser ad alta potenza, nonché della aPDT39. L’utilizzo di laser ad alta potenza può potenzialmente causare danni termici collaterali come il surriscaldamento della dentina, l’anchilosi delle radici, la fusione del cemento, provocare riassorbimento radicolare e necrosi peri-radicolare. L’uso della aPDT nel trattamento delle infezioni endodontiche è stato studiato con modelli ex vivo su denti estratti. Per esempio, Fonseca e coll.40 hanno trattato canali radicolari di denti estratti e contaminati con Enterococcus faecalis irrigando i canali con blu di toluidina e irradiando per 5 minuti con una fonte luminosa a 660 nm. La riduzione media di questo batterio nei canali trattati è stata pari al 99,9%. Nelle applicazioni cliniche la combinazione della terapia endodontica standard e della aPDT ha determinato una maggiore riduzione dei batteri nei canali radicolari rispetto alla sola terapia endodontica standard sia in dentizione permanente41 sia in dentizione decidua42.
La terapia fotodinamica in parodontologia
Risultati microbiologici
Nella patogenesi delle parodontiti la presenza di una flora patogena nel biofilm dentale è essenziale43. Questo è il motivo per il quale l’obiettivo terapeutico principale della terapia parodontale è tuttora la rimozione del biofilm batterico e l’eliminazione - o quantomeno la riduzione significativa - delle specie parodonto-patogene44 e il ripristino dell’omeostasi tra il sistema immunitario dell’individuo affetto da parodontite e il complesso ecosistema polimicrobico che caratterizza il cavo orale. Il viraggio tra stato di patologia a stato di salute parodontale sotto l’aspetto microbiologico è dato, nella maggior parte dei casi, da una riduzione nella proporzione dei batteri del complesso rosso all’interno dell’ecosistema microbico45. Socransky et al.46 hanno dimostrato che i batteri nelle tasche parodontali formano dei complessi microbici che condividono aspetti metabolici e patologici. Per questo motivo questo Autore li ha classificati in gruppi, assegnando a ognuno un colore, tra i quali in quello arancio e in quello rosso si ritrovano molti parodonto-patogeni. Nello specifico, il complesso rosso è rappresentato da 3 batteri Gram- anaerobi obbligati - P. gingivalis, T. forsythia e T. denticola - che compaiono nel biofilm batterico solo dopo giorni di crescita indisturbata e sono considerati tra le specie più patogene per il parodonto45. Sebbene per la strumentazione della superficie radicolare sono stati affinati negli ultimi anni sia lo strumentario manuale sia le punte delle apparecchiature dinamiche più raffinate, lo scaling e root planing (SRP) determina un miglioramento clinico e microbiologico ma l’eradicazione completa delle specie patogene dalle tasche parodontali non è normalmente ottenibile7, soprattutto quando ci troviamo a trattare tasche di difficile accessibilità, molto profonde e/o strette, forcazioni o difetti infraossei.
Per questo motivo la ricerca in parodontologia è spesso rivolta ad approcci terapeutici che possano migliorare il risultato microbiologico del trattamento non chirurgico. Per esempio, un miglioramento clinico e microbiologico nel trattamento di forme gravi di parodontite (cronica o aggressiva) può essere ottenuto con un approccio one-stage, basato sulla strumentazione di tutte le superfici radicolari nell’arco delle 24 ore, con o senza la disinfezione aggiuntiva con clorexidina47,48. La disinfezione aggiuntiva delle tasche parodontali è, ugualmente, l’obiettivo terapeutico della combinazione dello SRP con una terapia antibiotica sistemica o locale49,50. Nonostante nelle forme di parodontite aggressiva sia stato dimostrato un miglioramento sia clinico che microbiologico, rispetto al solo trattamento meccanico51, nella comunità scientifica internazionale si teme sempre di più l’incremento mondiale della resistenza batterica agli antibiotici. In seguito all’eccessivo uso e all’abuso di antibiotici, negli ultimi anni è notevolmente aumentato il numero di pubblicazioni che hanno riportato specie batteriche resistenti a molti o a tutti gli antibiotici conosciuti52. Inoltre, la possibilità di effetti indesiderati anche gravi e la necessità di una compliance del paziente al regime terapeutico più che ottimale limitano, ulteriormente, l’uso della via sistemica. Per questo motivo l’attenzione di parte dei ricercatori si è rivolta verso strategie antimicrobiche alternative quali la aPDT, facilmente applicabile in campo odontoiatrico e, nella fattispecie, in campo parodontale, considerato anche il fatto che, a oggi, non sono stati riportati casi di insorgenza di resistenza batterica a questo tipo di trattamento8,53. Abbiamo menzionato precedentemente che la reazione fotodinamica prevede l’utilizzo di una fonte luminosa di particolare lunghezza d’onda e la presenza contemporanea di una sostanza fotosensibilizzante (PS) e di ossigeno. Alcuni PS hanno la caratteristica di legare esclusivamente le membrane cellulari batteriche, in modo da essere attivi solo sulla flora batterica senza danneggiare i tessuti dell’organismo ospite54.
Il gruppo delle fenotiazine cationiche, quali il blu di toluidina (TBO) e il blu di metilene (MB), può essere utilizzato anche per infezioni sostenute da batteri Gram- anaerobi quali quelle che sostengono le malattie parodontali53. Per esempio, il TBO si è mostrato efficace su molti batteri parodontopatogeni conosciuti, sia in vitro55 che in modello sperimentale animale56. Esiste evidenza scientifica che dimostra che è possibile determinare la morte delle cellule batteriche sensibilizzate con un PS adeguato e irradiate con una fonte luminosa (per esempio, laser a diodi) a lunghezza d’onda idonea57. Zanin et al.58 hanno eseguito uno studio in vitro sull’applicazione della aPDT su biofilm orali formati in maniera naturale in vivo. L’applicazione di blu di toluidina e un diodo emettente luce rossa (620-660 nm) ha determinato una riduzione delle cellule batteriche fino al 99% all’interno del biofilm. Attività battericida è stata dimostrata in vitro55 e in modello animale59 anche su P. gingivalis e per biofilm di A. actinomycetemcomitans60. Studi clinici longitudinali su pazienti parodontali trattati con terapia non-chirurgica e terapia fotodinamica aggiuntiva, e nei quali sono stati prelevati anche campioni microbiologici dalle tasche parodontali, hanno mostrato risultati contrastanti. Polansky et al.61 non hanno mostrato differenze significative nei parametri microbiologici se al trattamento non chirurgico di pazienti affetti da parodontite cronica veniva aggiunta una singola applicazione di aPDT. Viceversa, Chondros et al.62 hanno potuto notare che la terapia aggiuntiva con aPDT determina una maggiore riduzione delle specie di Fusobacterium nucleatum ed Eubacterium nodatum a 3 mesi e di Eikenella corrodens e Capnocytophaga a 6 mesi rispetto alla sola terapia meccanica. In pazienti con parodontite cronica localizzata, con infezione sostenuta da F. nucleatum e trattati con scaling e root planing, un’unica applicazione di aPDT è stata in grado di ridurre significativamente la concentrazione di questo patogeno rispetto ai valori iniziali63.
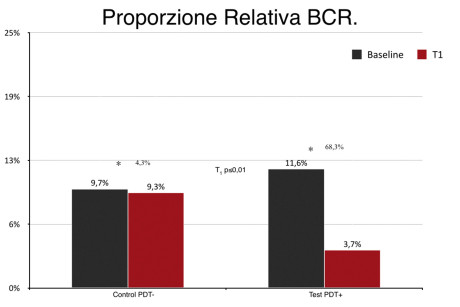
In tasche residue di pazienti parodontali in terapia di supporto, trattate con strumenti ultrasonici o con terapia fotodinamica, Rühling et al.64 pur ottenendo una riduzione immediata della carica patogena sottogengivale non sono riusciti a mantenere visibile questa differenza più di tre mesi. Il nostro gruppo di ricerca, presso l’Università Sapienza di Roma, ha condotto recentemente il primo studio clinico longitudinale nel quale è stata testata una lampada LED (Fotosan®, CMS Dental, Copenhagen, Danimarca), con emissione di onda luminosa non coerente a una frequenza di 635 nm, per applicazioni fotodinamiche65. Rispetto ai soft laser, quali i laser a diodi, questa lampada presenta vantaggi di aspetto ergonomico, di irradiazione (luce non puntiforme ma diffusa) ed economici. In questo studio split mouth, randomizzato controllato e condotto in cieco, sono stati arruolati 30 pazienti - trattati per parodontite cronica e in terapia di supporto parodontale da un anno - nei quali erano presenti almeno due tasche residue con profondità di sondaggio (PPD) di almeno 5 mm, in due quadranti opposti, e con positività al sanguinamento al sondaggio. Entrambi i siti sono stati trattati con scaling e root-planing e, dopo randomizzazione, una tasca è stata ulteriormente trattata con la terapia fotodinamica, in questo caso denominata LAD (Disinfezione Attivata dalla Luce), mentre quella residua è stata mantenuta come controllo. Da questi siti sono stati prelevati, alla baseline e una settimana dopo il trattamento, dei campioni di placca sottogengivale e analizzati con tecnica PCR real-time. I risultati di queste analisi hanno mostrato una maggiore riduzione delle proporzioni relative dei batteri del complesso rosso nelle tasche trattate con LAD rispetto a quelle in cui si è intervenuto con la sola terapia meccanica: mentre nei siti controllo si aveva una riduzione del complesso rosso del 4,1%, nei siti test la riduzione ha raggiunto una riduzione pari a oltre il 68% (Figura 4).
Risultati clinici
Nei pazienti affetti da parodontite, il primo approccio terapeutico è legato alla rimozione degli agenti patogeni alla base dell’infezione parodontale. Comunemente chiamata “terapia parodontale di fase 1” o “terapia parodontale eziologica o causale”, questa si basa sulla combinazione della motivazione del paziente alle corrette manovre di igiene orale domiciliare e la rimozione del biofilm dentale e del tartaro dalle superfici radicolari dei denti interessati dalla malattia, con lo scaling e la levigatura radicolare. Questo approccio terapeutico iniziale determina nell’arco di un breve periodo di tempo (4-6 settimane) una riduzione degli indici clinici della malattia: sanguinamento al sondaggio (BOP), profondità di sondaggio (PPD) e livello di attacco clinico (CAL). Generalmente questi effetti clinici positivi possono essere mantenuti se i pazienti vengono seguiti con una terapia parodontale di supporto, fatta da un sistema di richiami periodici ben strutturato (SPT)21. La terapia fotodinamica, in aggiunta alla terapia meccanica, si pone come obiettivo quello di determinare un ulteriore miglioramento di questi indici clinici e quindi ridurre la necessità di ulteriori trattamenti parodontali, quali la chirurgia. Per determinare l’effetto clinico aggiuntivo di tale terapia sono stati attuati, nel corso degli ultimi 15 anni, degli studi clinici longitudinali. Dal punto di vista dei risultati clinici le pubblicazioni scientifiche hanno prodotto risultati discordanti tra loro. Molti degli studi clinici hanno osservato una maggiore riduzione del sanguinamento al sondaggio quando la aPDT viene associata allo SRP, rispetto alla sola terapia meccanica.
Christodoulides et al.66 hanno seguito 24 pazienti affetti da parodontite cronica trattati con scaling e root planing seguito da una singola applicazione di aPDT o solo con scaling e root planing. Gli Autori hanno dimostrato un miglioramento significativo del Full Mouth Bleeding Score per i pazienti del trattamento combinato, sia a 3 che a 6 mesi di follow-up. De Olivera et al.67, in uno studio clinico split-mouth, hanno osservato lo stesso trend anche nei pazienti affetti da parodontite aggressiva. In termini di riduzione della PPD gli studi longitudinali, mettendo a confronto la aPDT + SRP rispetto alla sola terapia meccanica non chirurgica, hanno mostrato risultati discordanti8. Alcuni lavori più recenti, tuttavia, hanno mostrato, in pazienti parodontali trattati con terapia causale, riduzioni di PPD più favorevoli se a questa veniva aggiunta una singola applicazione di terapia fotodinamica68,69. Andersen et al.70 hanno valutato gli effetti clinici della terapia fotodinamica antimicrobica aggiuntiva allo SRP su 33 pazienti affetti da parodontite per un periodo di 12 settimane. Il PPD, il CAL e il BOP sono stati seguiti negli intervalli di 3, 6 e 12 settimane e il gruppo che aveva effettuato la terapia combinata di SRP + aPDT ha mostrato indici clinici significativamente migliori anche dopo un periodo di 12 settimane rispetto ai gruppi che avevano fatto solo SRP o solo aPDT. Negli ultimi anni sono anche state pubblicate in letteratura delle revisioni sistematiche con meta-analisi degli studi clinici longitudinali in materia di trattamento parodontale e terapia fotodinamica.
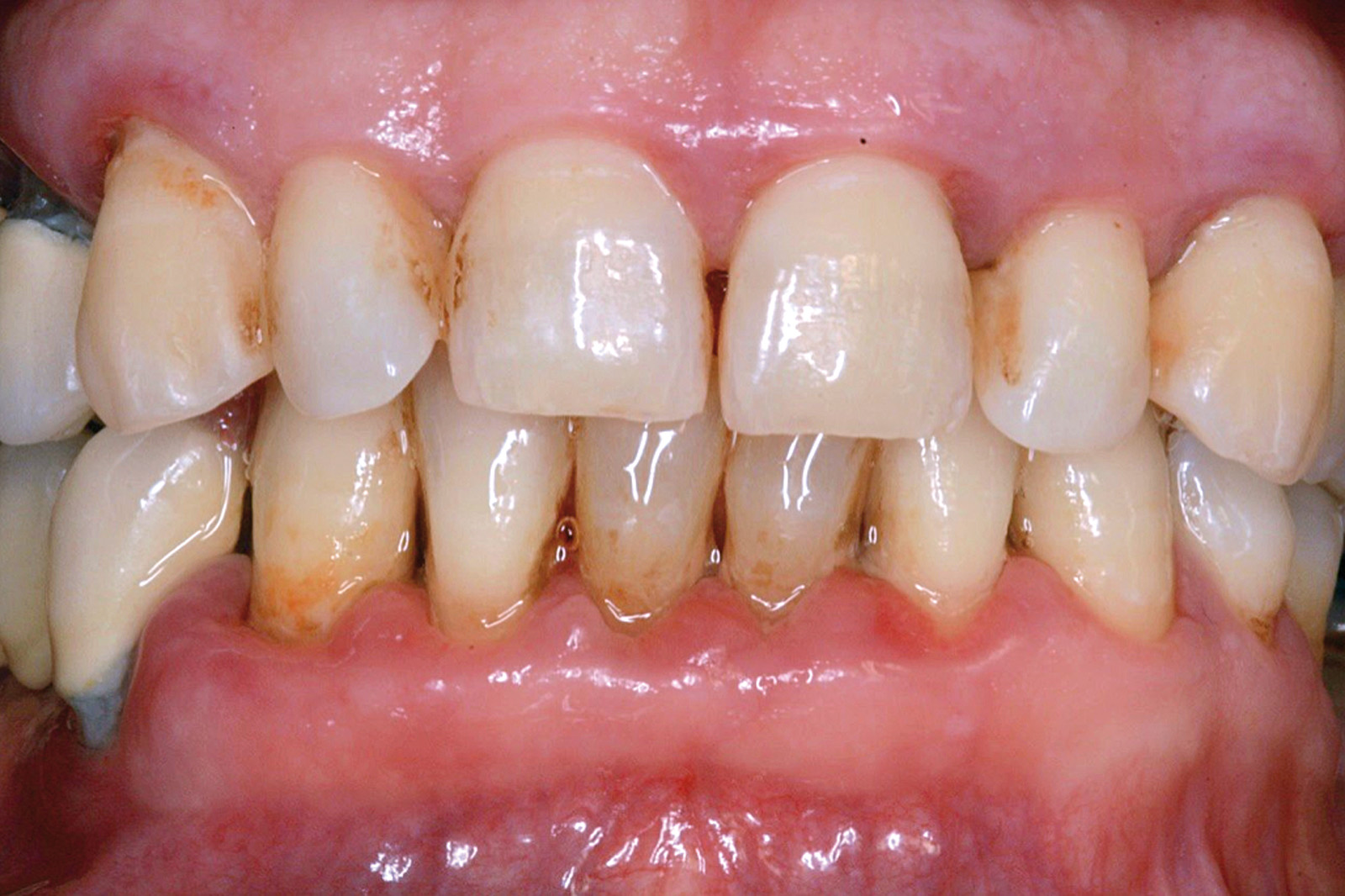
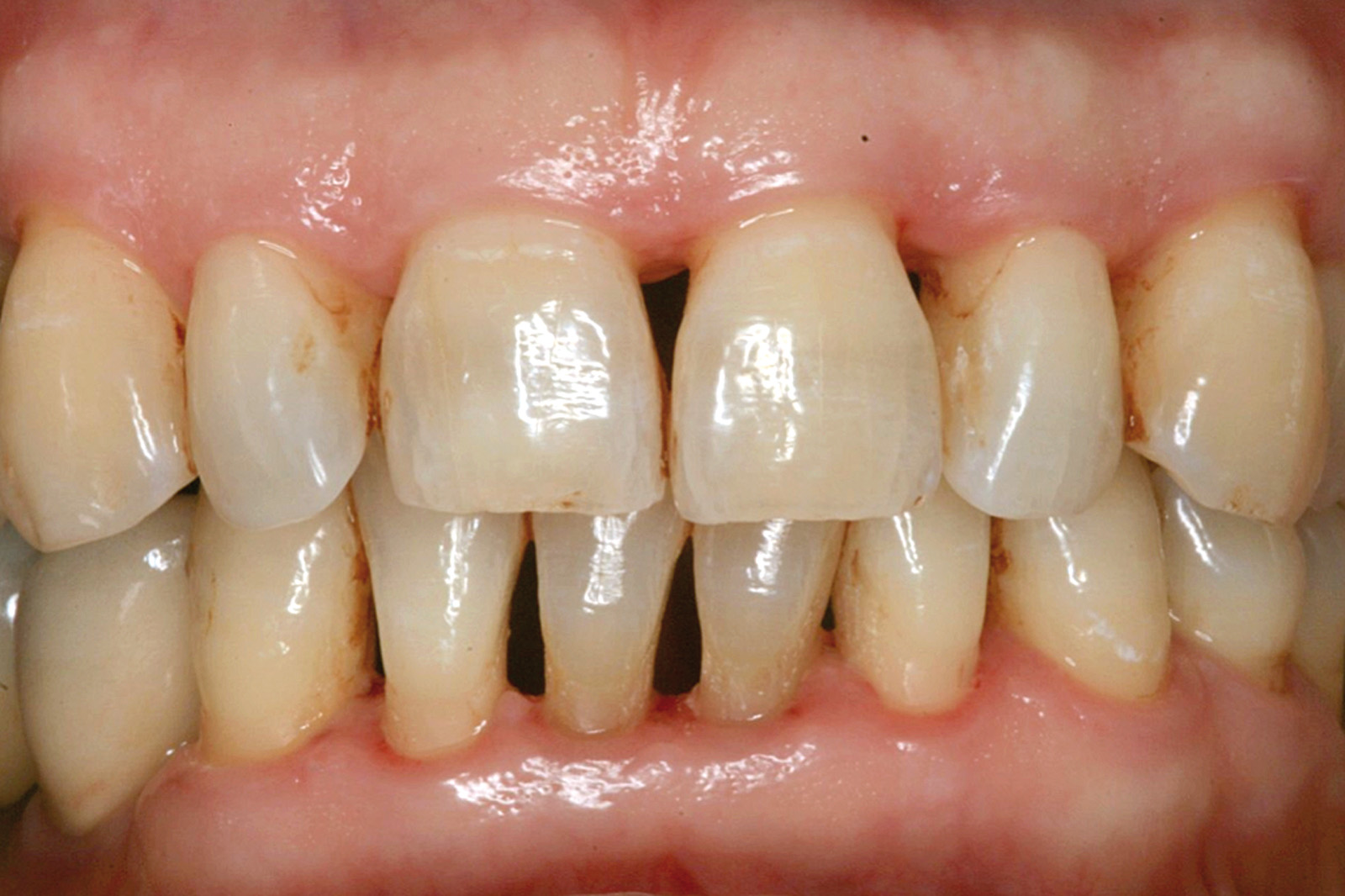
I dati che si possono evidenziare da queste revisioni indicano che il trattamento della parodontite cronica con PDT da sola rispetto al trattamento convenzionale con SRP non sembra mostrare alcun beneficio aggiuntivo71-73. Al contrario, quando la PDT viene impiegata assieme allo SRP i dati sembrano mostrare un beneficio clinico aggiuntivo positivo, specialmente nelle lesioni con condizioni anatomiche sfavorevoli71-73, sebbene esistano differenze tra studi a gruppi paralleli e studi nei quali è stata applicata una metodologia split-mouth73. Nelle Figure 5-8 riportiamo il caso di una paziente affetta da parodontite cronica avanzata generalizzata, trattata con terapia parodontale non chirurgica con l’aggiunta della terapia LAD per quelle tasche con profondità di sondaggio iniziale > 4 mm. In generale gli effetti della terapia parodontale causale non-chirurgica si riscontrano dopo poche settimane dal trattamento, ma nei casi inizialmente più avanzati possono persistere tasche residue che necessitano di ulteriore trattamento. Matuliene et al.15 hanno dimostrato che la persistenza di tasche residue profonde (PPD > 4 mm) al termine della fase attiva del trattamento parodontale e al momento dell’inserimento del paziente in terapia di supporto (SPT) rappresenta un rischio maggiore di progressione della parodontite nel tempo e in definitiva della perdita dell’elemento dentario. Il rischio aumenta ulteriormente se allo stesso tempo la tasca residua profonda presenta anche sanguinamento al sondaggio. Sembra quindi ragionevole utilizzare la terapia fotodinamica nel trattamento delle tasche residue nei pazienti in terapia di supporto parodontale. Alcuni studi hanno preso in considerazione gli effetti della aPDT in queste situazioni.
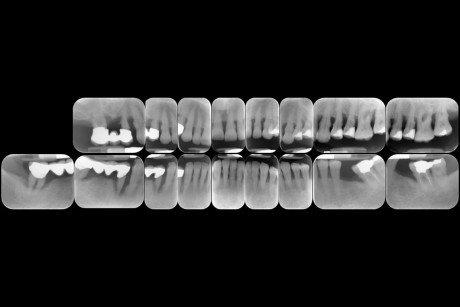
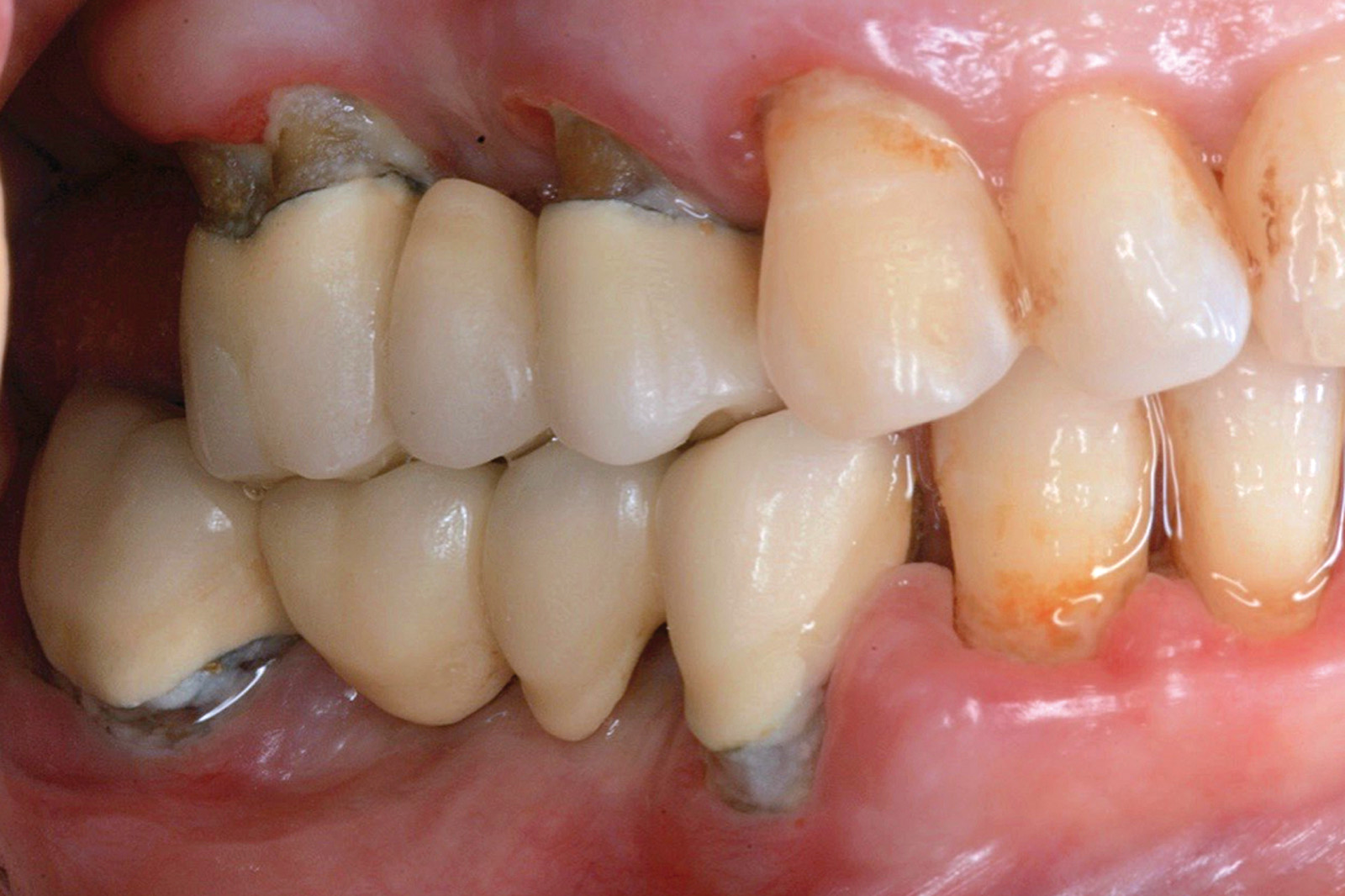
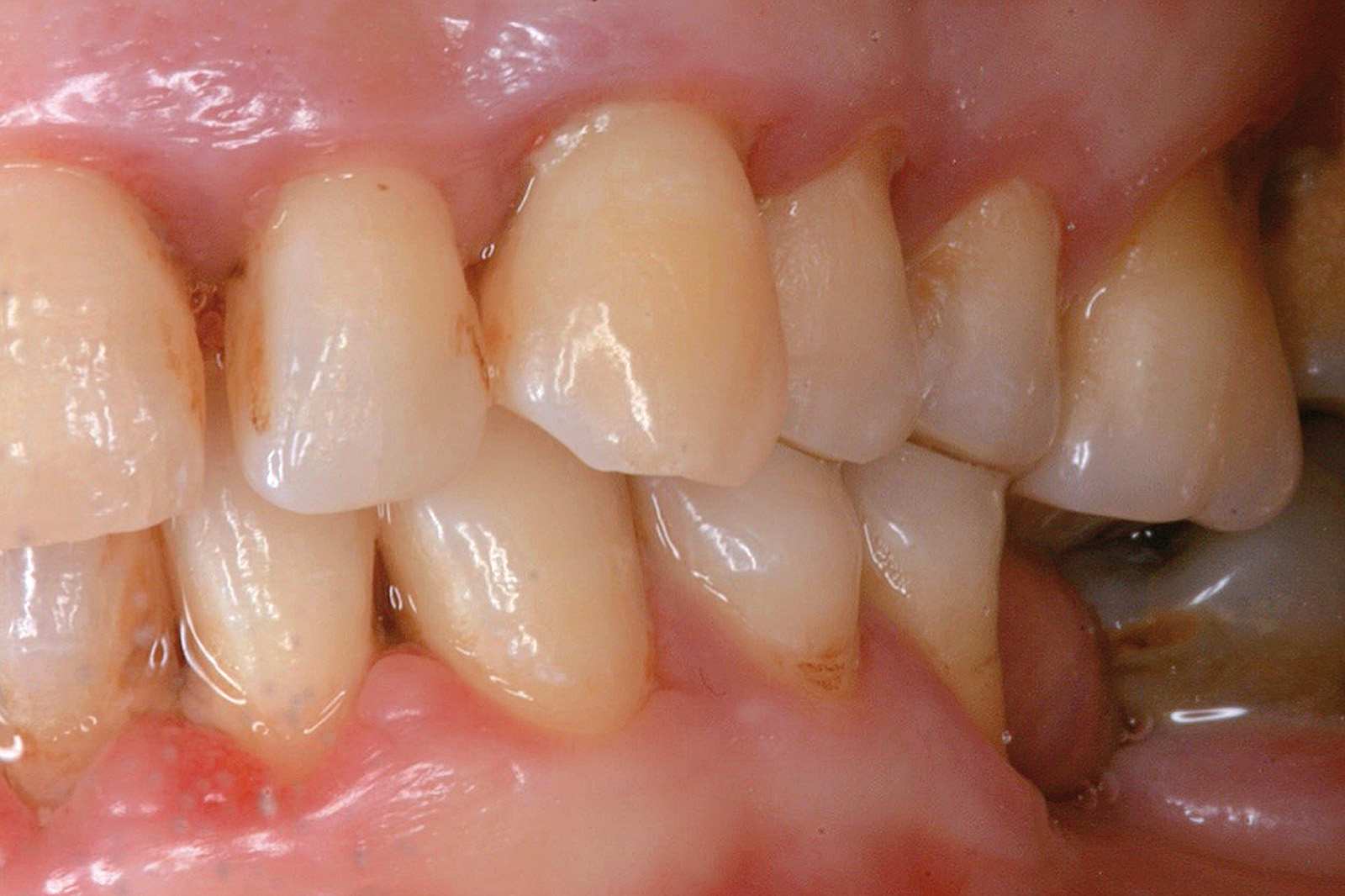
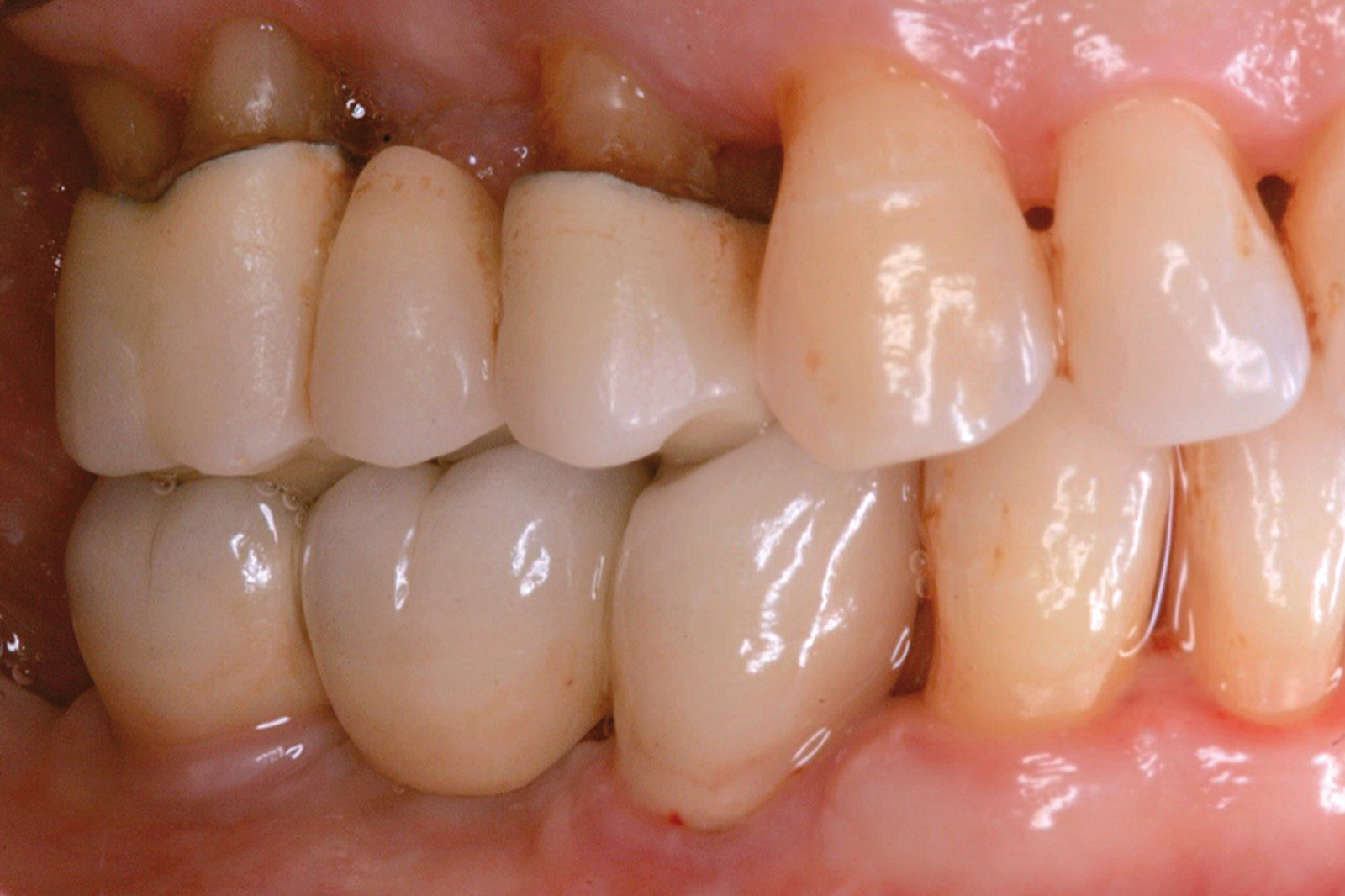
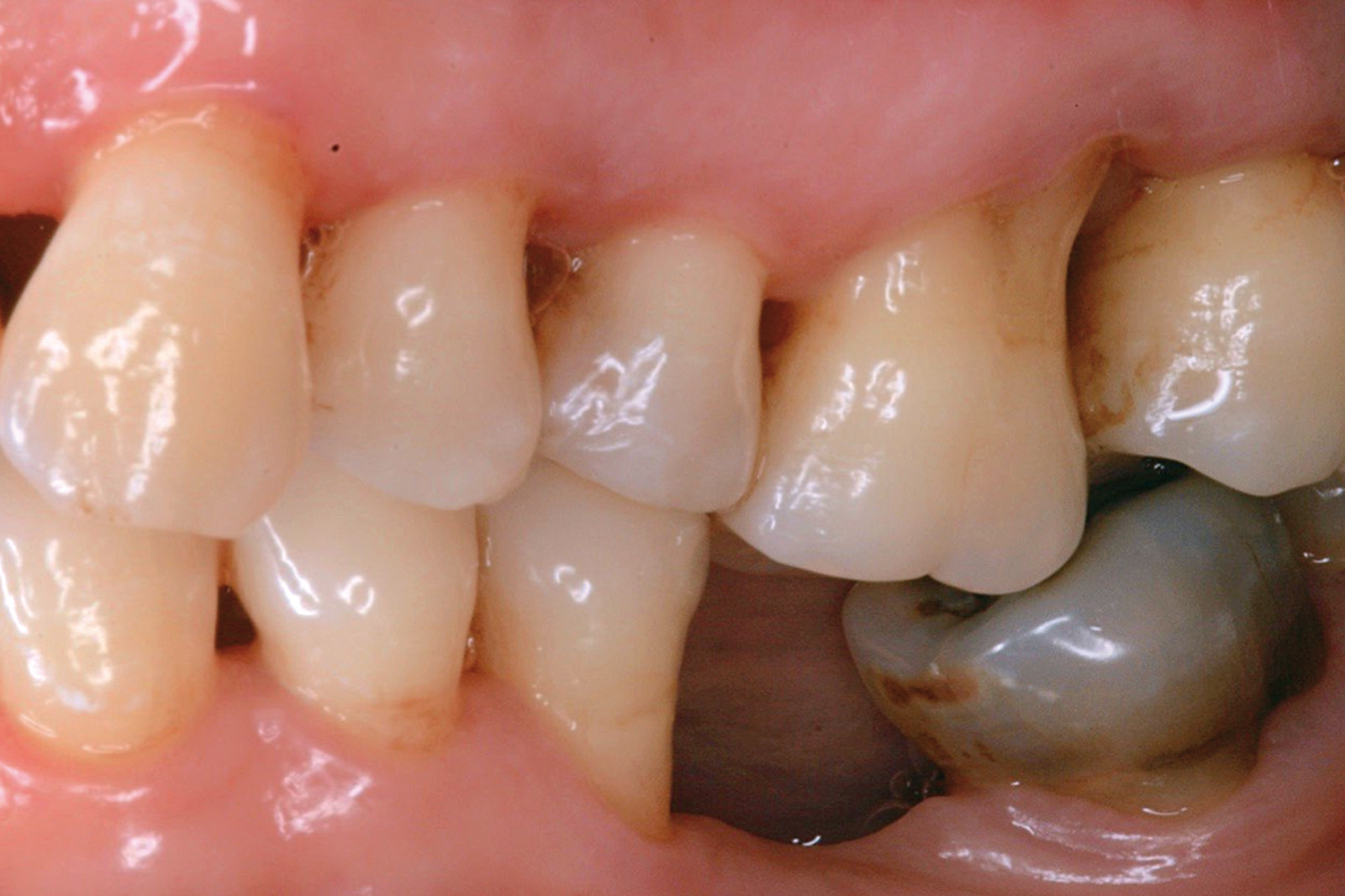
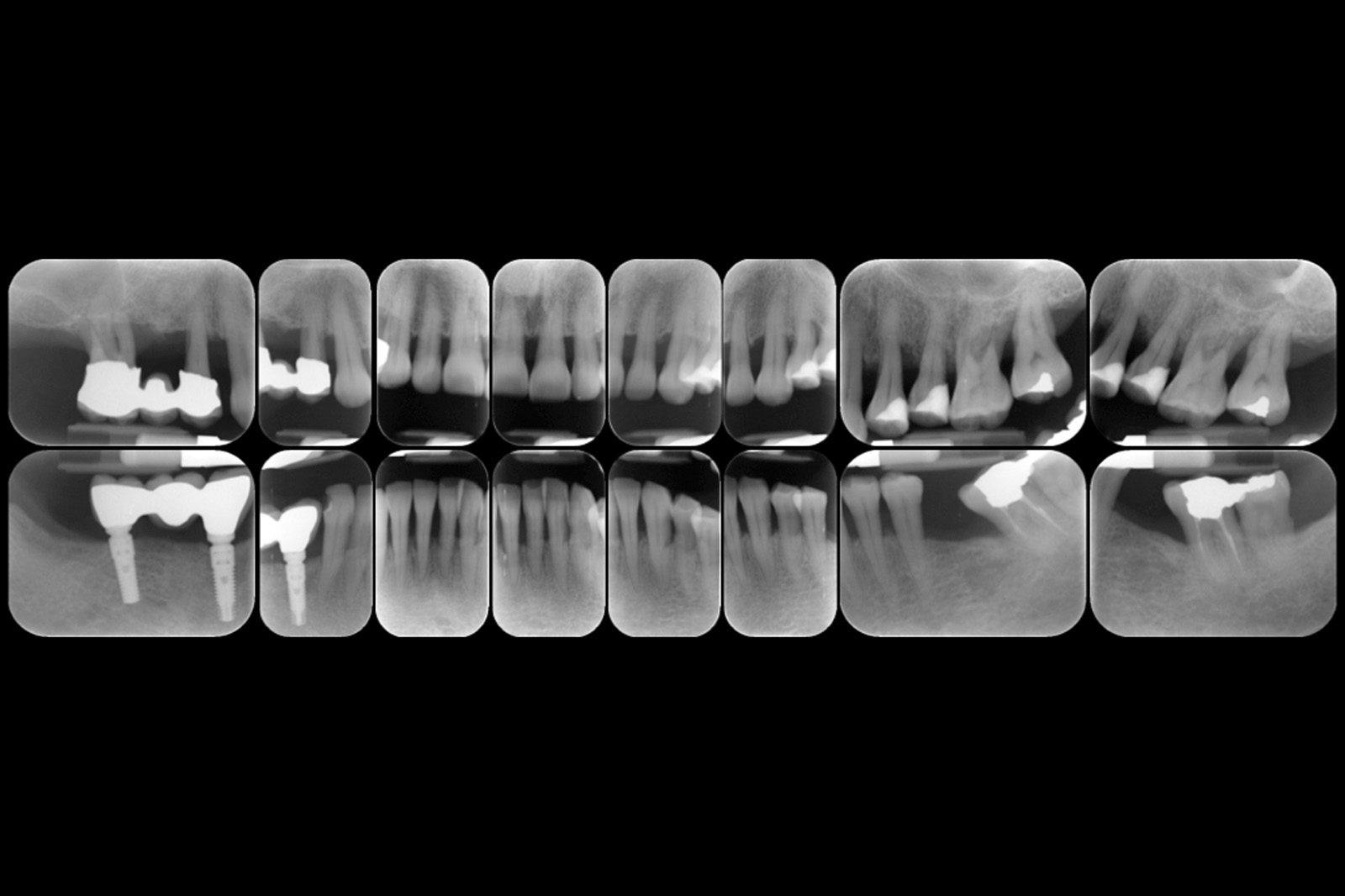
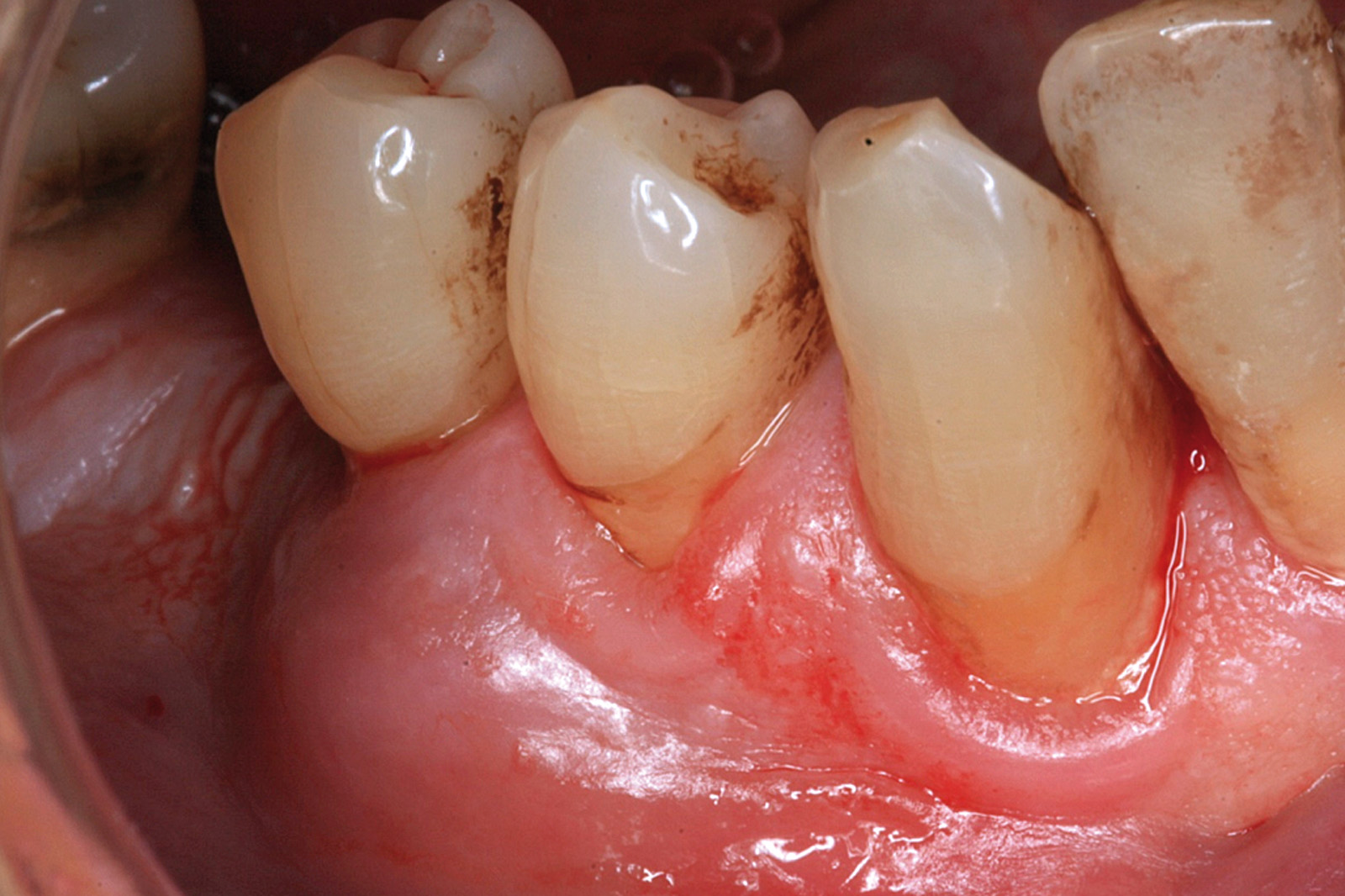
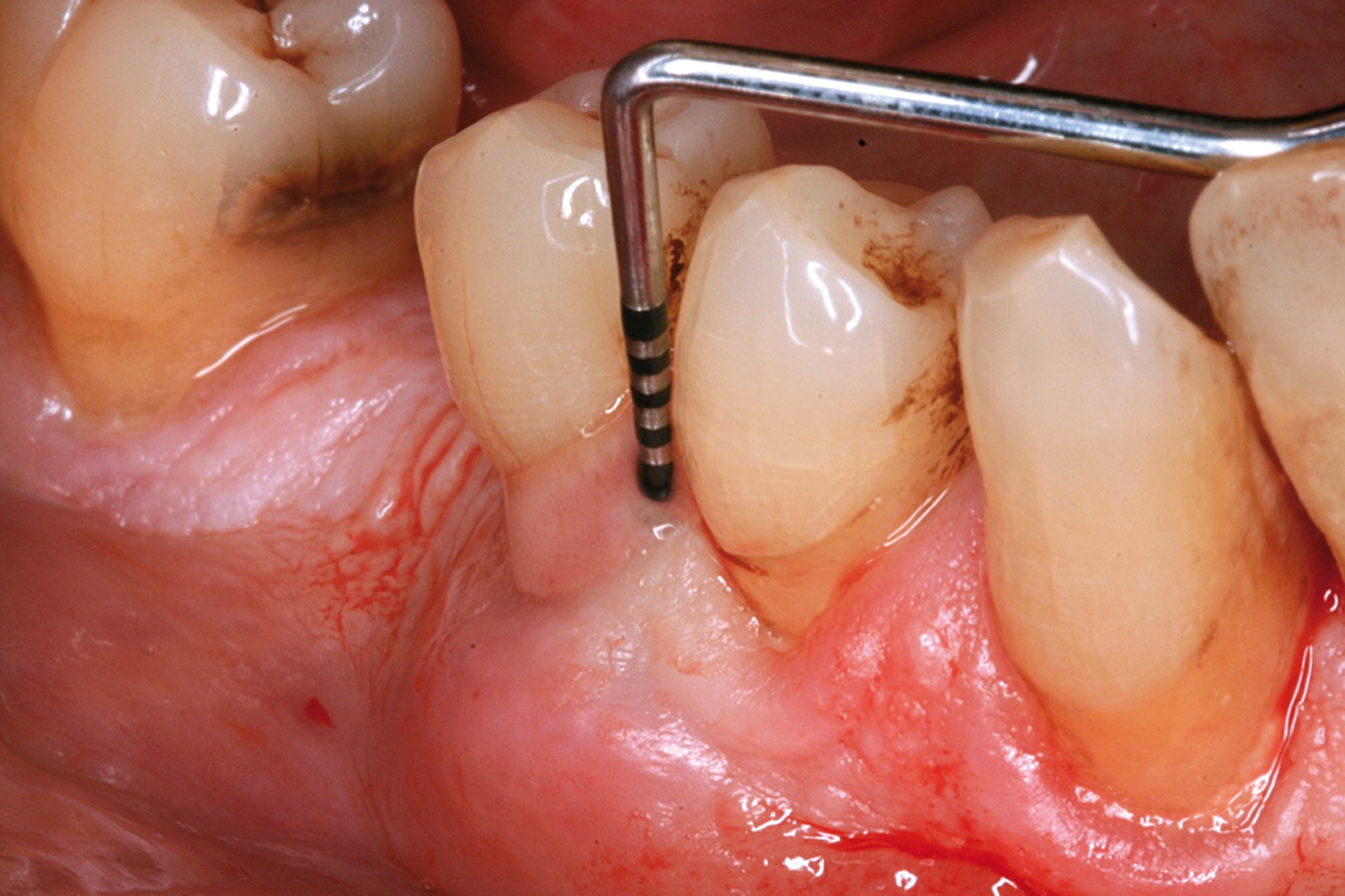
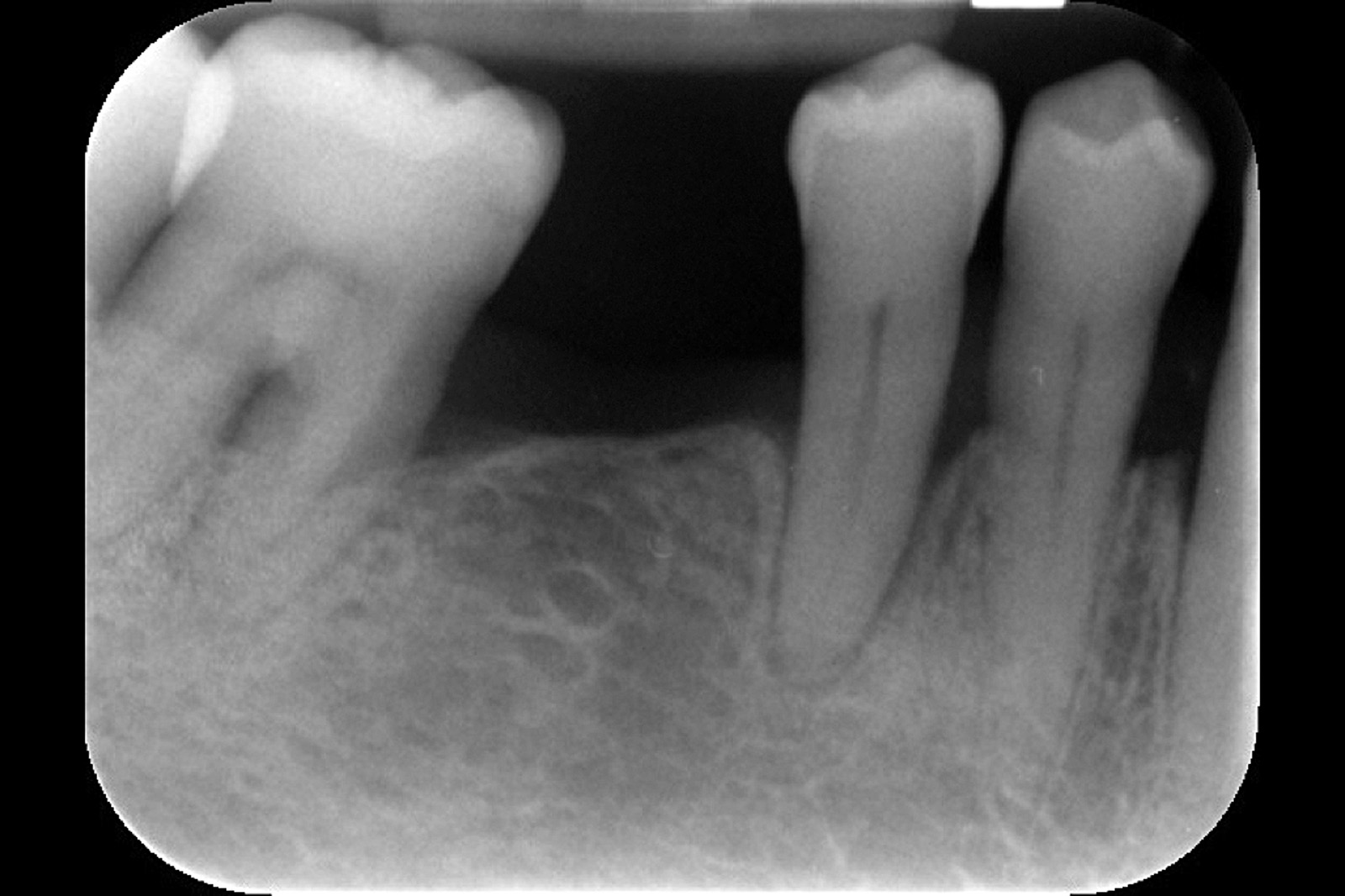
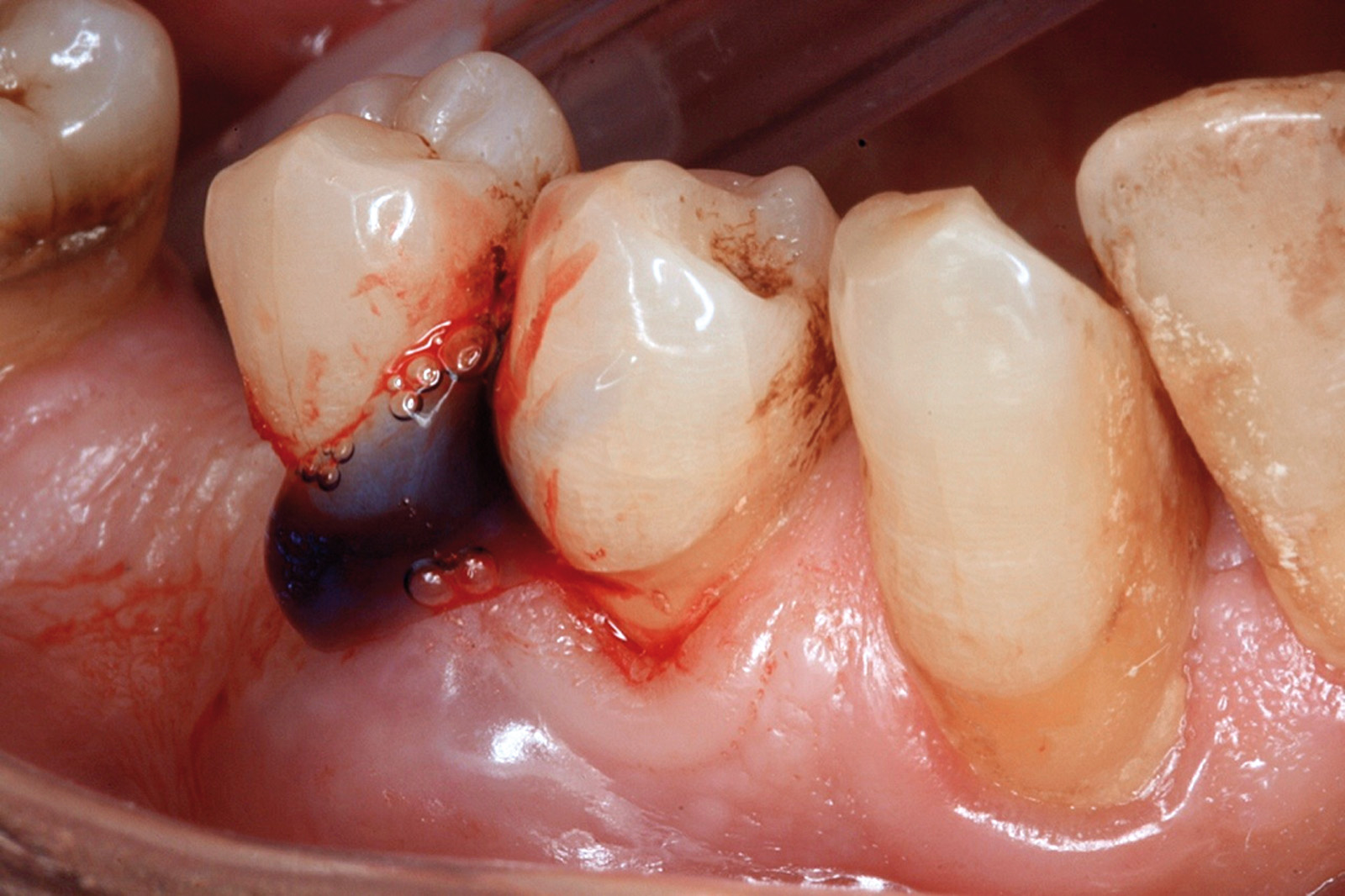
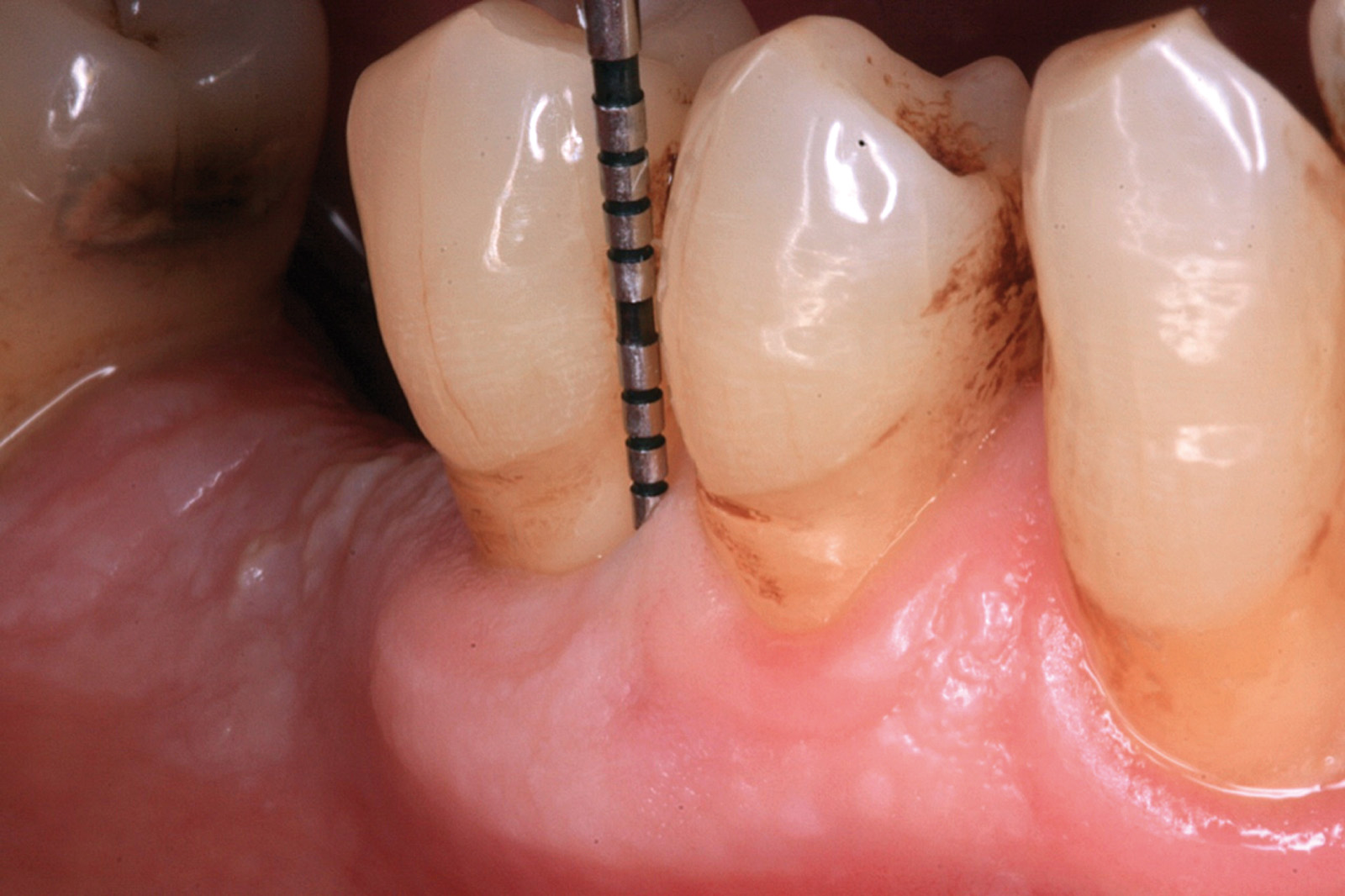
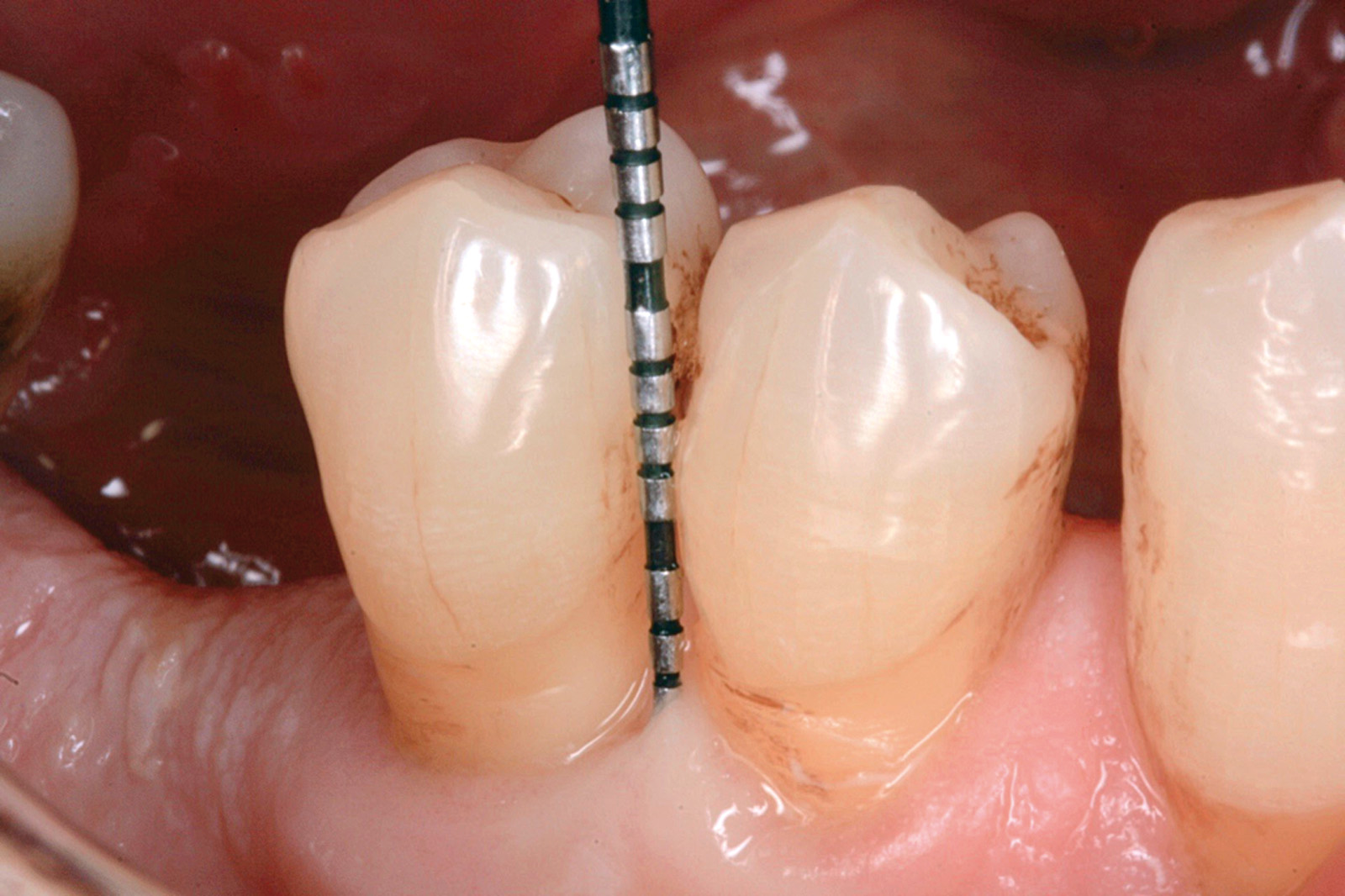
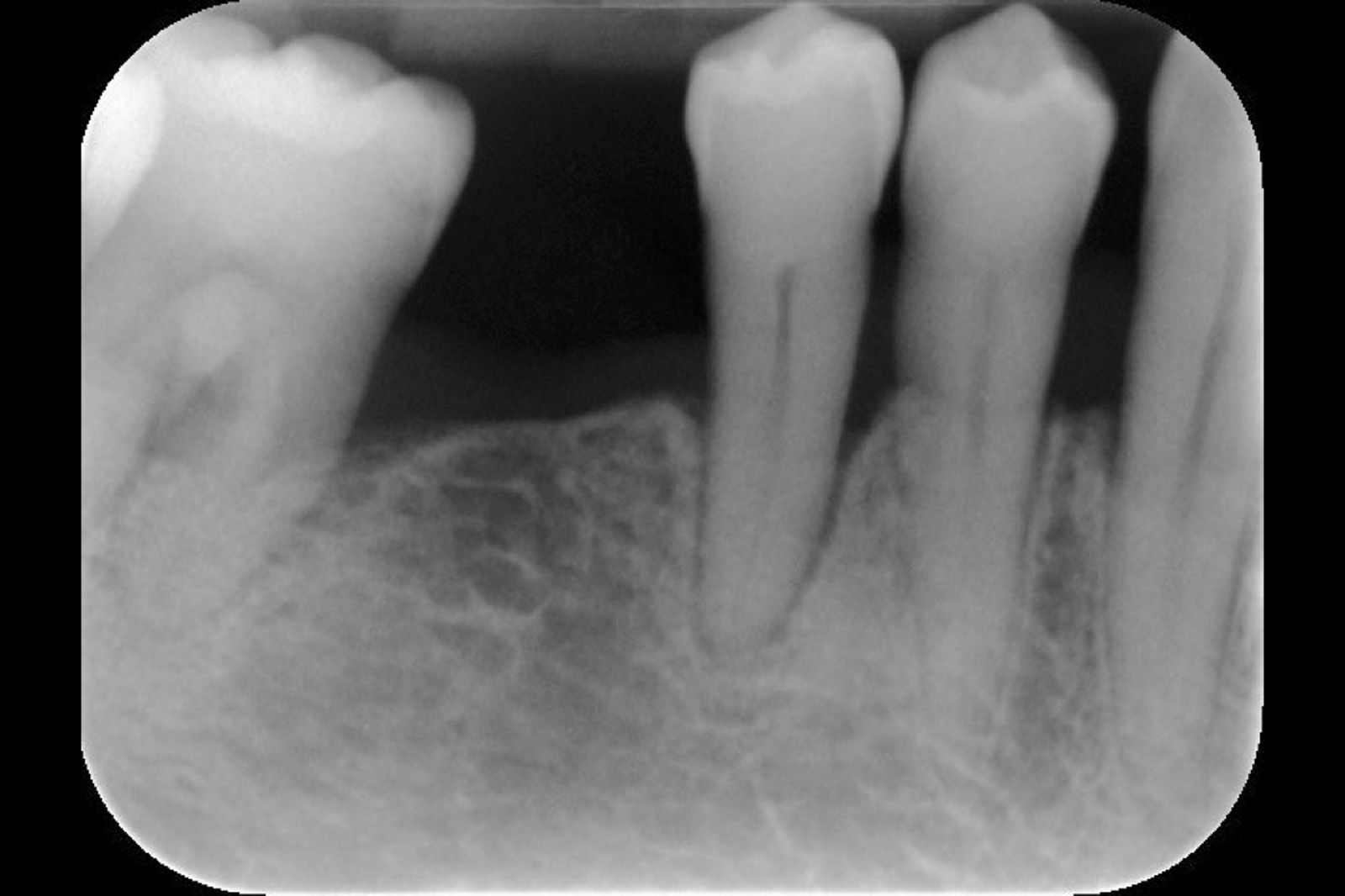
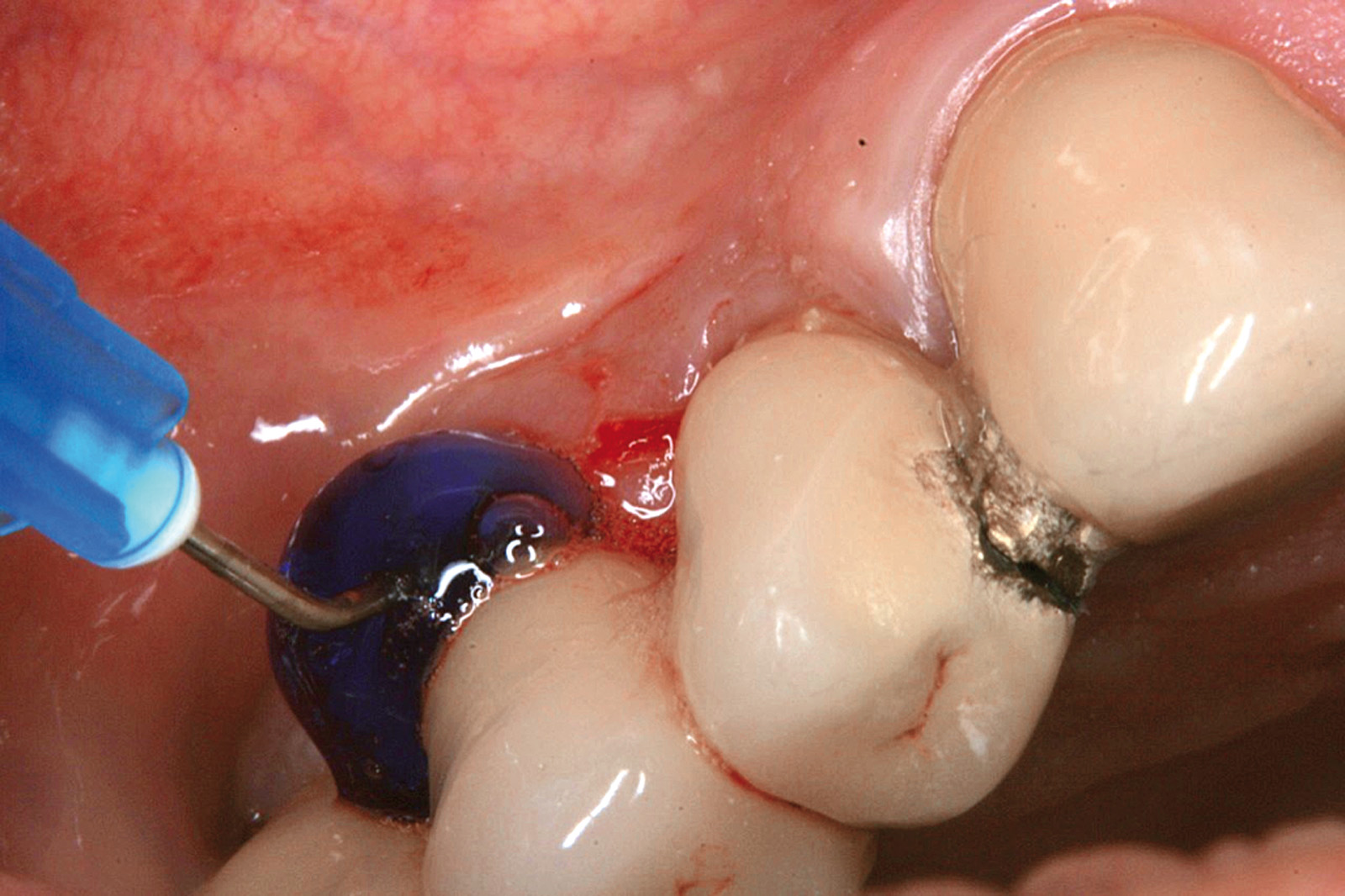
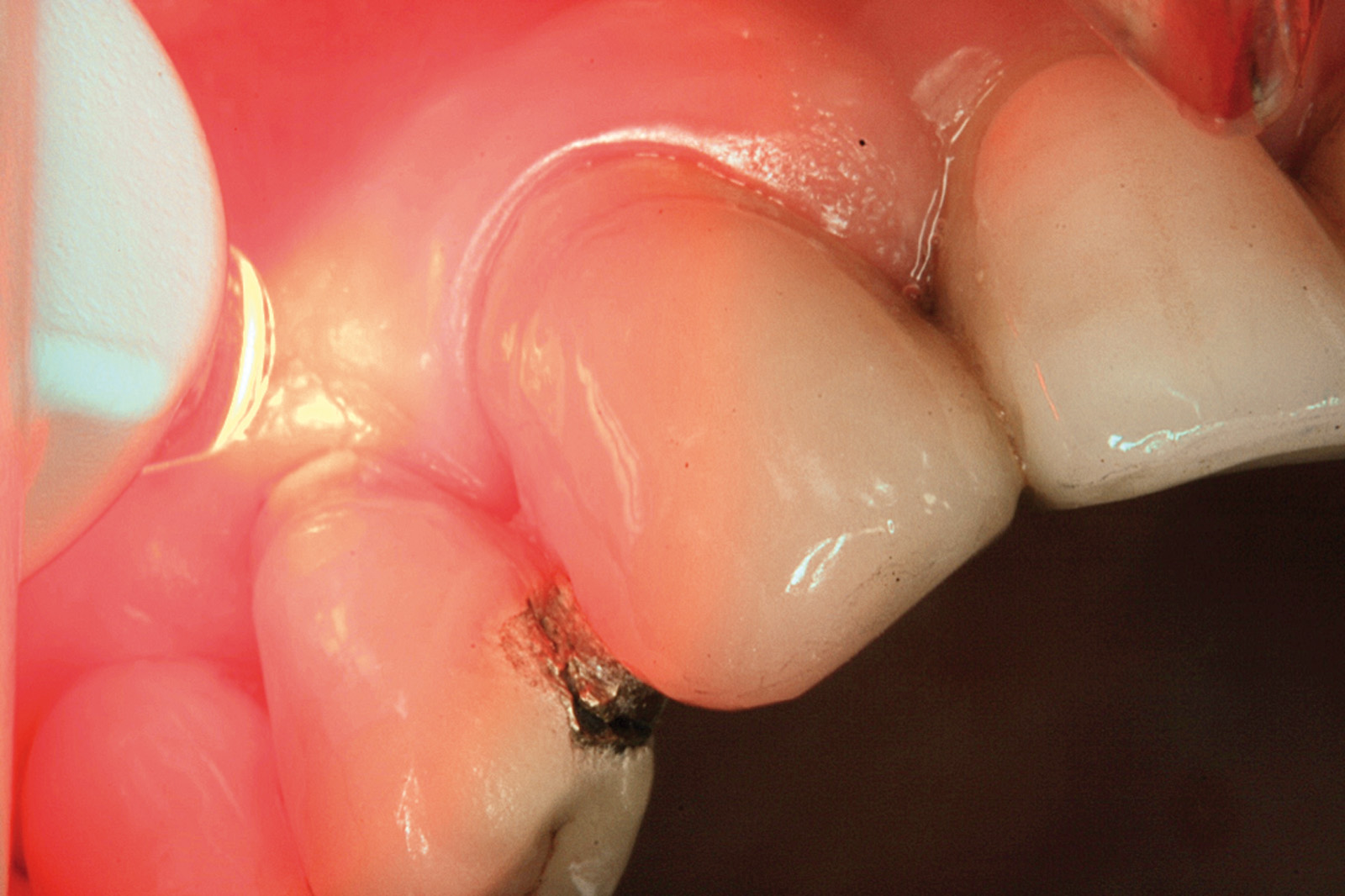
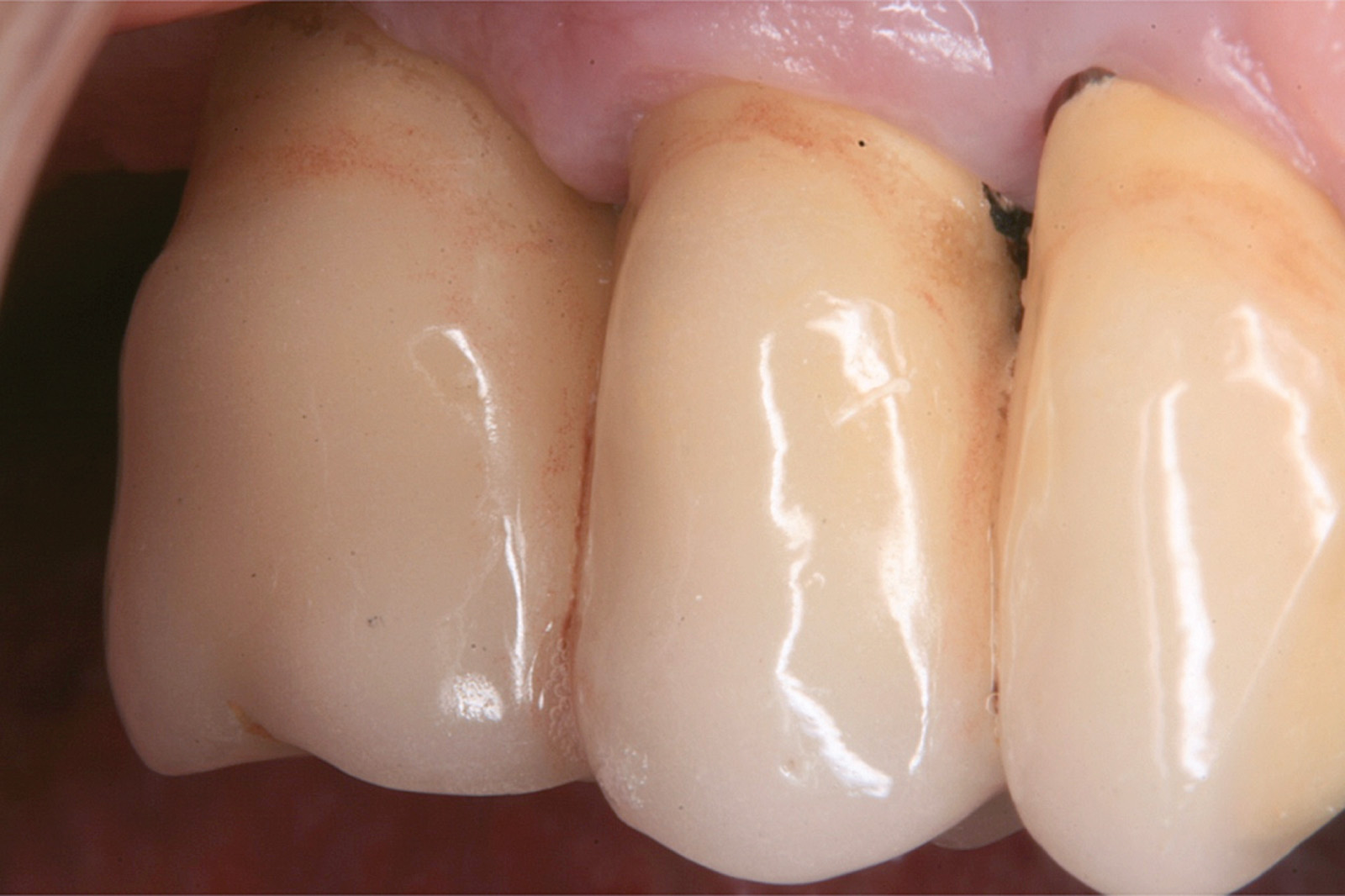
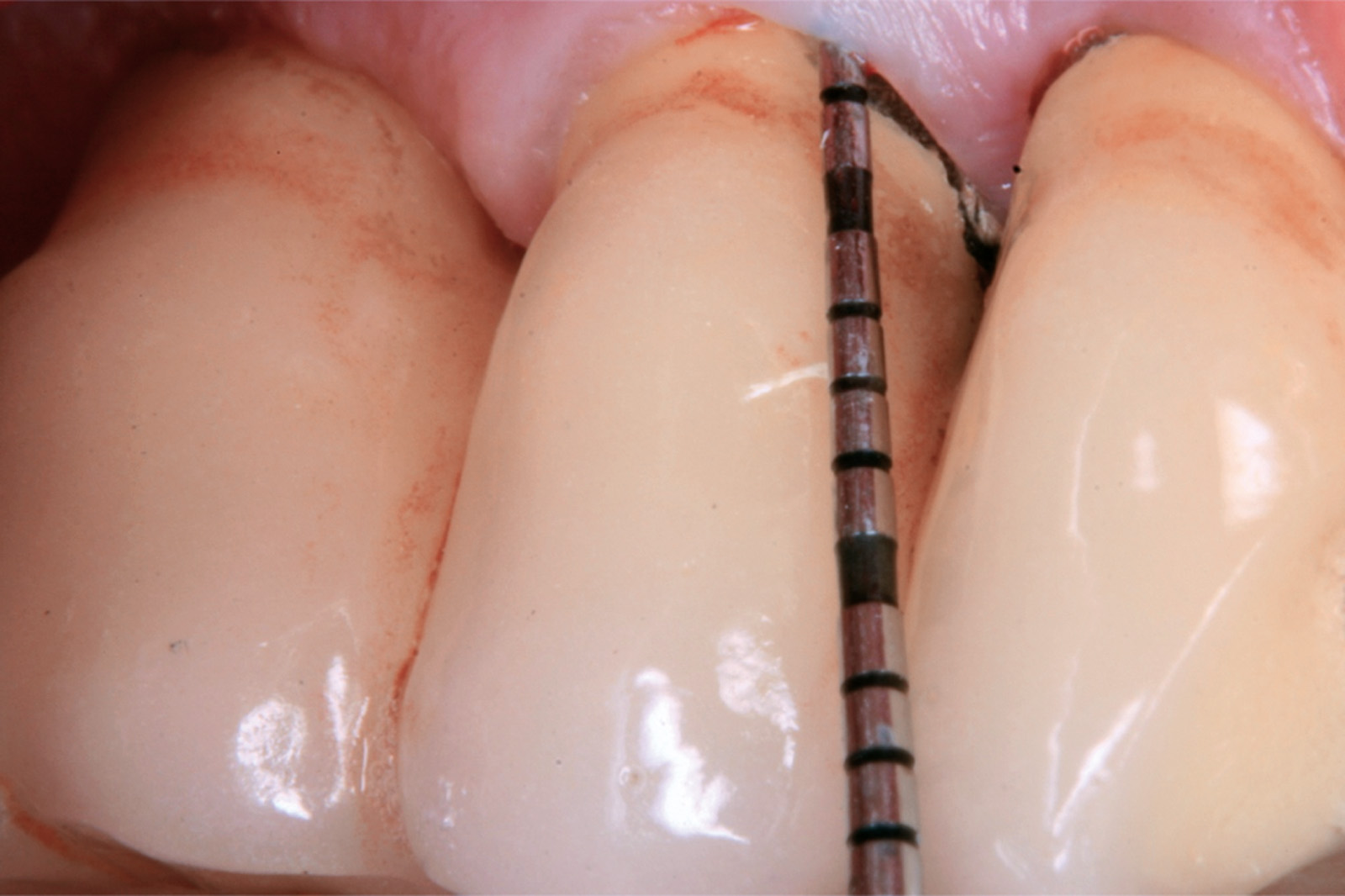
Chondros et al.62 hanno dimostrato che una singola applicazione di aPDT combinata con lo SRP in pazienti in SPT determina una significativa maggiore riduzione del BOP rispetto alla sola terapia meccanica, ma queste differenze non erano visibili in termini di riduzione della PPD. Rühling et al.64 in uno studio clinico randomizzato su pazienti con parodontite cronica trattata in SPT, ma utilizzando un fotosensibilizzante e un laser diversi, non hanno trovato alcuna differenza statistica né in termini di BOP né in altri parametri clinici. Più recentemente il nostro gruppo65 ha potuto dimostrare che utilizzando come fotosensibilizzante il blu di toluidina e una lampada LED come fonte di energia luminosa a lunghezza d’onda di 635 nm in tasche residue con PPD > 4 mm in pazienti in terapia di mantenimento, si ottengono migliori risultati clinici rispetto alla terapia convenzionale. In termini di riduzione del BOP il 73% delle tasche trattate con SRP+LAD non presentava più sanguinamento rispetto al 27% delle tasche trattate con SRP solamente. In termini di riduzione di PPD, i siti che avevano ricevuto anche terapia fotodinamica presentavano una maggiore riduzione media della profondità di tasca (+ 0,5 mm) e un maggior numero di siti che riducevano la profondità di oltre 2 mm. Risultati simili sono stati ottenuti da Campos et al.74 e Cappuyns et al.75. Le Figure 9-12 illustrano il caso di un paziente forte fumatore, affetto da parodontite cronica generalizzata di grado avanzato, trattato e inserito in terapia di mantenimento. In una delle sedute periodiche si presenta con un ascesso parodontale a carico dell’elemento 4.5 che viene trattato con scaling e root planing e terapia LAD aggiuntiva. Si nota l’ottimo risultato clinico sia nel breve (1 settimana) che nel medio periodo (3 mesi).
Conclusioni
La terapia fotodinamica, sebbene basata su principi la cui scoperta risale a oltre un secolo fa, ha trovato negli ultimi decenni nuova attenzione clinica per svariati campi di applicazione. Oltre a trattamenti diretti a patologie neoplastiche, dermatologiche e oftalmiche, negli ultimi anni si è sempre più puntata l’attenzione sulle possibilità di utilizzo nel trattamento delle infezioni. In campo odontoiatrico la ricerca di base e la ricerca clinica si sono soprattutto soffermate al campo endodontico e alle applicazioni parodontali. I risultati discordanti in merito all’utilità o meno di questa recente metodica di trattamento delle infezioni parodontali sono dovuti molto probabilmente a diversi fattori, spesso concomitanti. I diversi fotosensibilizzanti utilizzati, le differenti apparecchiature impiegate per la produzione di energia luminosa, le diverse lunghezze d’onda e la durata dell’esposizione alla luce, sono tutte variabili che possono spiegare i discordanti risultati ottenuti nei vari studi. Inoltre, anche il numero di applicazioni, singole o ripetute, il settaggio dei laser, il tempo di contatto del fotosensibilizzante nell’ambiente sottogengivale possono avere una influenza sui parametri clinici legati al trattamento parodontale e dare ragione delle differenze che si riscontrano nei vari studi clinici.
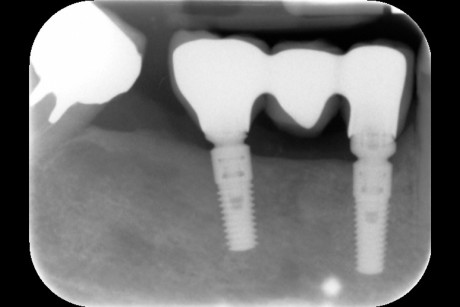
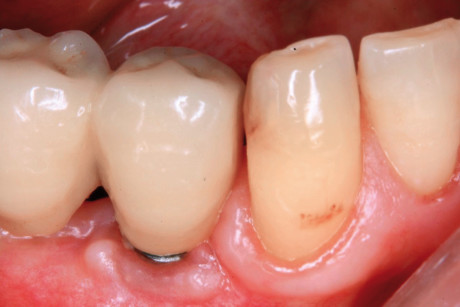
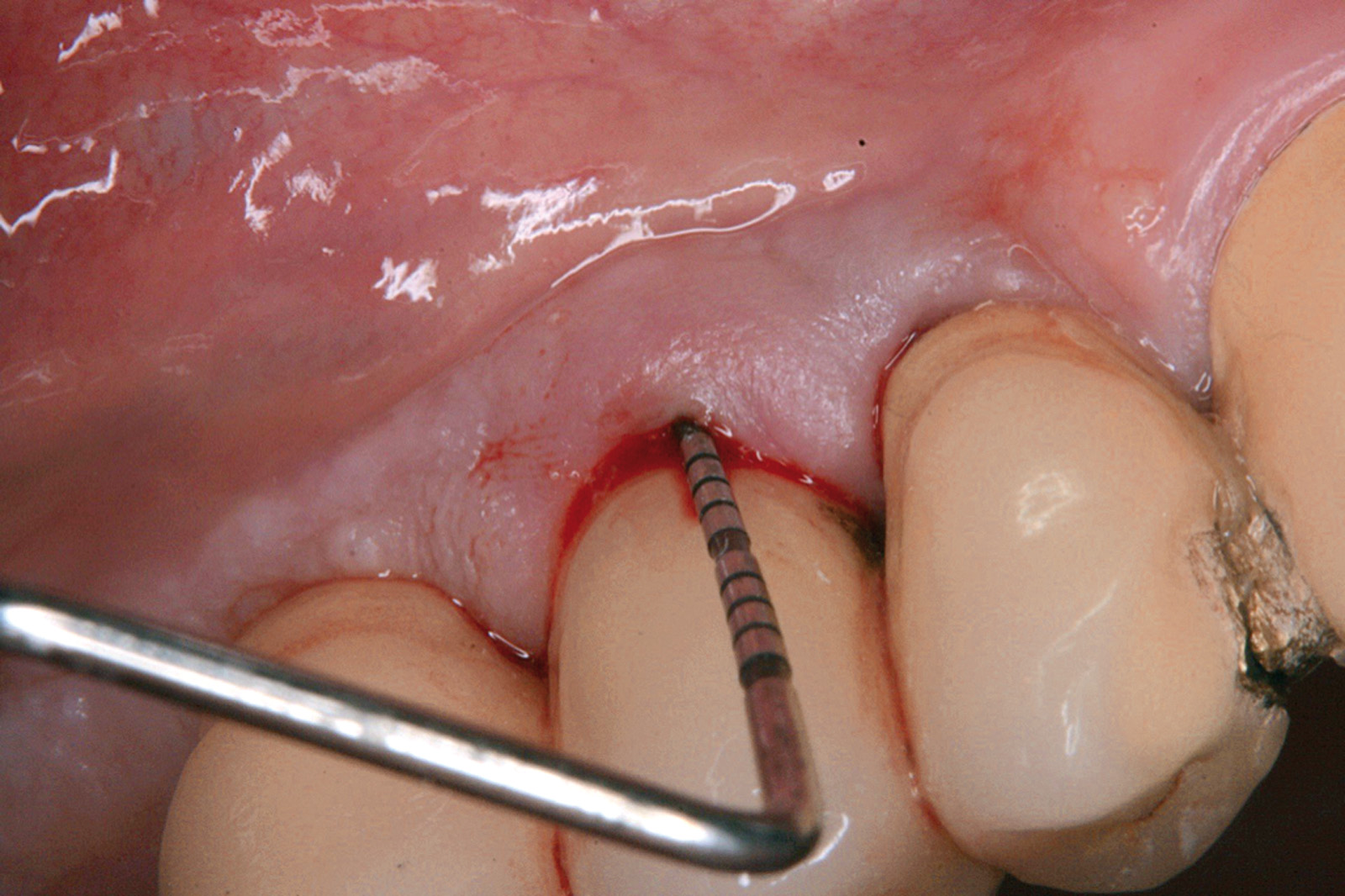
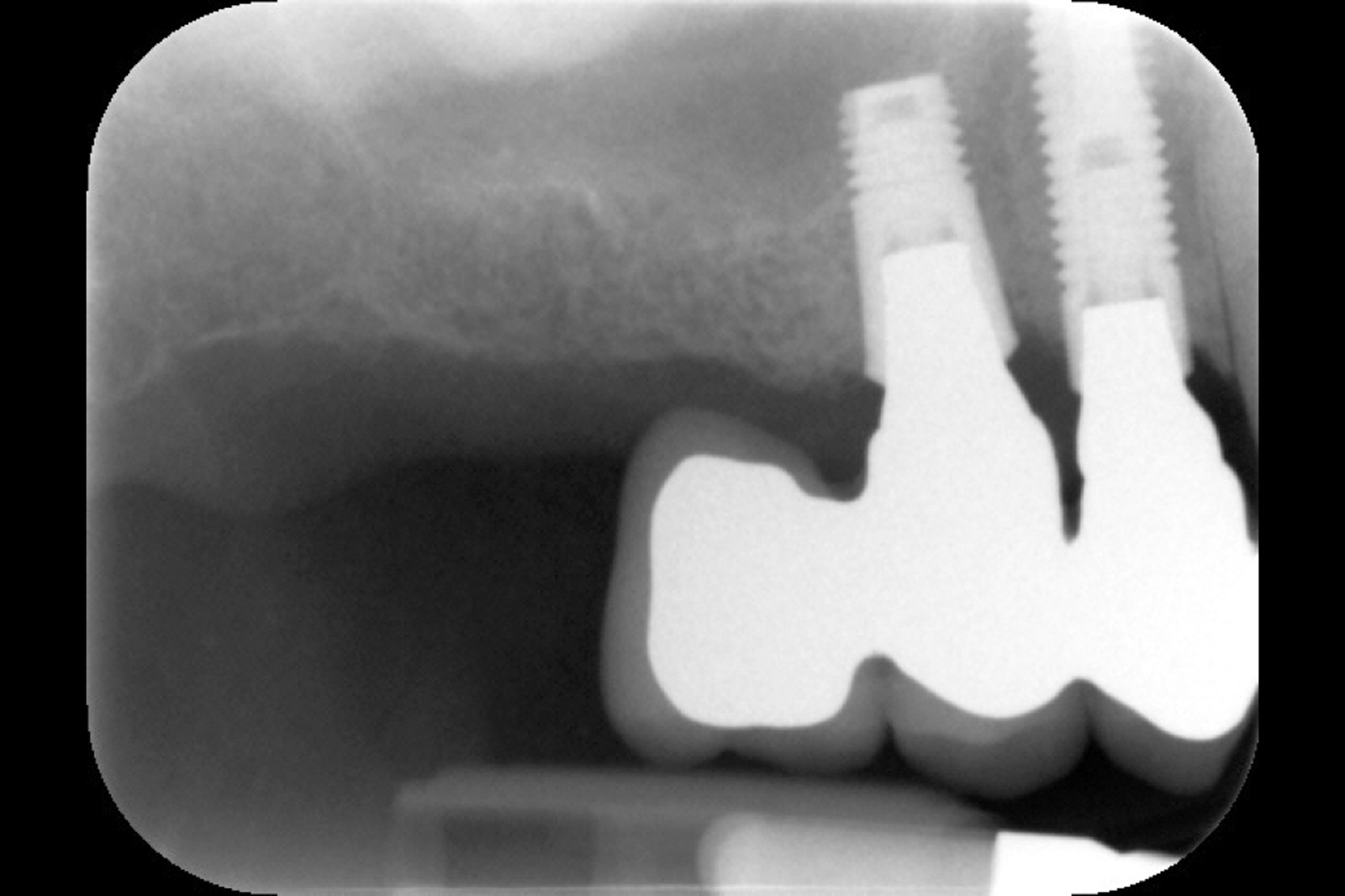
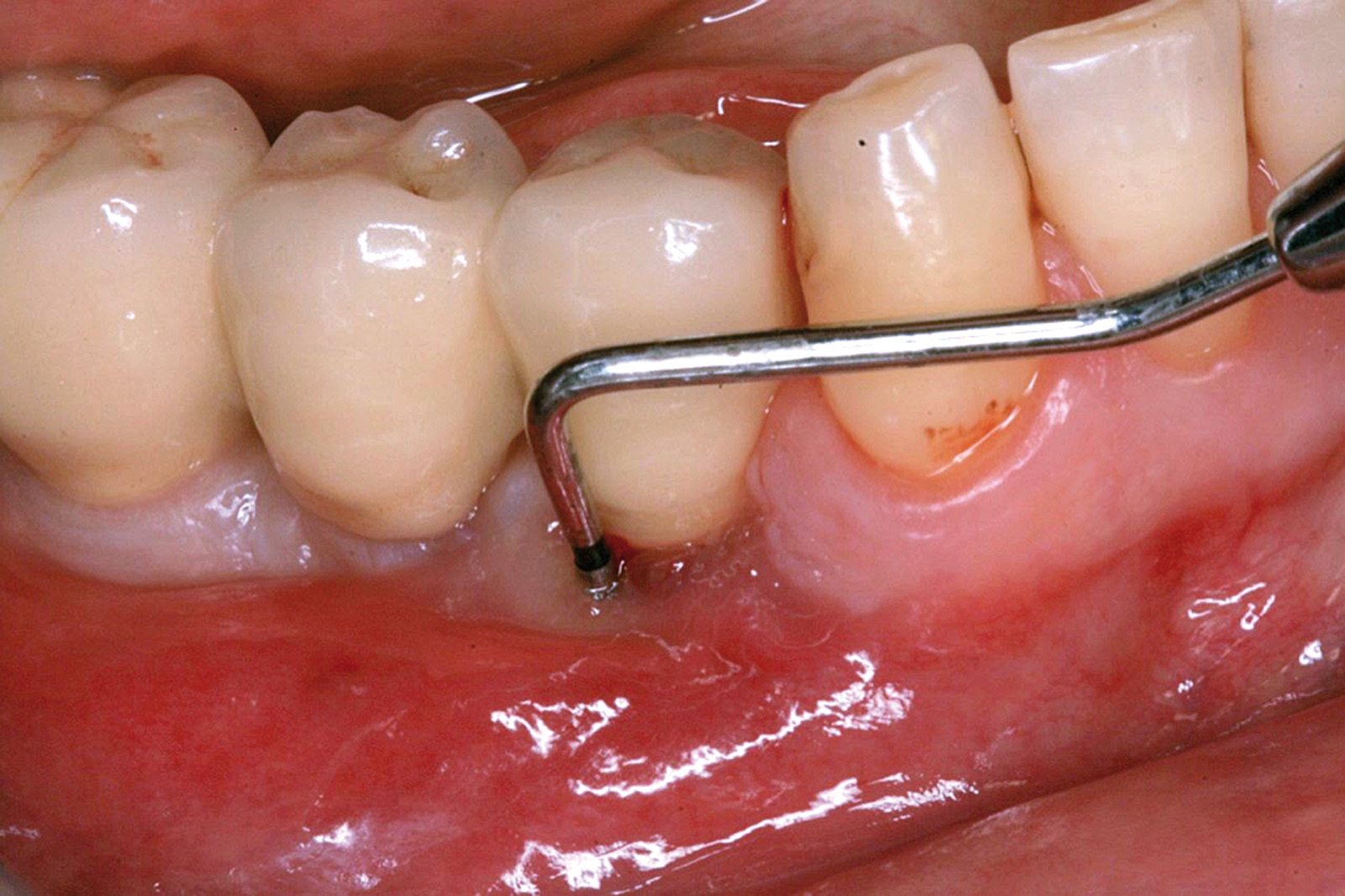
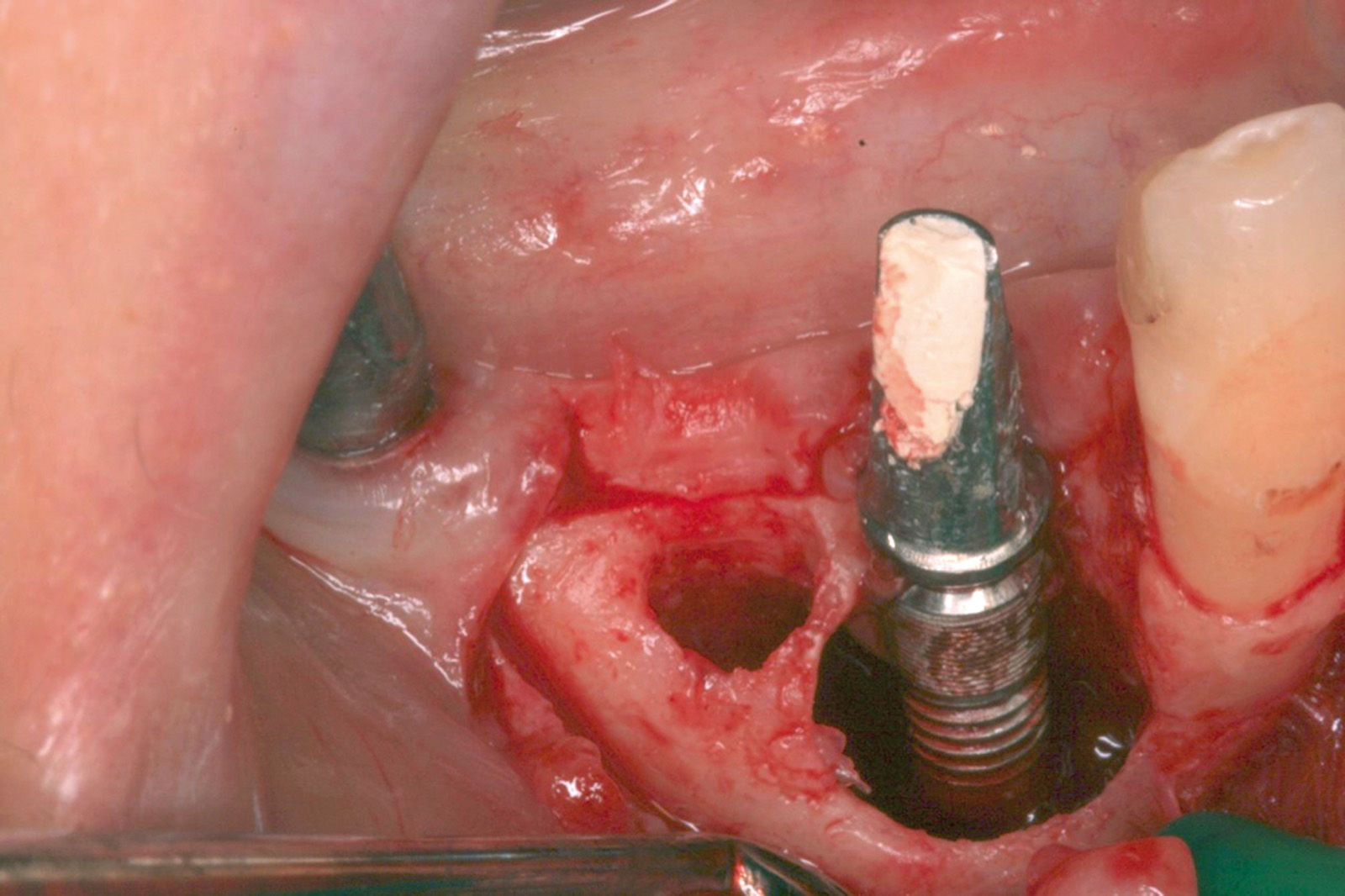
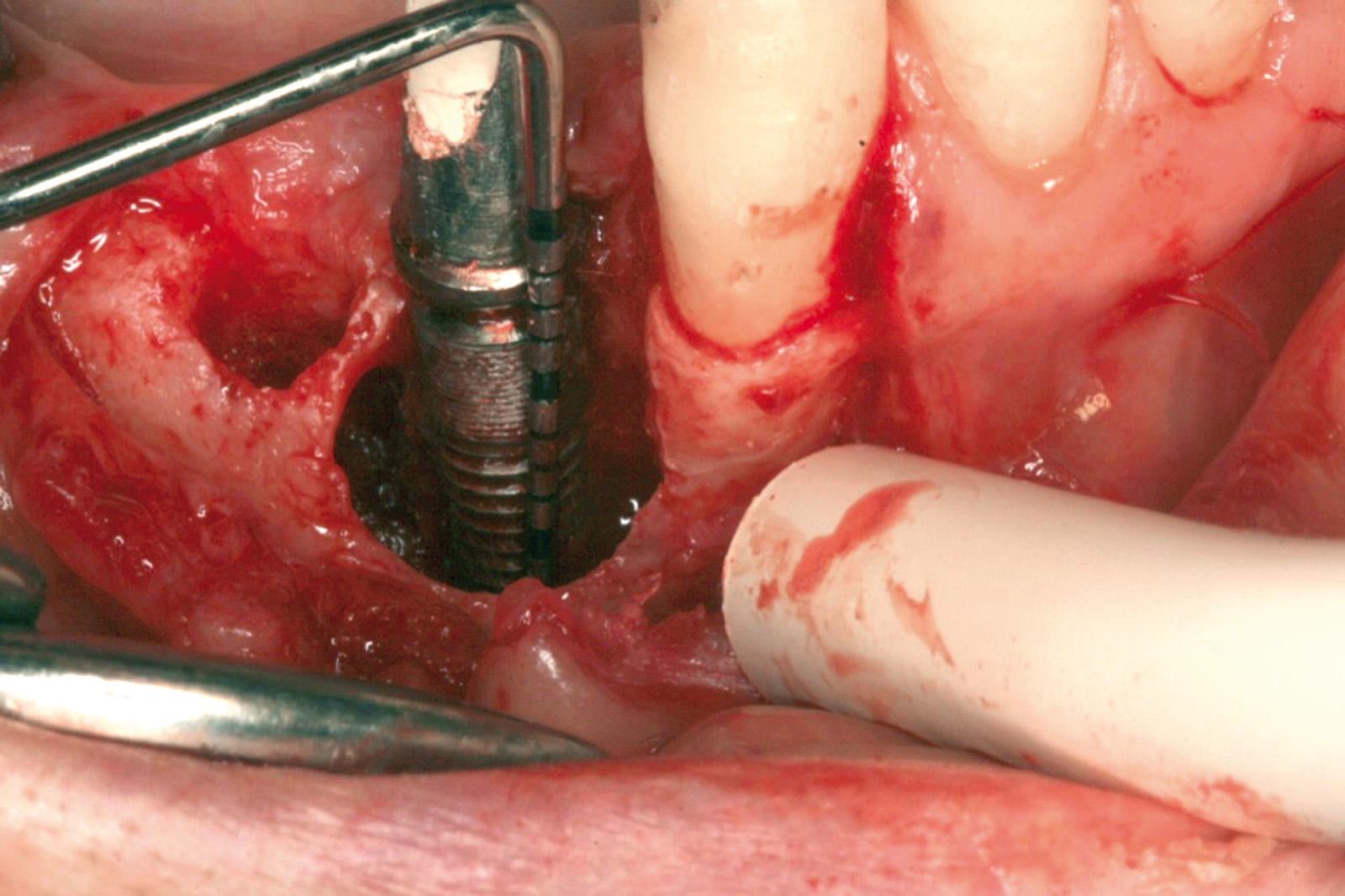
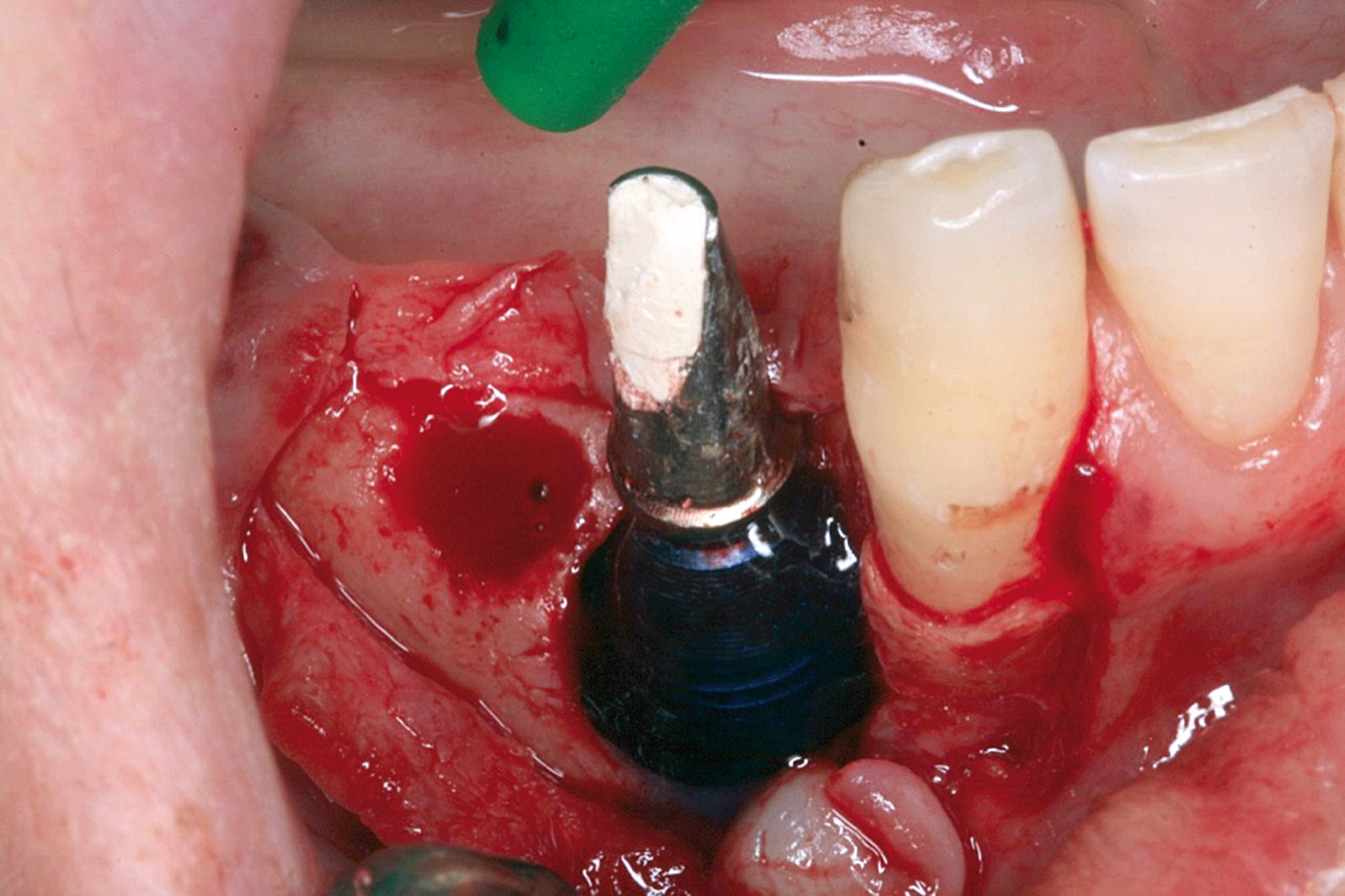
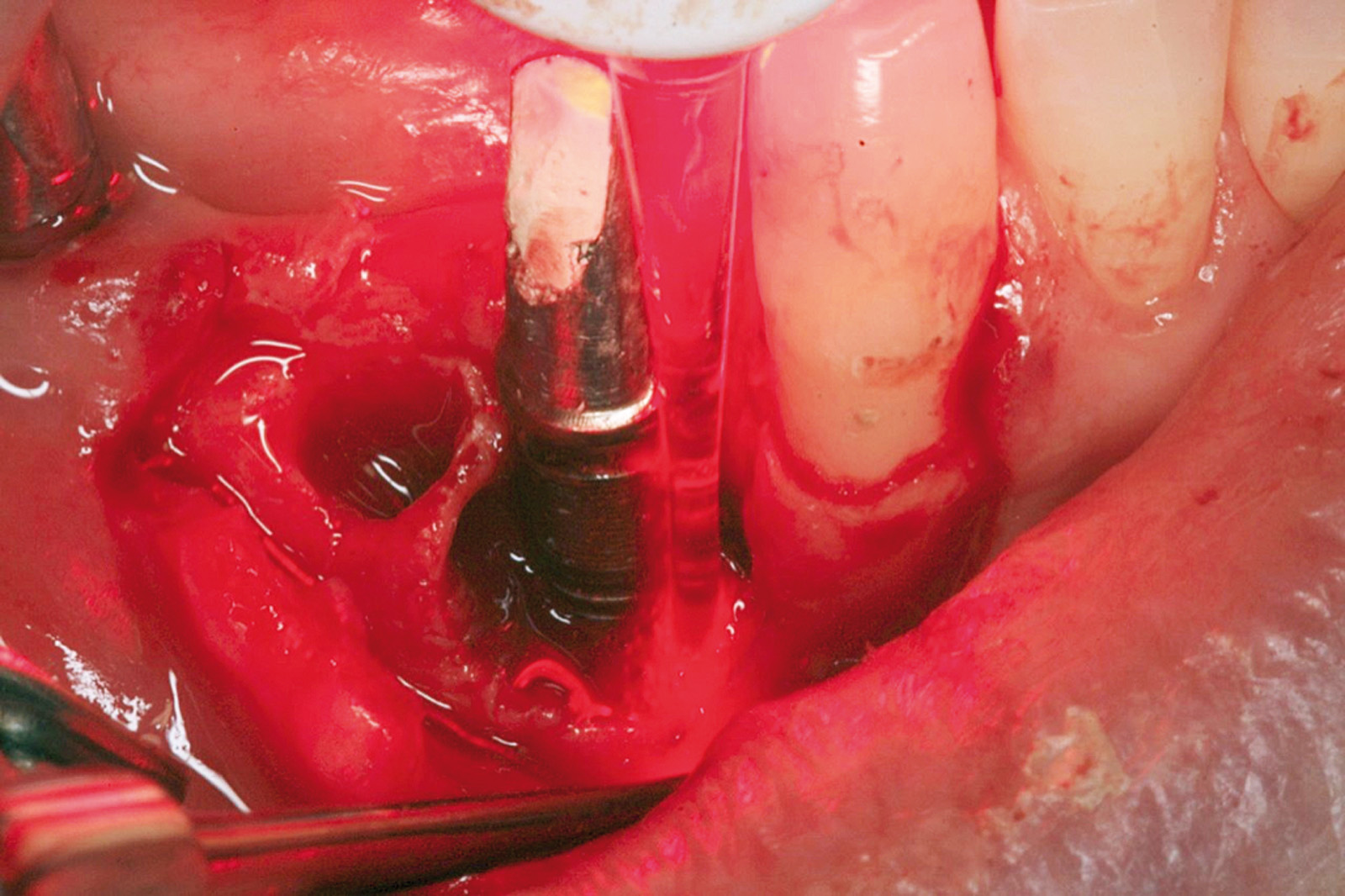
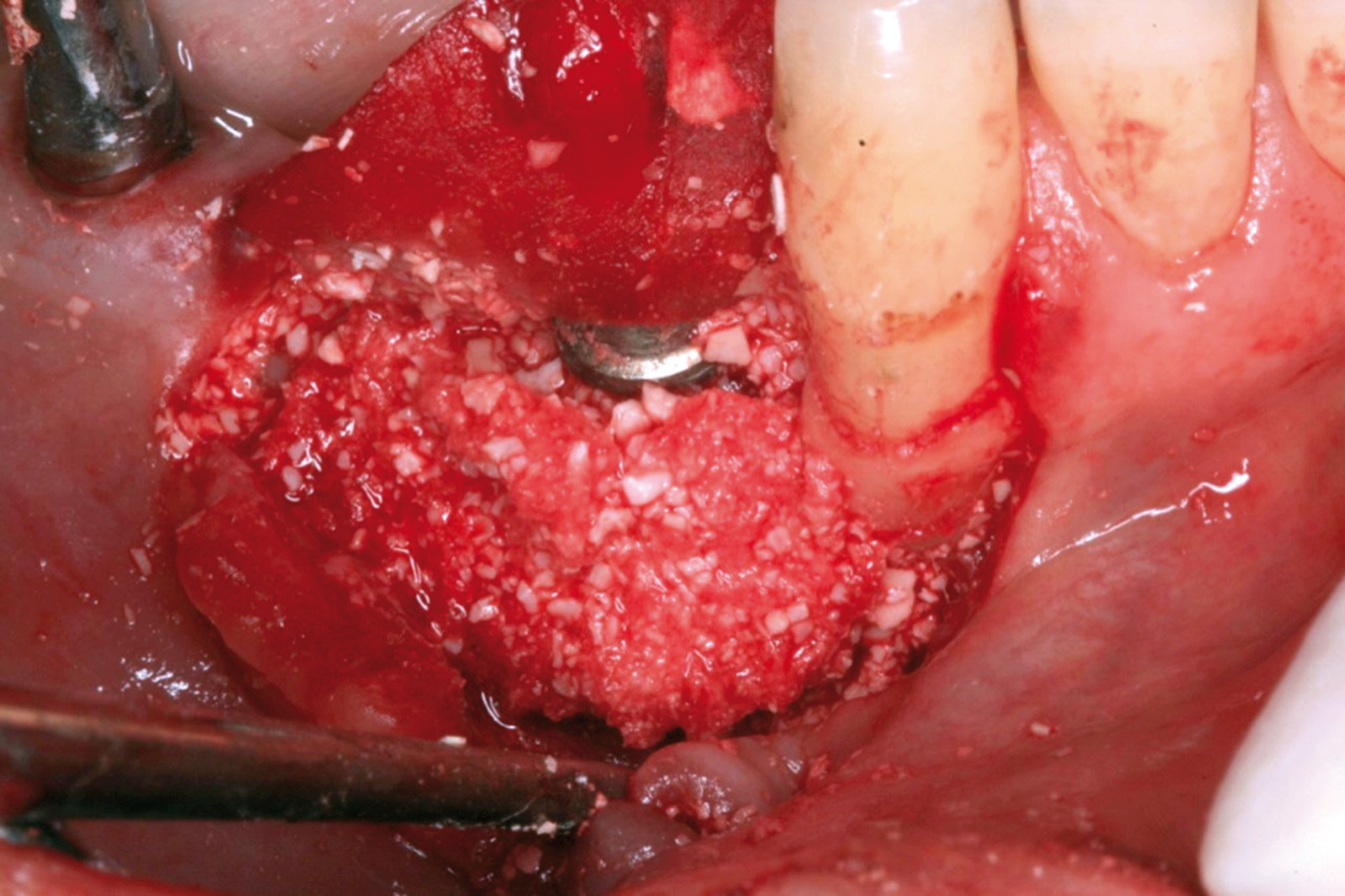
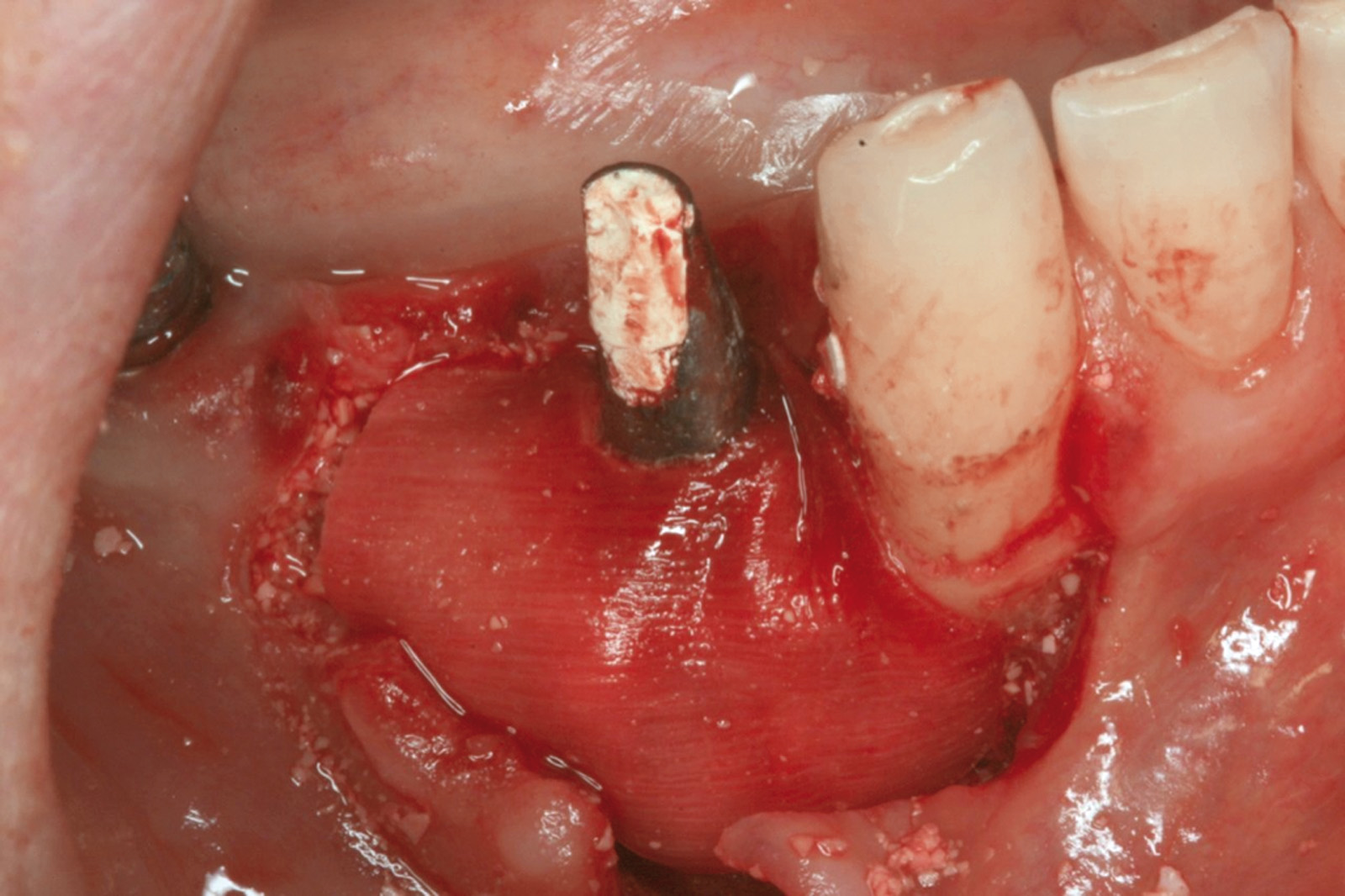
Ciò non toglie che il principio della disinfezione con terapia fotodinamica appare estremamente interessante per molte applicazioni, considerate anche le problematiche sempre più rilevanti nell’utilizzo degli antibiotici. Sono necessari quindi ulteriori studi scientifici che mettano in luce l’importanza dei vari aspetti in questo affascinante campo, viste anche le potenzialità di applicazioni diverse quali ad esempio la decontaminazione delle superfici degli impianti affetti da peri-implantite per la quale, a oggi, non abbiamo ancora un trattamento predicibile. Nel caso clinico descritto dalle Figure 13-15 diamo un esempio di applicazione della LAD nei casi di mucosite peri-implantare, mentre nel caso clinico successivo (Figure 16-18) l’applicazione intra-operatoria della stessa LAD per la decontaminazione della superficie di un impianto affetto da grave peri-implantite prima della terapia rigenerativa.
Corrispondenza
Claudio Mongardini
Sapienza, Università di Roma - Facoltà di Medicina e Odontoiatria
Via Caserta, 6 - 00161 Roma
claudio.mongardini@uniroma1.it



[…] https://www.ildentistamoderno.com/la-terapia-fotodinamica-in-parodontologia […]
[…] https://www.ildentistamoderno.com/la-terapia-fotodinamica-in-parodontologia […]