Smoke and oro-facial health: interactions with the Sleep Dentistry
Sono ben noti gli effetti nefasti del fumo sulla salute, generale e orale, mentre la loro ricaduta sul sonno rappresenta un ambito di studio più recente: bruxismo, russamento e apnee del sonno, in età adulta come in età infantile, vedono nel fumo, sia attivo che passivo, un forte fattore di rischio.
Riassunto
Bruxismo, russamento e apnee ostruttive del sonno (OSA) sono le patologie del sonno in cui più frequentemente l’odontoiatra riveste un ruolo in termini di intercettazione, diagnosi, terapia e, laddove possibile, di prevenzione, costituendo così la Sleep Dentistry. Questo lavoro intende approfondire come l’abitudine al fumo di sigaretta o l’esposizione al fumo passivo possano avere ripercussioni in tale ambito, sia sulla popolazione adulta che su quella infantile.
Bruxismo, russamento e apnee del sonno si presentano infatti con percentuali rilevanti in pazienti fumatori, ex fumatori o esposti al fumo passivo.
L’eziopatogenesi, nel caso di russamento e OSA, si può ricercare sia nell’azione diretta pro-flogogena a livello della mucosa delle alte vie respiratorie, sia attraverso un meccanismo indiretto legato al rapporto esistente tra nicotina, sistema dopaminergico, tono muscolare e soglia di microarousal. Quest’ultimo sembra anche essere il meccanismo legato al bruxismo.
L’esposizione al fumo passivo, inoltre, rende più probabile lo sviluppo di bruxismo e disturbi respiratori del sonno in età infantile.
Il fumo rappresenta un nemico a 360° dell’odontoiatria, non solo in termini di malattia parodontale e perimplantare, di patologie delle mucose, di complicanze post-chirurgiche, di pigmentazioni dentali e di alitosi, ma anche in termini di grave impoverimento della qualità del sonno, con nefaste ricadute sulla salute generale dell’individuo. Pertanto la lotta al fumo di sigaretta deve diventare una mission per l’intero staff dello studio odontoiatrico.
Summary
Bruxism, snoring and obstructive sleep apnea are the sleep disorders most commonly intercepted and treated in Dentistry. This paper means to look through the relationship between sleep disorders and smoking habits or second hand smoking, during pregnancy, childhood and adulthood. Smoking irritates and narrows the airways, facilitating the obstruction and leading to snoring and apnea. Moreover nicotine abstinence disrupts the sleep architecture and interacts with the dopaminergic system and the muscular tone during sleep. Smokers chronic hypoxia also seems to modulate the peripheral chemoceptors, modifying the arousal threshold.
Arousals and dopaminergic system are seemed to be involved also in bruxism genesis. Smoking during pregnancy reduces fetal oxygen level, compromises fetal growth and facilitates facial cleft and is the second cause, after sleeping position, for Sudden Infant Death Syndrome.
Second hand smoke exposure during childhood disrupts sleep quality and promotes dental decay and bruxism. Moreover, causing recurrent respiratory infections, may lead to respiratory sleep disorders and to oral breathing, inducing very severe alteration in child growth, both facial, physical and neuro-socio-psychological.
Patient’s general and oral health is highly threatened by smoking at all ages: smoking cessation must be promoted in the dental practice and should become its mission. This action must be strengthened if there are children involved.
Laureata a pieni voti nel 2007 presso l’Università degli Studi di Milano, libera professionista presso i reparti di Gnatologia e Gnatologia Neuromuscolare dell’Istituto Stomatologico Italiano, dove si occupa anche di Sleep Dentistry. Consulente presso diversi studi dentistici in Milano. Ha realizzato la mostra fotografica «Fumare ti scolora». Consigliera dell’Ordine dei Medici e degli Odontoiatri di Milano per il triennio 2015-17.

Come già discusso ampliamente in questa stessa sede1, il fumo di tabacco rappresenta ancora oggi uno dei più gravi problemi di salute pubblica al mondo non solo per le patologie direttamente legate a esso, quali i tumori e le infezioni delle vie respiratorie e le bronco-pneumopatie croniche (BPCO), ma anche per le ricadute sulle cardiomiopatie ischemiche, sulle cerebropatie vascolari e sui dismetabolismi2.
Il fumo inoltre concorre all’insorgenza e al mantenimento di disturbi come la Sindrome delle Apnee Ostruttive del Sonno (OSAS), che a sua volta determina l’aumento di morti per le precedenti patologie e il crescere del rischio di incidenti stradali da 1,2 a 4,9 volte3.
Per questo motivo, nonostante le OSAS siano una patologia fortemente sottodiagnosticata4, di recente si è visto un aumento del grado di attenzione del decisore politico con un giro di vite sulle norme per il rilascio e il rinnovo della patente di guida automobilistica in pazienti affetti da OSAS o sospetti tali5. Ci si augura che tale attenzione possa diventare un importante cassa mediatica per il fondamentale ruolo che può avere l’odontoiatra in termini di diagnosi precoce e strategie terapeutiche nel trattamento delle Apnee Ostruttive del Sonno (OSA).


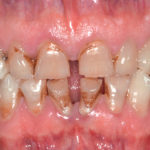
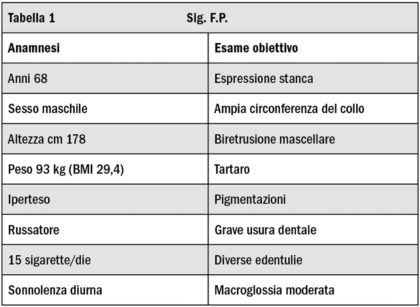
Queste ultime si presentano sempre accompagnate dal russamento e spesso dal bruxismo, manifestazioni cliniche che possono presentarsi anche indipendentemente dalla presenza di OSA.
Bruxismo, russamento e OSA si presentano in percentuali particolarmente rilevanti in pazienti fumatori o ex fumatori6, pertanto diversi studi hanno cercato di approfondire il ruolo del fumo nell’eziopatogenesi di tali disturbi.
I sopracitati disturbi del sonno possono presentarsi anche nell’età dello sviluppo, periodo durante il quale un’adeguata qualità del sonno è fondamentale per il corretto sviluppo psico-fisico dell’individuo. I bambini esposti a fumo passivo, o «second hand smoke» (SHS), presentano infatti un’aumentata incidenza di disturbi respiratori del sonno7: la maggiore suscettibilità ad asma e infiammazioni ricorrenti del tratto respiratorio possono predisporre allo sviluppo della respirazione orale, fattore che a sua volta predispone a diverse alterazioni dello sviluppo cranio-facciale, legame noto fin dagli anni ‘808,9.
Il fumo agisce sia in maniera diretta, con un’azione infiammatoria sulle mucose delle vie aeree superiori10, sia per via indiretta, per il legame esistente tra nicotina, sistema dopaminergico, tono muscolare e soglia di arousal, come meglio vedremo in seguito.
Per un’odontoiatra attento è piuttosto semplice intercettare, anche precocemente, bruxismo e abitudine al fumo, il primo per via delle faccette di usura e l’ipertono/ipertrofia masseterina, il secondo per l’alitosi e le caratteristiche pigmentazioni dentali. La gestione dei pazienti affetti da disturbi del sonno invece richiede non solo la conoscenza in termini sia epidemiologici che clinici di tali entità, ma soprattutto un’osservazione della salute del paziente ad ampio campo, che consenta di sviluppare una specifica chiave di lettura sia dell’anamnesi che dell’esame clinico, del paziente pediatrico come del paziente adulto.
Se siamo di fronte a un paziente di sesso maschile, di mezza età, in sovrappeso, fumatore e iperteso non possiamo non approfondire la qualità del suo sonno: fumo e OSAS rappresentano due tra i più importanti fattori di rischio cardiovascolare, con effetti moltiplicativi quando entrambi presenti11.
Parimenti, se ci troviamo di fronte a un bimbo respiratore orale, tanto più se presenta turbe del comportamento, sarà fondamentale approfondirne la qualità del sonno e l’eventuale abitudine al fumo dei genitori12.
Il fumo è un nemico a 360° della salute orale ed è un importantissimo fattore di rischio di parodontopatia, fallimento implantare e complicanze postchirurgiche, oltre che di lesioni degenerative delle mucose1. Pertanto nessun odontoiatra può prescindere dall’educare i pazienti (e i loro genitori) a uno stile di vita sano e attivo, e dal fare della lotta al fumo di sigaretta uno dei propri leitmotiv, tanto più se si occupa di Sleep Dentistry, Odontoiatria Pediatrica e Ortognatodonzia.
Il sonno e le sue funzioni
La medicina del sonno è una disciplina piuttosto recente: si pensi che fino agli anni ‘50, quando si scoprirono i rapid eye movement, il sonno era considerato una condizione passiva di riposo, senza particolari attività o funzioni.
Il quadro delle OSA, in particolar modo, è stato per decenni una patologia «orfana»: da una parte neurologi e psichiatri, che studiavano il sonno, non consideravano la respirazione, dall’altra pneumologi e otorini, che studiavano la respirazione, non consideravano il sonno.
Inoltre generazioni di odontoiatri hanno studiato e trattato il cavo orale di milioni di pazienti che soffrivano di disturbi respiratori del sonno senza nemmeno conoscerne l’esistenza13.
Per comprendere l’importanza di una buona qualità del sonno è fondamentale conoscerne il ruolo cruciale nel mantenimento dello stato di salute di un individuo.
Durante il sonno avvengono:
- il recupero energetico e il riposo dell’organismo;
- il ripristino biochimico (tra cui la sintesi proteica, la neurogenesi, il metabolismo del glicogeno e la secrezione di GH);
- la regolazione della funzione immunitaria;
- la codificazione delle informazioni acquisite durante la giornata e la consolidazione della memoria.
La deprivazione del sonno può portare ad alterazioni dell’umore, aggressività, depressione e comparsa di dolore14.
Durante il sonno avvengono periodicamente e fisiologicamente, da 6 a 14 volte in un’ora, delle attivazioni EEG accompagnate da altri fenomeni simpatici quali l’aumento dell’attività cerebrale, cardiaca e del tono muscolare, chiamati microarousal (MA).
Il significato funzionale dei MA sembra essere quello di una sorta di sentinella che mantiene il contatto con il mondo esterno, selezionando le informazioni in entrata e permettendo il risveglio in caso di pericolo: senza gli arousal il sonno sarebbe identico al coma15.
La sleep dentistry
Bruxismo
La Sleep Dentistry, o Odontoiatria del Sonno, è la disciplina che si occupa dell’intercettazione e del trattamento dei disturbi del sonno di pertinenza odontoiatrica.
Tra questi il più noto agli odontoiatri è il bruxismo; un tempo classificato come «parasonnia», è in realtà un disturbo del movimento caratterizzato da ripetitivi movimenti mandibolari che avvengono prevalentemente nella fase II del sonno non REM, durano circa 10-20 secondi e sono associati a microarousal. Il bruxismo colpisce sia in età infantile che in età adulta; ne soffre circa l’8-10% degli adulti, con picchi fino al 20%, frequenza che diminuisce con l’aumentare dell’età16,17.
La diagnosi certa di bruxismo avviene attraverso una polisonnografia (PSG) con elettromiografia ma una diagnosi di presunzione può essere effettuata attraverso la storia del paziente (che lamenterà dolenzia o senso di tensione al viso al risveglio), il racconto del partner di letto o dei genitori (che riferirà il caratteristico stridio o un violento sbattere dei denti) e l’esame clinico obiettivo (che rivelerà faccette d’usura sulle superfici dentali incisali o occlusali e l’ipertono e/o l’ipertrofia dei masseteri).
Le cause del bruxismo non sono ancora completamente chiare ma il ruolo principale sembra che lo giochino stress, ansia, problematiche occlusali, consumo di caffeina, fumo, sostanze psicotrope, farmaci antidepressivi e antipsicotici che determinano alterazioni del sistema dopaminergico e la posizione assunta durante il sonno16.
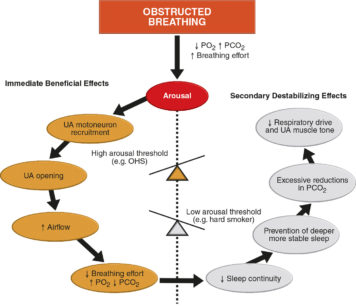
La gestione del bruxismo, soprattutto nei casi più severi, è fondamentale per qualunque odontoiatra in quanto il rischio di incorrere in fratture dentali o protesiche18 o in fallimenti implanto-protesici19 è estremamente alto e il paziente lamenta sia dolenzia al viso che l’antiestetica consunzione dei margini incisali.
Per quanto riguarda la gestione terapeutica del paziente bruxista, è fondamentale escludere la concomitante (e frequente) presenza di disturbi respiratori del sonno, in quanto molti pazienti bruxisti soffrono anche di russamento e OSAS.
Il ripetersi delle desaturazioni di ossigeno proprie del russamento porta ai micro-arousal, che sembrano essere i responsabili anche dell’attivazione dei muscoli masticatori propria del bruxismo20: l’origine periferica delle OSA potrebbe così almeno parzialmente spiegare l’origine centrale del bruxismo.
In caso di quadro clinico dubbio è fondamentale fare una PSG dirimente; una diagnosi sicura è necessaria in quanto due delle opzioni terapeutiche indicate nel bruxismo semplice sono invece controindicate nei disturbi respiratori perché possono peggiorare il quadro respiratorio:
- l’effetto miorilassante delle benzodiazepine, prezioso in caso di dolore muscolare, aumenta la collassabilità delle vie aeree;
- un semplice bite plane di protezione può permettere una maggiore retrusione mandibolare in posizione supina.
In primo luogo, comunque, l’odontoiatra dovrà sensibilizzare il paziente a seguire uno stile di vita sano e attivo e minimizzare quanto possibile i fattori di rischio.
Russamento e UARS
Il russamento, o roncopatia, è la vibrazione del palato molle associata al restringimento delle vie aeree durante la respirazione: la turbolenza del passaggio dell’aria produce il caratteristico rumore, talvolta tanto intenso da compromettere la qualità del sonno del partner.
Il russamento è molto diffuso nella popolazione, anche infantile (10%), e colpisce maggiormente gli uomini (35-45% oltre i 40 anni di età) che le donne (15-28%)21.
Il russamento è più frequente:
- in pazienti sovrappeso o obesi;
- in età avanzata;
- in pazienti fumatori;
- in pazienti con micrognazia;
- in pazienti respiratori orali;
- dormendo supini;
- dopo pasti abbondanti;
- dopo l’assunzione di alcolici;
- dopo l’assunzione di ansiolitici;
- durante la gravidanza.
Nei casi più lievi il russamento non è accompagnato da alterazioni dei parametri polisonnografici. Quando le vibrazioni dei tessuti molli rendono più difficoltosa la respirazione si parla di “Sindrome delle Aumentate Resistenze Respiratorie”, più nota con la sigla UARS (Upper Airways Resistance Syndrome). Questo quadro non è associato né a ipopnee/apnee, né a desaturazioni patologiche di ossigeno, ma comporta un aumento dei MA, rendendo il sonno frammentato e portando a una conseguente spossatezza al risveglio e sonnolenza diurna22.
OSAS
Le OSA sono l’evoluzione patologica del russamento e sono caratterizzate da ricorrenti ipopnee, (diminuzioni di almeno il 50% del flusso respiratorio) e/o apnee (interruzione completa del flusso) della durata dai 15 ai 60 secondi circa23.
Soffrono di OSAS il 2% delle donne e il 4% degli uomini tra i 30 e i 60 anni, e la percentuale aumenta fino all’11% se si considerano popolazioni sopra i 60 anni24.
Tra i principali parametri polisonnografici per valutare l’entità del fenomeno abbiamo:
- AHI (Apnea Hypopnea Index), l’indice più utilizzato, dato dalla somma delle apnee e ipopnee per ogni ora di sonno esaminata;
- ODI (Oxygen Desaturation Index), esprime il numero di episodi per ora in cui la saturazione di ossigeno del sangue scende di almeno il 4% della saturazione basale di quel soggetto;
- tempo di desaturazione, il periodo che il paziente passa con una saturazione al di sotto del normale, la cui soglia viene considerata solitamente il 95%;
- AI (Arousal Index), esprime il numero di arousal per ora, misurabile attraverso lo studio EEG.
La gravità delle OSA nei pazienti adulti viene definita in base allo AHI25:
- AHI 0-5 = respirazione nei limiti fisiologici;
- AHI 5-15 = OSAS lieve;
- AHI 15-30 = OSAS moderata;
- AHI >30 = OSAS grave.
Durante questi periodi di diminuzione del flusso aereo, l’abbassamento dell’ossiemoglobinemia e l’aumento della carbossiemoglobinemia oltre la soglia di sensibilità individuale determina l’attivazione dei chemocettori che innescano il microarousal: il sistema nervoso simpatico si attiva, la frequenza cardiaca e la pressione arteriosa aumentano e il sonno passa da uno stadio più profondo a uno più leggero, ripristinando un maggiore tono muscolare: in questo modo le pareti delle vie aeree superiori tornano a essere più tese e quindi più pervie e permettono il ritorno del flusso respiratorio26.
Il ripetersi continuo di passaggi tra diversi stadi del sonno porta alla frammentazione dello stesso, non solo rendendolo poco riposante ma trasformandolo in un vero e proprio stress cronico per l’organismo, con gravi conseguenze per l’individuo:
- ipertensione arteriosa;
- sonnolenza diurna;
- spossatezza;
- dismetabolismi;
- problematiche cardio-circolatorie;
- alterazioni dell’umore;
- incidenti stradali.
Uno degli effetti sistemici più nefasti delle apnee ostruttive è determinato dall’ipossia cronica intermittente che si verifica ogni notte. Le continue fluttuazioni della concentrazione di ossigeno evocano una risposta pro-infiammatoria mediata dal fattore nucleare NF-kB, con produzione di ROS e rilascio di TNF-alfa e IL-8, provocando la disfunzione endoteliale, coinvolta nella patogenesi dell’aterosclerosi27.
Lo stato infiammatorio cronico dovuto all’ipossia intermittente è inoltre in grado di alterare i processi metabolici, riducendo la sensibilità all’insulina, condizione particolarmente grave soprattutto nei pazienti in età evolutiva28. La comorbilità tra OSAS e sindrome metabolica è oggi sotto i riflettori della ricerca scientifica visto il suo enorme impatto sullo stato di salute dei cittadini e la relativa ricaduta sia in termini socio-economici che di coordinamento delle terapie mediche29.
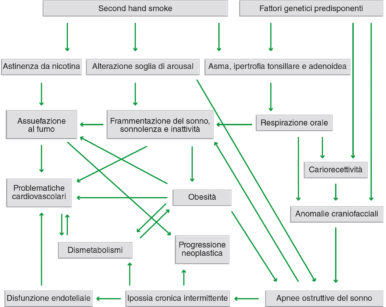
Recenti studi stanno infine evidenziando un ulteriore effetto nefasto delle OSAS: lo stato infiammatorio cronico induce atipie cellulari, favorendo la progressione neoplastica e l’ipossia cronica intermittente pare favorire, ancor più dell’ipossia cronica, l’angiogenesi tumorale, creando condizioni metaboliche che favoriscono la crescita tumorale30.
Forse l’anello di congiunzione tra i problemi cardiovascolari e lo sviluppo delle neoplasie si può ricercare nel metabolismo del triptofano, precursore della serotonina e della nicotinamide (che non ha nulla a che vedere con la nicotina) ma anche di diversi mediatori come la chinurenina e gli acidi antranilico, kinurenico e chinolinico31.
Queste scoperte potrebbero portare a interessanti sviluppi terapeutici nella cura delle patologie cardiovascolari, della sindrome metabolica e delle neoplasie solide, che devono prevedere un’attenta gestione di fattori di rischio quali la presenza di OSAS e l’abitudine al fumo di sigaretta.
Fumo e qualità del sonno: un’accoppiata perdente
Come già accennato è stato approfonditamente discusso in questa stessa sede come l’assuefazione al fumo di sigaretta rappresenti una delle cause principali del fallimento delle terapie odontoiatriche per via di un aumento di incidenza della malattia parodontale e perimplantare, di complicanze post-chirurgiche, di degenerazione delle mucose del cavo orale, di pigmentazione dentale e dei restauri dentali e dell’alitosi1.
Cerchiamo ora di analizzare i principali meccanismi attraverso i quali la dipendenza dal fumo di sigaretta interferisce con la qualità del sonno e aumenta, in misura variabile, il rischio per bruxismo, russamento e apnee del sonno.
Astinenza da nicotina e impoverimento della qualità del sonno
Che fumare peggiori la qualità della vita in termini di salute è ormai noto da decenni; più recente invece è l’attenzione alle ripercussioni dell’abitudine al fumo sulla qualità del sonno.
I primi importanti studi epidemiologici risalgono a circa 20 anni fa. In particolar modo due, svolti attraverso dei questionari, somministrati rispettivamente a circa 350032 e quasi 500 individui33, volti a indagare lo stato di salute generale e la qualità del sonno, mostrano come i fumatori presentino più frequentemente rispetto ai non fumatori difficoltà ad addormentarsi, sonnolenza diurna (soprattutto tra le pazienti di sesso femminile) e incubi notturni (prevalentemente tra quelli di sesso maschile).
Risultati simili sono stati trovati anche nel National Health and Nutrition Examination Survey, condotto nel 2005-2006 negli Stati Uniti, che ha coinvolto circa 5000 individui sopra i 6 anni, e nello Sleep Heart Health Study, studio multicentrico americano che ha coinvolto quasi 6500 individui sopra i 40 anni, iniziato nel 1994 e i cui risultati sono stati tracciati fino nel 2010.
In entrambi gli studi i fumatori presentavano complessivamente, rispetto ai non fumatori:
- durata minore del sonno;
- maggiore difficoltà ad addormentarsi;
- risvegli più frequenti e precoci.
Gli ex fumatori presentano, seppur in maniera meno significativa, le stesse alterazioni rispetto ai non fumatori34.
Una successiva analisi di alcuni valori del National Health and Nutrition Examination Survey ha confermato come uno dei principali fattori predittivi dell’impoverimento del sonno, in termini di durata dello stesso e sonnolenza diurna, sia il tempo trascorso dal risveglio all’accensione della prima sigaretta della giornata, dato che, più della quantità di sigarette fumate durante la giornata, esprime la dipendenza da nicotina35.
Che l’astinenza da nicotina possa essere uno dei fattori chiave nel comprendere come il fumo impoverisca il sonno era stato già ipotizzato confrontando l’analisi spettrale EEG durante la PSG di 44 pazienti fumatori, abbinati per sesso ed età ad altrettanti controlli. Le modifiche più consistenti nell’architettura del sonno avvengono nella prima metà della notte e diminuiscono nella seconda; questo risultato fa pensare che l’astinenza da nicotina, la cui emivita è da 2 a 4 ore, possa giocare un ruolo chiave nelle alterazioni del sonno nei pazienti fumatori36.
Fumo di sigaretta e alterazioni della soglia
dei chemocettori deputati a innescare gli arousal
L’ipotesi che il fumo provochi un’alterazione della soglia dell’arousal deriva in gran parte dall’esperienza in ambito pediatrico37.
La più drammatica conseguenza del SHS sui neonati è la Sudden Infant Death Syndrome (SIDS), la cosiddetta “morte bianca”. Poiché la posizione è stata la prima causa riconosciuta di SIDS, nel 1987 sono uscite in Olanda delle raccomandazioni ai genitori sulla posizione da far assumere ai neonati durante il riposo in culla che hanno avuto molto seguito, portando a una drastica riduzione delle SIDS38.
Uno studio, sempre olandese, ha raccolto dati su 142 SIDS occorse successivamente al 1987 e ha eseguito uno studio multivariato per determinare i fattori di rischio tra cui la posizione assunta durante il sonno, il fumo materno durante la gravidanza, il fumo parentale in età neonatale, la nascita prematura, il sesso, il tipo di allattamento e le condizioni socio-economiche familiari.
Il fumo passivo postnatale sembra essere un importante fattore di rischio ambientale per SIDS (OR un genitore = 2.5 [CI=1.2-5.0]; entrambi i genitori = 5.77 [CI=2.2-15.5]; materno = 2.7 [CI=1.0-6.4]; paterno = 2.4 [CI=1.3-4.5])39.
Anche l’analisi delle PSG di 30 neonati prematuri, 16 esposti al SHS e 14 controlli, sovrapponibili sia per età gestazionale che concezionale, ha mostrato come il fumo materno sia associato a un incremento significativo degli indici di apnea (AHI 28.6 +/-6.4/hour VS. 13.2 +/-3.9/hour; p<0.05), tenuto conto dei soli eventi di natura ostruttiva. L’indice di arousal, di contro, era notevolmente diminuito nel gruppo con madri fumatrici (34.5 +/- 2.3/hour VS. 46.3 +/- 5.6/hour; p<0.05), ed era soprattutto inibito dopo eventi respiratori (10.7 +/- 2.1% hour VS. 29.4 +/- 5.4% hour; p<0.05). Questi risultati mostrano quindi come i neonati esposti al SHS siano più soggetti a eventi respiratori di natura ostruttiva: l’alterazione della soglia di arousal ne determina l’inibizione, ritardando quindi l’attivazione della muscolatura delle alte vie respiratorie, esponendo il neonato a desaturazioni pericolose, così come succede nelle SIDS40.
La nicotina contenuta nel fumo di sigaretta disturba inoltre lo sviluppo fetale, alterando il sistema di trasmissione colinergico e serotoninergico, e legandosi ai recettori nicotinici cerebrali e del tronco encefalico, probabilmente alterandone lo sviluppo41,42.
È quindi possibile che tale legame tra la nicotina e i recettori encefalici e del tronco encefalico porti a un’alterazione nella modulazione centrale che determinerà desaturazioni più marcate nel futuro fumatore apneico. Questo legame cronico favorisce inoltre la maggiore espressione di tali recettori nell’SNC, esponendo il futuro giovane adulto a un maggiore rischio di dipendenza43.
Altra ipotesi accreditata è dovuta all’ipossia cronica in cui vivono i pazienti fumatori a causa del fortissimo legame tra il monossido di carbonio e l’emoglobina, che spiazza l’ossigeno, rendendolo meno disponibile a tutti i tessuti.
L’ipossia cronica potrebbe quindi determinare un adattamento delle soglie dei chemocettori periferici, con una conseguente diminuzione della soglia di arousal. I pazienti fumatori quindi trascorrerebbero un tempo maggiore in apnea prima che la saturazione di ossigeno scenda e quella di anidride carbonica salga a sufficienza da provocare l’arousal e ripristinare la pervietà delle vie aeree che consente il ritorno alla respirazione44.
Una conferma di tale ipotesi periferica potrebbe essere offerta da uno studio brasiliano, in cui sono stati osservati 1492 pazienti afferiti a un centro del sonno, divisi tra non fumatori, ex fumatori e fumatori, a loro volta suddivisi in due categorie, <15 pacchetti/anno e >/= 15 pacchetti/anno, definendo così la severità dell’abitudine al fumo. I risultati più significativi sono relativi al tempo di sonno passato con una saturazione di O2 inferiore al 90%:
- non fumatori: 6% +/- 13%;
- ex fumatori: 9% +/- 18%;
- fumatori di più di 15 pacchetti/anno: 16% +/- 21%;
- fumatori di meno di 15 pacchetti/anno: 22% +/- 24%.
Le differenze in termini di AHI non sono significative, mentre i pazienti fumatori presentano desaturazioni più lunghe e severe45.
Purtroppo, digitando su Pubmed le parole chiave «smoke and arousal threshold», si trovano infatti solo 15 risultati, svolti prevalentemente su neonati e animali da laboratorio: molto lavoro è pertanto ancora da fare per meglio comprendere come il fumo alteri la soglia degli arousal nei pazienti adulti.
Il fumo infiamma le vie respiratorie
La nicotina è solo una delle 4000 sostanze tossiche contenute nelle sigarette, 40 delle quali ritenute cancerogene.
Queste sostanze tossiche, derivate dalla combustione incompleta di tabacco e carta e volatilizzate per l’elevata temperatura, possono danneggiare direttamente o indirettamente le vie aeree e l’intero organismo. Tra queste vi sono numerosi irritanti, quali:
- aldeidi (acroleina, acetaldeide e formaldeide);
- acidi organici carbossilici (acido formico);
- fenoli e cresoli;
- ammine e ammoniaca;
- idrocarburi non aromatici di varie tipologie (principalmente alcani C12-C15) che contribuiscono a intaccare lo strato lipidico protettivo di organi e cellule, predisponendo all’aggressione di altri composti.
Le stesse apnee ostruttive, per via delle turbolenze del flusso aereo, tendono a infiammare le mucose dell’ugola, rendendole più ispessite e più edematose rispetto a quelle dei pazienti senza OSA.
I pazienti apneici e fumatori presentano inoltre alterazioni citologiche nella lamina propria dei tessuti dell’ugola, probabilmente legate a un aumentato livello del peptide calcitonina gene-correlato. Mucose infiammate delle vie aeree vuol dire mucose edematose, gonfie nonostante la transitoria vasocostrizione periferica dovuta all’azione della nicotina, ottenendo così un ulteriore restringimento delle vie aeree superiori46.
I pazienti fumatori tendono a presentare un russamento severo più in giovane età rispetto ai coetanei non fumatori, indipendentemente dal BMI, mostrando inoltre un aumento delle resistenze nasali, un minore volume delle cavità nasali dopo la decongestione e un’aumentata lunghezza del palato molle, sia in posizione eretta che supina47.
Altro aspetto di fondamentale importanza è la concomitante presenza di BPCO in pazienti forti fumatori e apneici. Il fumo di sigaretta o di sigaro, sia attivo che passivo, è ritenuto infatti la principale causa della BPCO, seguito dall’inquinamento ambientale, lo stato atopico e il deficit di α1-antitripsina. Negli USA 47 milioni di persone fumano (il 28% dei maschi e il 23% delle femmine): circa il 20% dei fumatori sviluppa la BPCO e circa il 30% dei forti fumatori oltre i 40 anni presenta una limitazione al flusso respiratorio. Il termine BPCO è stato creato per comprendere in un’unica denominazione due patologie spesso associate e mal separabili: la bronchite cronica e l’enfisema polmonare.
La prima rappresenta una condizione clinica caratterizzata da tosse produttiva cronica o ricorrente per la maggior parte del tempo per un minimo di tre mesi l’anno per almeno 2 anni consecutivi. Il secondo invece è una dilatazione abnorme degli spazi aerei distali al bronchiolo terminale, con la distruzione delle pareti alveolari e conseguente perdita irreversibile delle unità funzionali responsabili degli scambi gassosi. L’inalazione ripetuta di sostanze irritanti porta a uno stato infiammatorio cronico delle vie aeree; il tessuto polmonare viene progressivamente distrutto e gli esiti cicatriziali, insieme alla presenza diffusa di muco e all’atrofia muscolare generalizzata, determinano una significativa riduzione delle capacità respiratorie48.
Questa condizione porta invariabilmente a una compromissione sempre più severa degli scambi gassosi e allo sviluppo di dispnea che si presenterà inizialmente per sforzi moderati e poi si manifesterà progressivamente anche a riposo, fino a rendere invalido il paziente, obbligandolo all’ausilio dell’ossigenoterapia per poter svolgere anche le più comuni attività quotidiane49.
OSAS e BPCO prevalgono sulla popolazione generale con percentuali simili e il 10% dei pazienti con BPCO presenta la cosiddetta overlap syndrome, grave quadro clinico in cui le due patologie coesistono nell’individuo. Tale paziente accuserà desaturazioni notturne più gravi, che lo predisporranno all’ipertensione polmonare. L’indice di massa corporeo e l’abitudine al fumo sono determinanti nel realizzarsi di tale grave condizione clinica.
L’infiammazione cronica sistemica comune a BPCO e OSAS (tra cui l’aumentare di proteina C-reattiva, IL-6, α-TNF e IL-8), lo stress ossidativo e la disfunzione leucocitaria potrebbero essere meccanismi di interazione tra i due disturbi respiratori, creando le basi per lo sviluppo di disturbi cardiovascolari50.
Il fumo come fattore di rischio per il bruxismo
L’epidemiologia mostra come il bruxismo annoveri quale fattore di rischio tutto ciò che provoca alterazioni nel sistema dopaminergico, lo stress, il fumo, l’alcool, alcune sostanze psicotrope, alcuni farmaci neurolettici, seppure non sia ben chiaro il meccanismo di tale associazione16. La nicotina induce la trasmissione sinaptica di acetilcolina e glutammato e aumenta il rilascio di dopamina e questo, insieme a una suscettibilità genetica, sembra essere il meccanismo che lega l’abitudine al fumo con il bruxismo51. Così come i disturbi respiratori del sonno, anche gli episodi di bruxismo sono preceduti dai MA52.
Confrontando le PSG di pazienti bruxisti e non bruxisti, in termini di architettura del sonno, i primi hanno mostrato un numero significativamente più alto di arousal ed episodi di bruxismo nel sonno non REM (88%), maggiormente concentrati negli stadi I e II (p<0,0001). La frequenza cardiaca durante tali episodi di bruxismo aumenta in modo significativo rispetto ai periodi precedenti gli episodi di bruxismo (69.3+/-18.2 VS. 58.1+/-15.9; p<0.0001) e la maggioranza degli episodi è associata alla brusca attivazione dei muscoli tibiali anteriori53.
Un interessante studio finlandese su 220 coppie di giovani adulti mostra che, laddove c’è un gemello bruxatore almeno settimanalmente e uno che non ha mai bruxato, il primo è un fumatore e il secondo non lo è mai stato (p=0,0003), evidenziando un legame significativo tra bruxismo e dipendenza da nicotina54.
Uno studio canadese condotto su 2000 adulti mostra come i bruxisti fumatori siano il 12%, contro il 7% dei bruxisti non fumatori (OR=1,9); i fumatori soffrono di un bruxismo più severo rispetto ai non fumatori, mostrando come la severità del bruxismo possa avere un rapporto dose dipendente con la quantità di nicotina assorbita durante la giornata55.
Fumo e disturbi del sonno: tante domande, qualche risposta
Una recente revisione della letteratura effettuata dal gruppo di Thornton nel 201456 si intitola proprio «Where there is Smoke… there is Sleep Apnea» e prova ad analizzare le relazioni tra fumo e apnee del sonno, ponendosi alcune domande di cui segue la sintesi delle risposte.
1) Qual è l’evidenza scientifica dell’associazione tra fumo e OSA?
L’evidenza scientifica è ormai piuttosto consolidata. Già nel 1994 un importante lavoro dell’Università del Wisconsin con 811 partecipanti mostra come i fumatori abbiano un rischio 4.4 volte superiore ai non fumatori di soffrire di OSA moderate o severe e 2.3 volte il rischio di soffrire di russamento. I forti fumatori, sopra le 40 sigarette al giorno, hanno invece un rischio di 40 volte superiore ai non fumatori di sviluppare OSA moderate o severe e di 6.7 volte per OSAS lievi57.
Nel 2001 un lavoro trasversale, che coinvolgeva due gruppi di 100 pazienti, uno con AHI>10 e l’altro negativo per OSAS, mostrava che nel primo gruppo i fumatori erano il 35% mentre nel secondo il 18%. I dati sono stati aggiustati per età, sesso, indice di massa corporeo e numero di alcolici bevuti per settimana. Tenendo fissi tali fattori, i fumatori mostrano un rischio di 2,5 volte maggiore rispetto ai non fumatori insieme agli ex-fumatori (OR=2.5, CI=1.3-4.7, p=0.0049) e di 2,8 volte rispetto ai soli ex-fumatori (OR=2.8, CI=1.4-5.4, p=0.0028). Aggiustando per fattori sopra citati invece gli ex-fumatori non sembrano avere maggior rischio di soffrire di OSAS rispetto ai non fumatori (OR=1.2, CI=0.55-2.7, p=0.64). Pertanto, su tale campione, il fumo di sigaretta sembrerebbe essere un fattore di rischio indipendente per OSAS58.
2) Fumare aumenta il rischio di sviluppare le OSAS o di peggiorare un eventuale quadro già esistente?
Nonostante non ci siano ancora studi longitudinali sufficientemente strutturati che permettano di comprendere meglio l’associazione tra fumo e apnee del sonno, diversi legami sono stati proposti da vari autori. I meccanismi di azione del fumo sulla qualità del sonno e sulla pervietà delle vie respiratorie sono già stati discussi precedentemente.

3) La presenza di OSA predispone a sviluppare assuefazione al fumo di sigaretta?
Nonostante non esistano studi longitudinali su questo argomento, già nel 1994 Wetter32 e nel 1996 Schrand59 ipotizzavano non solo come il fumo potesse portare a sviluppare le OSA, ma potesse essere vero anche il processo inverso.
Chi soffre di OSA è tendenzialmente in sovrappeso e soffre di sonnolenza diurna: le sigarette aiutano a eliminare il senso di fame e sono eccitanti, oltre a dare una sensazione di piacere grazie alla stimolazione dopaminergica.
Qualunque gesto comporti un effetto di benessere, l’essere umano tende a ripeterlo, nonostante sappia che possa essere nocivo: ogni volta che un paziente OSA si sentirà stanco o affamato tenderà ad accendersi una sigaretta, aprendo la strada alla dipendenza60.
Fumare stimola il centro del piacere, dà un effimero aumento della ventilazione, rende transitoriamente più ampio il lume delle vie respiratorie, aumentando il tono muscolare e diminuendo l’edema mucoso con la vasocostrizione cronica dovuto all’effetto transitorio della nicotina. La pressione sociale, che richiede alte performance psichiche, oltre che un corpo magro, alimenta l’uso delle sigarette negli individui con OSA, tipicamente in sovrappeso e assonnati61.
Infine sembra che la somministrazione di nicotina per via subcutanea nei ratti durante il sonno REM induca la stimolazione dei neuroni serotoninergici del nucleo dorsale del rafe62. Ricordiamo che i nuclei del rafe sono fittamente connessi nella porzione più rostrale con il sistema limbico e con l’ipotalamo (tali connessioni fanno dunque supporre un coinvolgimento nella regolazione dei ritmi sonno-veglia e dell’atteggiamento emotivo), mentre nella porzione più caudale ricevono le afferenze somatosensitive dal midollo spinale e da nuclei sensitivi trigeminali (il cui ruolo quindi sembra essere la modulazione della nocicezione, esercitando un effetto inibitorio diretto, o mediato da interneuroni). Questo risultato potrebbe spiegare come i pazienti affetti da depressione maggiore e disordini dell’umore (entrambi molto comuni tra i pazienti che soffrono di OSA) abbiano benefici in termini di miglioramento dell’umore grazie al fumo: tali miglioramenti, ovviamente, favoriscono lo svilupparsi della dipendenza da sigarette.
4) Smettere di fumare migliora il quadro di OSA?
La cessazione del fumo può essere valutata in diversi modi, a seconda della sua durata e del tipo di interruzione, se con terapie nicotiniche e/o farmacologiche di supporto o meno.
Durante i primi 2 giorni dopo la cessazione, i sintomi da astinenza come l’insonnia o l’irritabilità possono mimare dei sintomi da OSA. Dopo questa fase iniziale, però, i benefici nel lungo termine includono un miglioramento della qualità del sonno, dato confermato sia dal già menzionato National Health and Nutrition Examination Survey che dal lavoro del 1994 del Winsconsin, già citato anch’esso32. Si è provato anche, su campioni esigui, di valutare la possibilità di una terapia nicotinica sostitutiva da utilizzare durante il sonno, ma senza risultati significativi63. Smettere di fumare, migliorando la salute della vie aeree e diminuendo la produzione di muco e il broncospasmo, sortisce indirettamente effetti positivi sulla qualità del sonno.
Al contrario, purtroppo, l’aumento di peso spesso associato allo smettere di fumare, in media di almeno 2 kg ma che può anche superare i 10, ha risvolti estremamente negativi per i pazienti OSA sia in termini di outcome clinici e polisonnografici, che di impatto negativo sullo stato emotivo, con aumento di ansietà e diminuzione della motivazione necessaria per superare le difficoltà che i pazienti fumatori, obesi e apneici incontrano nel cambiare drasticamente stile di vita, soprattutto a lungo termine64.
5) La terapia per le OSA modifica l’abitudine al fumo?
Non ci sono dati certi sulle correlazioni tra terapia OSAS – fumo di sigaretta, ma nel primo studio longitudinale sugli effetti dell’uso prolungato di CPAP si evidenzia come il 60% di forti apneici fumatori, durante i circa 5 anni di terapia con CPAP, abbia smesso di fumare65. Ovviamente non è possibile imputare questo successo alla sola terapia con CPAP: è difatti più probabile che coloro i quali riescono a sottoporsi per lungo tempo alle terapie e dimostrino davvero di desiderare una vita migliore, entrino in un circuito virtuoso di maggiore attenzione verso la propria salute.
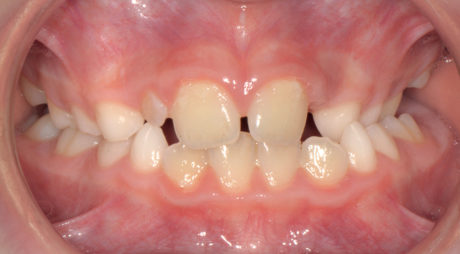
Fumo, sonno e gravidanza
Il legame tra fumo in gravidanza e salute fetale è già stato discusso in precedenza relativamente all’alterazione della soglia dei chemocettori periferici. Inoltre nicotina e monossido di carbonio superano la barriera placentare, causando:
- ridotto apporto di ossigeno nei tessuti fetali;
- aumento della frequenza cardiaca del feto;
- alterazioni dello sviluppo fetale;
- riduzione ponderale;
- aumentato rischio di malformazioni fetali;
- aumentato rischio di parto pretermine.
Di particolare interesse odontoiatrico è lo sviluppo di labio e/o palatoschisi, la malformazione facciale non sindromica più frequente nei nascituri: tale rischio è raddoppiato e sovrapponibile sia che la madre fumi da 1 a 10 sigarette al giorno66, sia che sia esposta a fumo passivo67. Per quanto riguarda i disturbi del sonno, il fumo materno durante la gravidanza quasi raddoppia il rischio per il neonato, da 1 giorno a 29 settimane, di sviluppare apnee del sonno (RR 1.76, 95% CI=1.17-2.64)68.
Se la madre è fumatrice il rischio di apnea rimane aumentato, seppur in maniera meno significativa, anche nei neonati dai 6 ai 18 mesi (RR 1.25, 95% CI=1.06-1.47)69. Naturalmente il rischio è maggiore dove entrambi i genitori sono fumatori, rispetto a dove solo uno lo è (p=0,007)68. Fumare durante la gravidanza non ha conseguenze solo sulla salute del nascituro ma anche sulla salute della futura madre, con un aumento di menorragie gravidiche e un’aumentata suscettibilità a infezioni batteriche e virali dovute a un abbassamento delle difese immunitarie. Per quanto riguarda il sonno, il periodo della gravidanza è già di per sé associato a un peggioramento della qualità dello stesso, e in parte legato ai fattori caratteristici del terzo trimestre come il bisogno di urinare più frequentemente, l’aumento del volume dell’addome, i movimenti del feto e l’aumento globale di peso70, 71. L’abbinamento fumo-gravidanza provoca soprattutto un aumento della sonnolenza diurna rispetto alle donne gravide non fumatrici, associato alle alterazioni tipiche dell’astinenza da nicotina già descritte72.
Le stesse alterazioni valgono anche per il fumo passivo. Un ampio studio giapponese condotto nel 2002 su 16.396 e nel 2006 su 19.386 donne gravide attraverso la somministrazione di questionari, mostra come il fumo passivo peggiori la qualità soggettiva del sonno, renda più difficile addormentarsi e respirare confortevolmente, favorisca il russamento e il risveglio precoce al mattino, accompagnato da un’aumentata sonnolenza diurna. I valori di questi parametri si trovano in un range intermedio tra quello riscontrato tra le donne gravide fumatrici e non fumatrici non sottoposte a fumo ambientale73.
Il fumo passivo nell’età dello sviluppo facciale
Anche il fumo passivo rappresenta una concreta minaccia per la salute a 360°, soprattutto per le fasce di popolazione più giovani e vulnerabili, dove le ripercussioni possono essere, soprattutto a distanza di anni, clinicamente molto rilevanti. Si pensi che uno studio longitudinale finlandese, condotto su quasi 2500 bambini seguiti a distanza di 26 anni, mostra che l’esposizione al SHS, dovuta a scarse misure di igiene comportamentale dei genitori, aumenta il rischio di sviluppare placche aterosclerotiche carotidee in età adulta (OR 4.0; 95% CI 1.7-9.8; P=0.002)74. Il SHS raddoppia inoltre le probabilità che, da adolescente, diventi egli stesso un fumatore a causa dell’aumentato numero di recettori nicotinici che facilitano l’assuefazione dell’adolescente in cerca di esperienza nuove43.



sorriso. Potete scaricare da
www.ildentistamoderno.com
questo decalogo, realizzato in collaborazione con Fondazione ISI, Fondazione Umberto Veronesi e Fondazione ANDI. Il questionario può essere una traccia da seguire durante un breve counseling con i pazienti
in studio e successivamente appeso nel luogo più frequentato della casa, soprattutto in caso di genitori fumatori
L’apparato che forse più risente del fumo passivo è quello respiratorio, con un aumento di incidenza di asma, riniti allergiche, tonsilliti, tosse e bronchiti75,76. Uno studio condotto a Cincinnati su oltre 200 bambini asmatici mostra infatti, tra quelli sottoposti a SHS rispetto ai coetanei che non lo erano, un crollo globale della qualità del sonno (p=.0002), con un’aumentata difficoltà a prendere sonno (p=.004), russamento (p=.02), parasonnie (p=.002) e sonnolenza diurna (p=.022)7. Un recente studio americano retrospettivo, condotto su giovani pazienti sotto i 15 anni, mostra come 121 (47.27%) su 256 piccoli pazienti sottoposti a tonsillectomia per tonsilliti ricorrenti siano sottoposti a SHS. Nel gruppo di controllo, formato da 241 bambini sottoposti ad altro intervento chirurgico addominale, solo 67 (27.80%) erano figli di fumatori. I bambini esposti a SHS mostrano quindi un rischio più che doppio di sviluppare tonsillectomie ricorrenti, tanto da necessitare l’intervento chirurgico (OR 2.49, p=0.004)77. Anche un importante studio multicentrico ha provato a indagare la correlazione tra la severità delle OSA e fattori di rischio come il sesso, l’età, la razza, l’indice di massa corporea, il fumo passivo, la nascita prematura e lo stato socio-economico. Analizzando le PSG di oltre 1220 bambini di età compresa tra i 5 e i 10 anni, candidati per essere sottoposti ad adenotonsillectomia, la razza afro-americana (p=0,002) e il SHS (p=0,026) sembrano essere correlati a un valore AHI del 20% più alto, sottolineando quindi il ruolo genetico e del fumo passivo nello sviluppo di gravi OSAS pediatriche78. Le difficoltà respiratorie croniche incontrate da questi bambini li inducono alla respirazione orale, con una sequela di ricadute sull’accrescimento oro-facciale molto note agli ortodontisti fin dagli anni ‘808,9. La respirazione orale altera infatti la normale postura linguale e in generale il tono muscolare facciale, fondamentali per lo sviluppo del massiccio facciale, creando un pattern di crescita sfavorevole, caratterizzato da:
- volta palatale stretta e profonda;
- micrognazia;
- sviluppo mandibolare in post-rotazione;
- ipotono e incompetenza labiale;
- ipotono dei muscoli masticatori;
- crossbite posteriori.
La respirazione orale e la particolare anatomia sopra descritta favoriscono il collasso delle vie aeree posteriori, aprendo la strada ai disturbi respiratori del sonno fin dalla tenera età79.
Se quindi è vero che i bambini con disturbi respiratori sono predisposti allo sviluppo di disturbi del sonno, lo saranno ancora di più quelli esposti al fumo passivo, sottoposti a ulteriori stress, quali l’infiammazione delle vie aeree a causa dei prodotti della combustione incompleta e all’astinenza da nicotina che avviene durante la notte, entrambi fattori che concorrono, come già illustrato per i pazienti adulti, a peggiorare la qualità del sonno.
Se il sonno è fondamentale per la salute degli adulti, lo è ancora di più nei bambini, dove la sua carenza cronica, soprattutto in caso di OSAS, può causare:
- turbe del comportamento;
- ritardi dello sviluppo cognitivo;
- problemi scolastici e di socializzazione;
- dismetabolismi e obesità;
- deficit di crescita staturale;
- enuresi notturna.
Sul quarto punto la ricerca si sta sviluppando molto, in quanto diabete e obesità infantili sono problemi dilaganti, con ricadute sulla salute gravissime e costi sociali esorbitanti80. Se nell’adulto un valore AHI inferiore a 5 viene considerato normale, le recenti Linee Guida Ministeriali pubblicate nel marzo 2016 specificano come per porre diagnosi di OSAS in un bambino bastino un AHI anche solo di 1 evento/ora, accompagnato da russamento e dalla presenza di un episodio di desaturazione di ossigeno sotto il 92%81.

L’OSAS è una condizione clinica che deve essere assolutamente e precocemente trattata per permettere la quanto più normale crescita psico-fisica del bimbo. In aggiunta, la respirazione orale rende la bocca un ambiente secco, con un’insufficiente autodetersione salivare e un aumento della cariorecettività82. I bambini figli di fumatori infatti presentano un aumento dell’incidenza della carie rispetto ai bimbi non esposti al SHS83.
Infine un’interessante revisione della letteratura condotta dal gruppo italiano di Castroflorio sul bruxismo nei bambini evidenzia come i bambini esposti a un intenso fumo passivo mostrano un aumento del bruxismo notturno (OR=4.5, CI=2.2-9.4) e che i bambini con disturbi respiratori del sonno presentano anch’essi un aumento del bruxismo (OR=3.3, CI=1.6-6.6), entrambe associazioni presenti anche negli adulti fumatori84.
Conclusioni
I diversi effetti nefasti del fumo sulla salute, generale e orale, sono stati ampiamente studiati e dimostrati. Gli stessi sul sonno sono un ambito di studio più recente, che necessita numerosi approfondimenti, soprattutto in ambito delle OSAS, dove la sindrome da overlap con le BPCO può sortire effetti confondenti.
È chiaro però che il consumo di sigarette è associato ad alterazioni dell’architettura del sonno, sia durante il periodo di fumo attivo che dopo la cessazione, dove il rischio di aumento del peso corporeo può gravemente peggiorare il quadro respiratorio e deve essere strettamente monitorato.
Il fumo presenta un’infinità di effetti negativi sulla salute orale e pertanto la sua cessazione deve essere dall’odontoiatra sempre caldamente incoraggiata, fornendo ai pazienti materiale informativo e gli indirizzi dei centri antifumo sul territorio.
Queste azioni devono essere tanto più incisive quanto più il paziente presenti fattori di rischio sovrapposti (problematiche respiratorie del sonno, cardiovascolari e dismetaboliche).
Fino a che i pazienti non comprenderanno l’importanza di una vita sana e attiva, la nostra battaglia per la loro salute, sia orale che generale, sarà vana. Noi abbiamo il dovere morale di dare il buon esempio, facendoci portatori di corretti stili di vita.
Questo discorso è ancora più importante nel caso di genitori fumatori, che fortunatamente si dimostrano più disposti al «sacrificio» per la salute dei propri figli.
Un bambino che non dorme bene oggi avrà altissime probabilità di essere un adulto gravemente malato domani: il ruolo dei dentisti pediatrici e degli ortodontisti è pertanto fondamentale per intercettare il più precocemente possibile i disturbi respiratori dei piccoli pazienti e per accompagnare i genitori lungo l’iter diagnostico-terapeutico, in stretta collaborazione con il pediatra e l’otorinolaringoiatra. Quale che sia la terapia, ortodontica con espansione palatale o chirurgica con adenoidectomia e/o tonsillectomia, l’educazione comportamentale dei genitori è fondamentale per rendere l’ambiente in cui cresce il figlio smoke-free.
Il fumo in casa deve essere fortissimamente scoraggiato, anche quello di «terza mano», che si deposita sui vestiti con cui poi vengono tenuti in braccio o abbracciati i figli85.
I genitori che sottopongono i figli al fumo di sigaretta devono sapere che stanno compromettendo la loro salute e il loro futuro.
Corrispondenza
giulia_borromeo@yahoo.it
1. Paglia L, Ginocchio L, Crespi A, Crippa R. Fumo e salute oro-facciale: analisi della letteratura e razionale scientifico. Il Dentista Moderno 2013;5:44-70.
2. World Health Organization. WHO Report on the Global Tobacco Epidemic, 2011.
3. Tregear S, Reston J, Schoelles K, Phillips B. Obstructive sleep apnea and risk of motor vehicle crash: systematic review and meta-analysis. J Clin Sleep Med 2009 Dec 15;5(6):573-81.
4. Fuhrman C, Fleury B, Nguyên XL, Delmas MC. Symptoms of sleep apnea syndrome: high prevalence and underdiagnosis in the French population. Sleep Med 2012 Aug;13(7):852-8.
5. http://www.gazzettaufficiale.it/eli/id/2016/01/13/16A00299/sg
6. Deleanu OC, Pocora D, Mih?lcu?? S, Ulmeanu R, Zaharie AM, Mih??an FD. Influence of smoking on sleep and obstructive sleep apnea syndrome. Pneumologia 2016 Jan-Mar;65(1):28-35.
7. Yolton K, Xu Y, Khoury J, Succop P, Lanphear B, Beebe DW, Owens J. Associations between secondhand smoke exposure and sleep patterns in children. Pediatrics 2010 Feb;125(2):e261-8.
8. Bresolin D, Shapiro PA, Shapiro GG, Chapko MK, Dassel S. Mouth breathing in allergic children: its relationship to dentofacial development. Am J Orthod 1983 Apr;83(4):334-40.
9. Principato J. Upper airway obstruction and craniofacial morphology. J.Otolaryngol Head Neck Surg 1991 Jun;104(6):881-90.
10. Kim KS, Kim JH, Park SY, Won HR, Lee HJ, Yang HS, Kim HJ. Smoking induces oropharyngeal narrowing and increases the severity of obstructive sleep apnea syndrome. J Clin Sleep Med 2012 Aug 15;8(4):367-74.
11. Lavie L, Lavie P. Smoking interacts with sleep apnea to increase cardiovascular risk. Sleep Med 2008 Mar;9(3):247-53.
12. Brouilette R, Hanson D, David R, Klemka L, Szatkowski A, Fernbach S, Hunt C. A diagnostic approach to suspected obstructive sleep apnea in children. J Pediatr 1984 Jul;105(1):10-4.
13. Lavigne G. La medicina del sonno per Odontoiatri, Quintessenza edizioni, 2012.
14. Tobaldini E, Costantino G, Solbiati M, Cogliati C, Kara T, Nobili L, Montano N. Sleep, sleep deprivation, autonomic nervous system and cardiovascular diseases. Neurosci Biobehav Rev 2016 Jul 7.
15. Halász P1, Terzano M, Parrino L, Bódizs R. The nature of arousal in sleep. J Sleep Res 2004 Mar;13(1):1-23.
16. Lavigne GJ, Khoury S, Abe S, Yamaguchi T, Raphael K. Bruxism physiology and pathology: an overview for clinicians. J Oral Rehabil 2008 Jul;35(7):476-94.
17. Macaluso GM, Guerra P, Di Giovanni G, Boselli M, Parrino L, Terzano MG. Sleep bruxism is a disorder related to periodic arousals during sleep. J Dent Res 1998 Apr;77(4):565-73.
18. Johansson A, Omar R, Carlsson GE. Bruxism and prosthetic treatment: a critical review. J Prosthodont Res 2011 Jul;55(3):127-36
19. Salvi GE, Brägger U. Mechanical and technical risks in implant therapy. Int J Oral Maxillofac Implants 2009;24 Suppl:69-85.
20. Kostrzewa-Janicka J, Jurkowski P, Zycinska K, Przybyłowska D, Mierzwi?ska-Nastalska E. Sleep-Related Breathing Disorders and Bruxism. Adv Exp Med Biol 2015;873:9-14.
21. Chan CH, Wong BM, Tang JL, Ng DK. Gender difference in snoring and how it changes with age: systematic review and meta-regression. Sleep Breath 2012 Dec;16(4):977-86.
22. Pépin JL, Guillot M, Tamisier R, Lévy P. The upper airway resistance syndrome. Respiration 2012;83(6):559-66.
23. American Academy of Sleep Medicine. International Classification of Sleep Disorders, ed. 2 Westchester, IL: America Academy of Sleep Medicine, 2005:297.
24. Young T, Peppard PE, Gottlieb DJ. Epidemiology of obstructive sleep apnea: a population health perspective. Am J Respir Crit Care Med 2002 May 1;165(9):1217-39
25. The Report of an American Academy of Sleep Medicine Task Force. Sleep-related breathing disorders in adults: recommendations for syndrome definition and measurement techniques in clinical research. Sleep 1999 Aug 1;22(5):667-89.
26. Eckert DJ, Younes MK. Arousal from sleep: implications for obstructive sleep apnea pathogenesis and treatment. J Appl Physiol 1985. 2014 Feb 1;116(3):302-13.
27. Phillips CL, Cistulli PA. Obstructive sleep apnea and hypertension: epidemiology, mechanisms and treatment effects. Minerva Med 2006 Aug;97(4):299-312.
28. Gozal D. Sleep, sleep disorders and inflammation in children. Sleep Med 2009;10 Suppl 1:S12-S16.
29. Greco C, Spallone V. Obstructive Sleep Apnoea Syndrome and Diabetes. Fortuitous Association or Interaction? Curr Diabetes Rev 2015;12(2):129-55.
30. Michiels C, Tellier C, Feron O. Cycling hypoxia: A key feature of the tumor microenvironment. Biochim Biophys Acta 2016 Aug;1866(1):76-86.
31. Boulet L, Flore P, Le Gouellec A, Toussaint B, Pépin JL, Faure P. Is tryptophan metabolism involved in sleep apnea-related cardiovascular co-morbidities and cancer progression? Med Hypotheses 2015 Oct;85(4):415-23.
32. Wetter DW, Young TB. The relation between cigarette smoking and sleep disturbance. Prev Med 1994 May;23(3):328-34.
33. Phillips BA, Danner FJ. Cigarette smoking and sleep disturbance. Arch Intern Med 1995 Apr 10;155(7):734-7.
34. McNamara JP, Wang J, Holiday DB, Warren JY, Paradoa M, Balkhi AM, Fernandez-Baca J, McCrae CS. Sleep disturbances associated with cigarette smoking. Psychol Health Med 2014;19(4):410-9.
35. Branstetter SA, Horton WJ, Mercincavage M, Buxton OM. Severity of Nicotine Addiction and Disruptions in Sleep Mediated by Early Awakenings. Nicotine Tob Res 2016 Jul 14.
36. Zhang L, Samet J, Caffo B, Bankman I, Punjabi NM. Power spectral analysis of EEG activity during sleep in cigarette smokers. Chest 2008 Feb;133(2):427-32.
37. DiFranza JR, Aligne CA, Weitzman M. Prenatal and postnatal environmental tobacco smoke exposure and children’s health. Pediatrics 2004 Apr;113(4 Suppl):1007-15.
38. de Jonge GA, Burgmeijer RJ, Engelberts AC, Hoogenboezem J, Kostense PJ, Sprij AJ. Sleeping position for infants and cot death in The Netherlands 1985-91. Arch Dis Child 1993 Dec;69(6):660-3.
39. Liebrechts-Akkerman G, Lao O, Liu F, van Sleuwen BE, Engelberts AC, L’hoir MP, Tiemeier HW, Kayser M. Postnatal parental smoking: an important risk factor for SIDS. Eur J Pediatr 2011 Oct;170(10):1281-91.
40. Sawnani H, Jackson T, Murphy T, Beckerman R, Simakajornboon N. The effect of maternal smoking on respiratory and arousal patterns in preterm infants during sleep. Am J Respir Crit Care Med 2004 Mar 15;169(6):733-8.
41. Falk L, Nordberg A, Seiger A, Kjaeldgaard A, Hellstrom-Lindahl E. Smoking during early pregnancy affects the expression pattern of both nicotinic and muscarinic acetylcholine receptors in human first trimester brainstem and cerebellum. Neuroscience 2005;132:389-97.
42. Lavezzi AM, Ottaviani G, Mingrone R, Matturri L. Analysis of the human locus coeruleus in perinatal and infant sudden unexplained deaths. Possible role of the cigarette smoking in the development of this nucleus. Dev Brain Res 2005;154:71-80.
43. Gorini G, Carreras G, Cortini B, Verdi S, Petronio MG, Sestini P, Chellini E. Smoke-free homes and youth smoking behaviour in Italy: findings from the SIDRIAT longitudinal study. Nicotine Tob Res 2016 Jun 9.
44. Lin YN, Li QY, Zhang XJ. Interaction between smoking and obstructive sleep apnea: not just participants. Chin Med J (Engl) 2012 Sep;125(17):3150-6.
45. Conway SG et al. Effect of smoking habits on sleep. Braz J Med Biol Res 41(8) 2008:722-7.
46. Kim KS, Kim JH, Park SY, Won HR, Lee HJ, Yang HS, Kim HJ. Smoking induces oropharyngeal narrowing and increases the severity of obstructive sleep apnea syndrome. J Clin Sleep Med 2012 Aug 15;8(4):367-74.
47. Virkkula P, Hytönen M, Bachour A, Malmberg H, Hurmerinta K, Salmi T, Maasilta P. Smoking and improvement after nasal surgery in snoring men. Am J Rhinol 2007 Mar-Apr;21(2):169-73.
48. Vestbo J1, Hurd SS, Agustí AG, Jones PW, Vogelmeier C, Anzueto A, Barnes PJ, Fabbri LM, Martinez FJ, Nishimura M, Stockley RA, Sin DD, Rodriguez-Roisin R. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: GOLD executive summary. Am J Respir Crit Care Med 2013 Feb 15;187(4):347-65.
49. Viviers PJ, van Zyl-Smit RN. Chronic obstructive pulmonary disease, diagnosis and classification of severity. S Afr Med J 2015 Sep;105(9):786-8.
50. McNicholas WT. Chronic obstructive pulmonary disease and obstructive sleep apnea: overlaps in pathophysiology, systemic inflammation, and cardiovascular disease. Am J Respir Crit Care Med 2009 Oct 15;180(8):692-700.
51. Ohayon MM, Li KK, Guilleminault C Risk factors for sleep bruxism in the general population. Chest 2001 Jan 119(1):53-61.
52. Lavigne GJ, Huynh N, Kato T, Okura K, Adachi K, Yao D, Sessle B. Genesis of sleep bruxism: motor and autonomic-cardiac interactions. Arch Oral Biol 2007 Apr;52(4):381-4.
53. Macaluso GM, Guerra P, Di Giovanni G, Boselli M, Parrino L, Terzano MG. Sleep bruxism is a disorder related to periodic arousals during sleep. J Dent Res 1998 Apr;77(4):565-73.
54. Rintakoski K, Ahlberg J, Hublin C, Broms U, Madden PA, Könönen M, Koskenvuo M, Lobbezoo F, Kaprio J. Bruxism is associated with nicotine dependence: a nationwide Finnish twin cohort study. Nicotine Tob Res 2010 Dec;12(12):1254-60.
55. Lavigne GL, Lobbezoo F, Rompré PH, Nielsen TA, Montplaisir J. Cigarette smoking as a risk factor or an exacerbating factor for restless legs syndrome and sleep bruxism. Sleep 1997 Apr;20(4):290-3.
56. Krishnan V, Dixon-Williams S, Thornton JD. Where there is smoke…there is sleep apnea: exploring the relationship between smoking and sleep apnea. Chest 2014 Dec;146(6):1673-80.
57. Wetter DW, Young TB, Bidwell TR, Badr MS, Palta Smoking as a risk factor for sleep-disordered breathing. M. Arch Intern Med 1994 Oct 10;154(19):2219-24.
58. Kashyap R, Hock LM, Bowman TJ. Higher prevalence of smoking in patients diagnosed as having obstructive sleep apnea. Sleep Breath 2001 Dec;5(4):167-72.
59. Schrand JR. Is sleep apnea a predisposing factor for tobacco use? Med Hypotheses 1996 Dec;47(6):443-8.
60. Changeux JP, Bertrand D, Corringer PJ, Dehaene S, Edelstein S, Léna C, Le Novère N, Marubio L, Picciotto M, Zoli M. Brain nicotinic receptors: structure and regulation, role in learning and reinforcement. Brain Res Brain Res Rev 1998 May;26(2-3):198-216.
61. Collins AC. Genetic influences on tobacco use: a review of human and animal studies. Int J Addict 1990-1991;25(1A):35-55
62. Guzmán-Marín R, Alam MN, Mihailescu S, Szymusiak R, McGinty D, Drucker-Colín R. Subcutaneous administration of nicotine changes dorsal raphe serotonergic neurons discharge rate during REM sleep. Brain Res 2001 Jan 12;888(2):321-5.
63. Zevin S, Swed E, Cahan C. Clinical effects of locally delivered nicotine in obstructive sleep apnea syndrome. Am J Ther 2003 May-Jun;10(3):170-5.
64. Williamson DF, Madans J, Anda RF, Kleinman JC, Giovino GA, Byers T. Smoking cessation and severity of weight gain in a national cohort. N Engl J Med 1991 Mar 14;324(11):739-45.
65. Chaouat A, Weitzenblum E, Kessler R, Oswald M, Sforza E, Liegeon MN, Krieger J.Five-year effects of nasal continuous positive airway pressure in obstructive sleep apnoea syndrome.Eur Respir J 1997 Nov;10(11):2578-82.
66. Little J, Cardy A, Arslan MT, Gilmour M, Mossey PA. Smoking and orofacial clefts: a United Kingdom-based case-control study. Cleft Palate Craniofac J 2004 Jul;41(4):381-6.
67. Sabbagh HJ, Hassan MH, Innes NP, Elkodary HM, Little J, Mossey PA. Passive smoking in the etiology of non-syndromic orofacial clefts: a systematic review and meta-analysis. PLoS One 2015 Mar 11;10(3).
68. Kahn A, Groswasser J, Sottiaux M, Kelmanson I, Rebuffat E, Franco P et al. Prenatal exposure to cigarettes in infants with obstructive sleep apneas. Pediatrics 1994 May;93(5):778-83.
69. Kukla L, Hruba D, Tyrlik M. Influence of exposure to passive smoking after the birth on health status of children in suckling and toddler’s ages. Results of ELSPAC study. Cesko-Slovenska Pediatrie 2005;60(2):62-9.
70. Lee KA. Alterations in sleep during pregnancy and postpartum: a review of 30 years of research. Sleep Med Rev 1998 Nov; 2(4):231-42.
71. Izci Balserak B. Sleep disordered breathing in pregnancy. Breathe (Sheff). 2015 Dec;11(4):268-77.
72. Kaneita Y, Ohida T, Takemura S, Sone T, Suzuki K, Miyake T, Yokoyama E, Umeda T. Relation of smoking and drinking to sleep disturbance among Japanese pregnant women. Prev Med 2005 Nov-Dec; 41(5-6):877-82.
73. Ohida T, Kaneita Y, Osaki Y, Harano S, Tanihata T, Takemura S, Wada K, Kanda H, Hayashi K, Uchiyama M. Is passive smoking associated with sleep disturbance among pregnant women? Sleep 2007 Sep;30(9):1155-61.
74. West HW, Juonala M, Gall SL, Kähönen M, Laitinen T, Taittonen L, Viikari JS, Raitakari OT, Magnussen CG. Exposure to parental smoking in childhood is associated with increased risk of carotid atherosclerotic plaque in adulthood: the Cardiovascular Risk in Young Finns Study. Circulation 2015 Apr 7;131(14):1239-46.
75. Akinbami LJ, Moorman JE, Garbe PL, Sondik EJ. Status of childhood asthma in the United States,1980-2007. Pediatrics Mar; 2009 123(3):S131-145.
76. McEvoy CT, Spindel ER. Pulmonary Effects of Maternal Smoking on the Fetus and Child: Effects on Lung Development, Respiratory Morbidities, and Life Long Lung Health. Paediatr Respir Rev 2016 Aug 19. pii: S1526-0542(16)30079-3.
77. Straight CE, Patel HH, Lehman EB, Carr MM. Prevalence of smoke exposure amongst children who undergo tonsillectomy for recurrent tonsillitis. Int J Pediatr Otorhinolaryngol 2015 Feb;79(2):157-60.
78. Weinstock TG, Rosen CL, Marcus CL, Garetz S, Mitchell RB, Amin R, Paruthi S, Katz E, Arens R, Weng J, Ross K, Chervin RD, Ellenberg S, Wang R, Redline S. Predictors of obstructive sleep apnea severity in adenotonsillectomy candidates. Sleep 2014 Feb 1;37(2):261-9.
79. Defabjanis P. Impact of nasal airway obstruction on dentofacial development and sleep disturbances in children: preliminary notes. J Clin Pediatr Dent 2003 Winter;27(2):95-100.
80. Ievers-Landis CE, Redline S. Pediatric sleep apnea: implications of the epidemic of childhood overweight. Am J Respir Crit Care Med 2007 Mar 1;175(5):436-41.
81. http://www.salute.gov.it/imgs/C_17_pubblicazioni_2484_allegato.pdf
82. Widmer RP. Oral health of children with respiratory diseases. Paediatr Respir Rev 2010 Dec;11(4):226-32.
83. Hanioka T, Ojima M, Tanaka K, Yamamoto M. Does secondhand smoke affect the development of dental caries in children? A systematic review. J Environ Res Public Health 2011 May;8(5):1503-19.
84. Castroflorio T, Bargellini A, Rossini G, Cugliari G, Rainoldi A, Deregibus A. Risk factors related to sleep bruxism in children: A systematic literature review. Arch Oral Biol 2015 Nov;60(11):1618-24.
85. Acuff L, Fristoe K, Hamblen J, Smith M, Chen J. Influence of smoking on sleep and obstructive sleep apnea syndrome. Third-Hand Smoke: Old Smoke, New Concerns. J Community Health 2016 Jun;41(3):680-7.







