Judit Nemes, D.M.D., Ph.D.1
Béla Nagy, M.D., Ph.D.2
Márta Alberth, M.D., L.D.S., Ph.D.1
1Department of Pediatric Dentistry and Orthodontics - University of Debrecen, Hungary
2Department of Pediatrics - University of Debrecen, Hungary
L'asma è un disturbo cronico molto diffuso nei bambini, caratterizzato da infiammazione dei bronchi con vie aeree ipersensibilizzate che porta a episodi ricorrenti di rantolii, tensione toracica, difficoltà a respirare associati a tosse, in particolar modo con frequenza accentuata nella notte e nella prima mattinata. Questi episodi sono spesso associati con ostruzione delle vie aeree che sono di tipo generalmente reversibile, in modo spontaneo o attraverso trattamento terapeutico1.Negli ultimi decenni l’asma è diventata sempre più diffusa, sia negli adulti che nei bambini. L’aumento della prevalenza dell’asma, parallelamente a un incremento similare di altri disordini di tipo allergico come eczemi e riniti, ha portato allo studio dell’associazione con l’incremento della sensibilità cutanea. La prevalenza dell’asma diagnosticata va dallo 0,7% al 18,4% nelle popolazioni di diverse aree geografiche2. Nonostante la prevalenza dell’asma sia relativamente bassa nelle regioni dell’Europa dell’Est, negli ultimi anni si è assistito a un incremento di bambini con questa patologia. Uno studio ungherese di Budapest riferisce del 2,26% nel 1999 e 2,68% nel 20033. Un altro studio proveniente da una diversa regione dell’Ungheria (Baranya) nel 2006 ha rilevato che il 6,7% dei ragazzi di età compresa tra i 6 e i 14 anni soffre di asma diagnosticata clinicamente4. Nella prima infanzia la patologia è più comune nei maschi, ma durante la pubertà (tra gli 11 e i 16 anni) si assiste a un cambiamento di genere, con una più alta prevalenza nella popolazione femminile ai 16 anni5.
Il “Global Initiative for Asthma” (GINA) classifica la malattia in 4 gruppi a seconda della gravità della manifestazione clinica. La gravità della malattia è valutata in base al livello dei sintomi e alla funzionalità polmonare: intermittente (GINA I), debolmente persistente (GINA II), moderatamente persistente (GINA III), altamente persistente (GINA IV)1. Questa classificazione non è raccomandata come base su cui progettare i trattamenti terapeutici poiché una verifica periodica del controllo dei fenomeni asmatici è più utile e rilevante6. Un controllo sia parziale che completo delle manifestazioni cliniche può essere ottenuto con una somministrazione giornaliera di farmaci anti infiammatori e uso di rimedi d’urgenza dosati secondo necessità7.
Diversi farmaci per l’asma sono disponibili in forma inalatoria, in tre soluzioni principali: il metodo più comunemente utilizzato è il dosatore calibrato (MDI) che utilizza un propellente chimico per spingere la medicazione al di fuori dell’inalatore; i nebulizzatori, invece, trasportano l’aerosol attraverso una maschera facciale utilizzando aria od ossigeno in pressione; infine, gli inalatori a polvere secca (DPI) che trasportano il farmaco senza utilizzo di propellenti chimici. Gli inalatori sono molto vantaggiosi perché i farmaci vengono trasportati direttamente all’interno delle vie aeree, dando quindi una maggior efficacia e un minor rischio di effetti collaterali8. Nonostante questo, diversi studi hanno dimostrato effetti collaterali locali in associazione con terapie a base di corticosteroidi, evidenziando in particolar modo candidosi orofaringea9, disfonia10, xerostomia, ulcerazione della mucosa orale11, erosione dentale12 e carie13. Trattamenti a lungo termine con alte dosi possono aumentare il rischio di effetti collaterali1. Lo scopo di questo studio è quello di valutare lo stato di igiene orale di bambini che assumono diversi tipi di farmaci per l’asma e di confrontare la salute orale e le abitudini di gruppi trattati con diversi farmaci.
Materiali e metodi
Il gruppo di studio è costituito da 49 bambini e adolescenti trattati per asma presso la “Division of Pulmonology, Department of Pediatrics, Medical and Health Science Center, University” di Debrecen. 30 maschi e 19 femmine presentavano un’età media di 9,02 anni, in un range compreso tra 4 e 17 anni. È stato ottenuto un consenso informato scritto da parte dei tutori dei partecipanti. Le condizioni orali e dentali sono state valutate senza conoscere la gravità del disturbo asmatico, il tipo e la durata della terapia farmacologica. Lo studio è stato condotto secondo le linee guida dell’Organizzazione Mondiale della Sanità (OMS) sulla valutazione delle patologie cariose14. È stato raccolto l’indice per la carie valutando denti cariati, mancanti, superfici otturate (dmf-s, DMF-S) e placca (Silness-Löe Plaque Index15). Lo status dentale è stato valutato con l’aiuto strumentale di uno specchietto e di una sonda.
I genitori hanno compilato un questionario nel quale dovevano descrivere la dieta e le abitudini di igiene orale dei bambini. I dati riguardanti lo stato di salute dei pazienti (gravità della patologia, data della diagnosi e somministrazione farmacologica) sono stati presentati dal pediatra solo dopo l’esame della cavità orale. Per differenziare in gruppi i bambini asmatici sono state utilizzate tre variabili: (1) gravità dell’asma al momento di valutazione iniziale del paziente, (2) tipo di terapia farmacologica e (3) durata della terapia.
I farmaci per inalazione utilizzati nei gruppi di pazienti sono stati:
- budesonide (inalatore pressurizzato a dose fissa [pMDI], 50 μg/dose) 100 μg due volte al giorno;
- budesonide (inalatore a polvere secca [DPI], 100 μg/dose), 100 μg due volte al giorno;
- fluticasone (pMDI, 125 μg/dose), 125 μg due volte al giorno;
- fluticasone (DPI, 100 o 250 μg/dose), 100 o 250 μg due volte al giorno;
- ciclesonide (pMDI, 160 μg/dose), una volta al giorno;
- fluticasone+salmeterol (DPI, 100 o 250 μg/dose), 100 o 250 μg due volte al giorno;
- budesonide+formoterol (DPI, 80/4.5 μg o 160/4.5 μg /dose), due volte al giorno.
I pazienti con reflusso gastrointestinale sono stati esclusi. Le analisi statistiche sono state condotte con il software Statistical Package for Social Sciences, versione 13.0 (SPSS Inc., Chicago, Illinois, USA). Le variabili categoriche sono state analizzate con il test di chi-quadro. Il t-test a campioni indipendenti e ANOVA sono stati utilizzati per verificare la significatività statistica delle differenze osservate tra i gruppi. Il livello di significatività è stato stabilito allo 0,05.
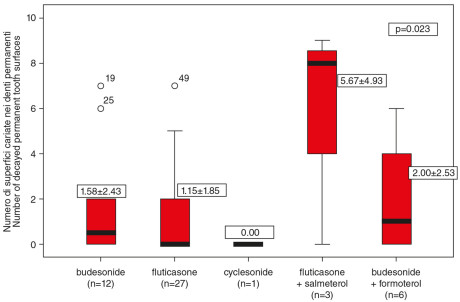
1. Relationship between medication and number of decayed tooth surfaces.
Risultati
La durata della terapia nel gruppo studio era compresa tra 1 e 10 anni, con una media di 3,59 anni. Il valore medio rilevato di dmf-s è stato 5,51, mentre di DMF-S 2,36. La componente più determinante in questo risultato è stato il numero delle superfici cariate (d-s, D-S). Nel caso di dentizione primaria il valore è stato di 5,43 (SD±7,95) in un range compreso tra 0 e 25. Per quanto invece riguarda i denti permanenti, il valore medio di superfici coinvolte era di 1,61 (SD±2,43) in un range tra 0 e 9. Il PI è risultato essere 0,99 (SD±0,47). Il genere, la gravità dei sintomi asmatici e il numero di volte al giorno in cui i pazienti si lavano i denti non ha effetti statisticamente significativi sulla presenza di carie e sull’indice di placca. È stata trovata invece una correlazione significativa tra il numero di denti permanenti cariati (D-S) e il tipo di terapia farmacologica (p=0,023, Figura 1). I bambini che ricevevano sia corticosteroidi inalati che agonisti-ß2 hanno mostrato un più alto PI (p=0,001) e maggiore D-S di quanti, invece, ricevevano solo somministrazione di corticosteroidi inalati (Figure 2, 3).
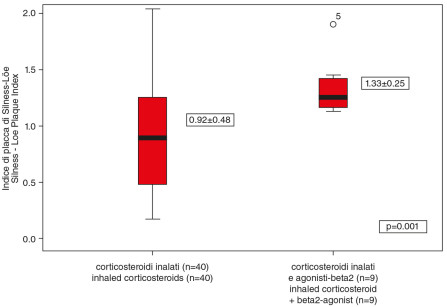
2. Relationship between combination of asthma medication and plaque indices.
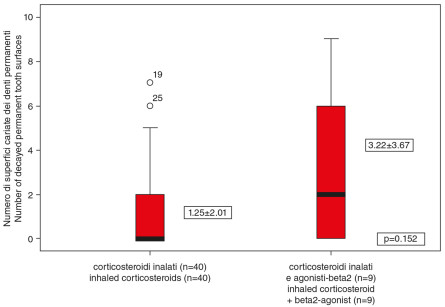
3. Relationship between the combination of asthma medication and number of decayed permanent tooth surfaces.
La durata della terapia per l’asma ha mostrato effetti significativi sulle patologie cariose a carico degli elementi definitivi a distanza di 3 anni (p=0,003). Gli inalatori a polvere secca hanno causato un indice di placca e carie significativamente maggiore degli altri gruppi con aerosol in caso di dentizione mista o definitiva (p=0,001 e p<0,001, Figure 4, 5). L’assunzione regolare di bevande contenenti carboidrati influenza il numero di denti decidui cariati, mentre mangiare snack durante il giorno influisce sul numero di denti permanenti cariati (p=0,033, Figure 6, 7). Nel caso della dentizione decidua è stato ritrovato un indice di placca significativamente più basso che nella dentizione mista o permanente (p=0,025, Figura 8). La correlazione tra PI e D-S è risultata significativa per tutta la popolazione (p<0,001).
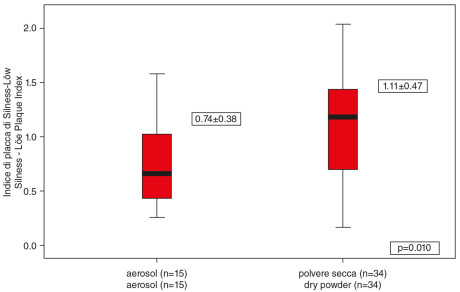
4. Relationship between the form of inhaled medication and plaque indices.
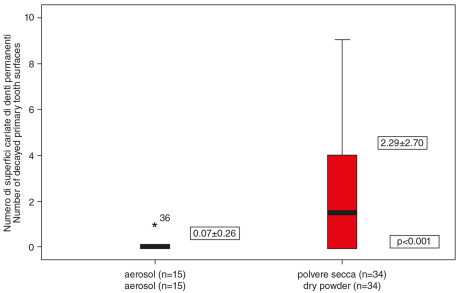
5. Relationship between the form of inhaled medication and and the number of the decayed permanent tooth surfaces.
Discussione
I corticosteroidi per inalazione (budesonide, fluticasone, ciclesonide) sono i farmaci più efficaci nella terapia di controllo e, per questo motivo, sono indicati per il trattamento dell’asma nei pazienti di tutte le età. Questi farmaci sono in grado di migliorare la situazione clinica, la funzionalità polmonare e conseguentemente la qualità della vita, riducendo la frequenza delle manifestazioni asmatiche acute e il ricorso a strutture ospedaliere16. Nel caso in cui non sia possibile controllare l’asma con bassi (100-200/μg) o medi (200-400/μg) dosaggi giornalieri di corticosteroidi inalati, viene presa in considerazione la combinazione con agonisti-ß2 a lento rilascio. Gli agonisti-ß2 ad azione rapida (formoterol) e lenta (salmeterol) sono degli efficaci broncodilatatori e andrebbero sempre usati in combinazione17. Nonostante siano farmaci ben tollerati anche nei bambini, sono stati osservati effetti collaterali sia a livello sistemico che locale, nel lungo periodo18. Diversi studi hanno evidenziato come i bambini trattati per l’asma abbiano una maggior incidenza di carie rispetto ai pazienti sani13,19,20, mentre altri articoli non hanno trovato differenze significative tra soggetti asmatici e non21-23. Matthews, dopo aver effettuato una revisione su 18 studi attinenti, ha sostenuto che l’asma potesse duplicare il rischio di carie sia in dentizione decidua che permanente13. Il maggior rischio di carie è associato alla minor produzione salivare, spesso causata dall’azione degli agonisti-ß2 a lento rilascio24. Kargul et al. hanno dimostrato che il pH delle cavità orali scendeva a 5,5 a mezz’ora di distanza dall’assunzione di una terapia con inalatore per asma25.
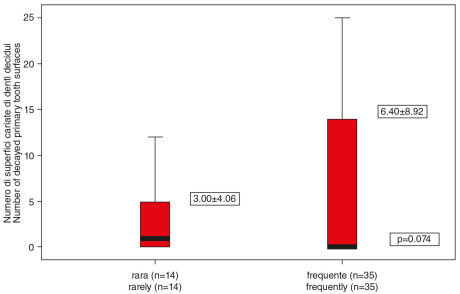
6. Relationship between frequency of intake of highly cariogenic drinks and number of decayed primary tooth surfaces.
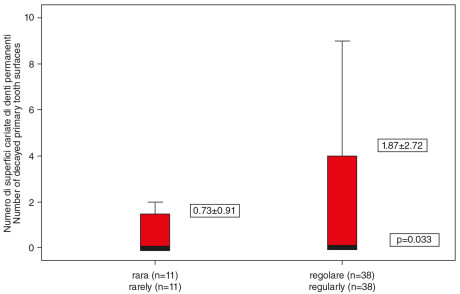
7. Relationship between frequency of snacking and number of decayed permanent tooth surfaces.
Nella formulazione DPI gli ingredienti attivi di dimensioni microscopiche sono associati a carrier più grandi, gli eccipienti. Gli eccipienti sono utilizzati quindi per incrementare la stabilità fisica e chimica del componente farmaceutico attivo e le sue capacità meccaniche e farmacologiche, come la solubilità e la penetrazione nei tessuti. Gli eccipienti permettono di creare delle masse di farmaco più sfruttabili in termini di maneggevolezza, somministrazione e misurazione della componente terapeutica; inoltre sono in grado di mascherare il sapore originale e sgradevole del farmaco26. Al giorno d’oggi il lattosio è l’eccipiente più frequentemente utilizzato. I DPI contengono generalmente 12,5-25 mg di lattosio per dose. Componenti alternativi, ma meno comuni, possono essere il mannitolo e il glucosio27,28. Il lattosio, nonostante sia considerato meno cariogeno del glucosio, viene rapidamente fatto fermentare per azione degli streptococchi (tra cui lo Streptococco mutans) e può causare una diminuzione del pH della cavità orale29. Il basso valore di pH, in associazione con una ridotta produzione di saliva, rende i bambini asmatici più suscettibili alla carie30. Ryberg et al. hanno evidenziato, dopo uno studio con 4 anni di follow up, che i pazienti asmatici trattati con agonisti-ß2 avevano una maggiore suscettibilità alla carie a causa di una ridotta produzione di saliva indotta dai farmaci assunti contro l’asma31. Nel nostro studio la patologia cariosa è risultata più alta nei pazienti che prendevano corticosteroidi per via inalatoria associati ad agonisti-ß2 presi attraverso un inalatore a polvere secca. Il tempo di esposizione ha influenzato la prevalenza di carie a distanza di 3 anni. Sag et al. hanno trovato una correlazione significativa tra il trattamento combinato e la riduzione del flusso salivare, con conseguente incremento di indice di placca in bambini e adolescenti32. Milano et al. dopo aver esaminato 179 pazienti asmatici in età pediatrica hanno evidenziato come la frequenza dell’assunzione di farmaci per l’asma fosse proporzionale alla suscettibilità alla carie. I bambini che usavano il farmaco per l’asma più di due volte al giorno risultavano decisamente più propensi a sviluppare carie sia nella dentizione decidua che in quella permanente.
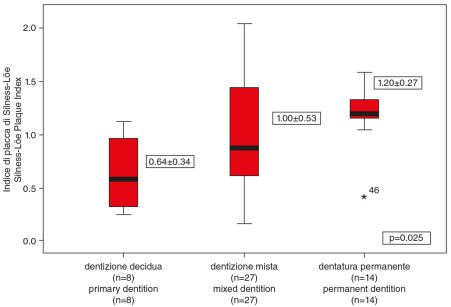
8. Relationship between type of dentition and plaque indices.
Tuttavia, la durata del trattamento per l’asma è risultata associata con una minore suscettibilità33. Il nostro studio mostra come il fattore più influente sulla salute orale è la durata e non la frequenza dell’inalazione di farmaci per l’asma. Non è stato possibile tuttavia trovare alcuna associazione tra la gravità della patologia e le condizioni orali, così come già descritto da Eloot et al.34, ma in contrapposizione con quanto espresso da Reddy e collaboratori35. Wogelius et al. descrissero come il trattamento per l’asma incrementasse il rischio di carie nei molari appena erotti36. Questi risultati contradditori possono essere parzialmente giustificati dalle differenze di età nei gruppi e dai diversi tipi di farmaci utilizzati. Nel nostro protocollo, confrontando i diversi farmaci e la durata della terapia, abbiamo riscontrato che la durata della terapia inalatoria può influenzare il rischio di carie dopo 3 anni, e la terapia combinata con inalatori a polvere secca può indurre un deterioramento dello stato di salute orale dei bambini asmatici. Per minimizzare il rischio di carie, in particolar modo in questi soggetti, è consigliabile una serie regolare di richiami e screening preventivi odontoiatrici. I farmaci per inalazione infatti non solo innalzano il rischio di carie, ma possono accrescere il rischio di patologie orali; tuttavia, con una corretta igiene orale questo rischio può essere controllato. È consigliabile somministrare la terapia anti asmatica prima dell’igiene orale domiciliare al mattino e alla sera. Se per qualche motivo non fosse possibile effettuare lo spazzolamento, anche il risciacquo può essere utile per rimuovere i residui di farmaco dopo l’inalazione. Effettuare risciacqui e gargarismi con acqua (o con collutori contenenti fluoro) in combinazione con lo spazzolamento è risultata essere la tecnica più efficace37.
The Global Initiative for Asthma (GINA) classified the disease into 4 groups according to the severity of the disease. Severity of the disease is based on the level of symptoms and lung function variability: intermittent (GINA I), mild persistent (GINA II), moderate persistent (GINA III) or severe persistent (GINA IV)1. This classification is not recommended as the basis for ongoing treatment decisions, because a periodic assessment of asthma control is more relevant and useful6. A partially or complete clinical control can be achieved and maintained with daily administration of anti-inflammatory medications and relievers used on an as-needed basis7. There are several asthma medications available in inhaled form. There are three basic types of devices for inhaled medications delivery. The most common is the metered – dose inhaler (MDI), which uses a chemical propellant to push the medication out of the inhaler. Nebulizers deliver aerosols through a face mask, using air or oxygen under pressure. Dry powder inhalers (DPIs) deliver medication without using chemical propellants. Inhalers are very advantageous because drugs are delivered directly into the airways producing higher efficacy and less risk of systemic side effects8. Several studies demonstrated, however, local adverse effects in association with the widely used corticosteroid therapy such as oropharyngeal candidasis9, dysphonia10, xerostomia and, ulceration of the oral mucosa11, as well as dental erosion12 and caries13. Long-term treatment with higher doses can increase the risk of these adverse effects1. The aim of the present study was to investigate the oral health status of children on different type of medication and to compare the oral health parameter and habits of groups of children with different asthma medications. Material and methods Gastro-esophageal reflux had been excluded in all patients. Data analysis was performed using the software Statistical Package for Social Sciences, version 13.0 (SPSS Inc., Chicago, Illinois, USA). Categorical variables were analyzed using chi-squared test. Independent t-test and one-way ANOVA were used to assess the statistical significance of the differences in the studied continuous variables between the groups. The level of statistical significance for all tests was set at 0.05. Results Discussion In our study the caries prevalence was the highest in those taking inhalative corticosteroid together with long-acting ß2-agonist from a dry powder inhalator. The exposure time to the asthma medication significantly influenced caries prevalence after 3 years. Sag and co-workers found significant association between combination treatment, decrease in the salivary flow rate and increase of the plaque indices in children and adolescents32. Milano et al. after examining 179 asthmatic children concluded that increased frequency of asthma medication use was associated with increased likelihood of caries experience. Children who used their medication greater than twice daily were significantly more likely to experience dental disease both in primary and mixed dentitions. On the other hand, the duration of asthma treatment was associated with a decreased likelihood of caries experience33. Our study results show that the main factor to influence the oral health was the duration and not the frequency of the anti-asthmatic drug inhalation. We could not find, however, any association between the severity of the asthma and the oral condition, similarly to Eloot et al.34 but in contrary to Reddy and co-workers35. Wogelius et al concluded that asthma-drugs may increase the risk of caries in newly erupted permanent molars36. These contradictory results can partly be explained with the different age-groups investigated, and the different type of medication they used. In our study comparing the different medicaments and the duration of the treatment we found that the length of inhalative therapy can influence the caries rate after 3 years, and combination therapy delivered by dry powder inhalers might have significant deteriorating effect on the oral health of asthmatic children. In order to minimize the caries risk regular dental screenings and preventive measures are required. Inhaled asthma drugs may increase not only the risk of dental caries but the risk of oral infections too. With proper oral hygiene asthmatics can reduce this risk too. It’s advisable to administer the asthma-drugs before the regular tooth brushing in the morning and in the evening. If brushing is inconvenient for some reason, mouth washing has a significant influence on the removal of drug residues following inhalation of asthma medication. Gargling and rinsing with water (or fluoride containing mouth rinses) in combination considered to be the most effective37.
Asthma is a very common chronic disease in childhood characterized by bronchial inflammation with airway hyperresponsiveness that leads to recurrent episodes of wheezing, chest tightness, and breathlessness together with coughing particularly at night or in the early morning. These episodes are associated with airway obstruction that is often reversible either spontaneously or with treatment1. Asthma has become more common in both children and adults around the world in recent decades. The increase in the prevalence of asthma – paralleled by similar increases in other allergic disorders such as eczema and rhinitis – has been associated with an increase in atopic sensitisation. The prevalence of clinically diagnosed asthma ranges from 0.7% to 18.4% of the population in different countries2. Though the prevalence of asthma is generally low in Eastern Europe, in recent years, there has been an increase in the number of children with asthma. A Hungarian study from Budapest reported 2.26% in 1999 and 2.68% in 20033. Another study from a different part of Hungary (Baranya County) in 2006 found that 6.7% of the 6-14 year olds are suffering from clinically diagnosed asthma4. In early childhood it’s more common in boys, but during puberty (between 11 and 16 years), a gender shift in asthma prevalence occurs, and the prevalence is higher in female than male subjects at 16 years of age5.
The study group consisted of 49 children and adolescents treated for asthma at the Division of Pulmonology, Department of Pediatrics, Medical and Health Science Center, University of Debrecen. The 30 boys and 19 girls mean age was 9.02 years, ranged from 4- 17 years. Informed written consent was obtained from the caretakers of the participants. The oral and the dental survey were taken without knowing the severity of the underlying disease, the type and duration of the medication. The survey followed the World Health Organization (WHO) guidelines on dental caries assessment14. Indices were recorded for dental caries by the decayed, missing, filled surfaces (dmf-s/DMF-S) and dental plaque (Silness-Löe Plaque Index15). The dental status was taken with the help of the dental mirror and probe. Parents were asked to fill in a questionnaire referring to dietary and oral health habits. The patient’s general health data (severity of the disease, date of diagnosis and regularly taken asthma medication) were presented by the pediatrician after the oral examinations. To differentiate asthmatic children three variables were used: (1) severity of asthma on the initial assessment of a patient, (2) type of the medication, and (3) the duration of asthma treatment. The inhaled asthma medications used in our patient group were:
The duration of medication in the study group ranged 1 to 10 years, with a mean 3.59 yrs. The mean dmf-s was 5.51, while the DMF-S was 2.36. The main determining component was the number of the decayed surfaces (d-s, D-S). In case of primary teeth it was 5.43 (SD±7.95), ranging from 0-25. In relation to the permanent teeth the mean decayed surface was 1.61 (SD±2.43) ranging from 0-9. The PI was 0.99 (SD±0.47). Gender, severity of the asthmatic symptoms and the number of daily tooth brushings had no significant effect on the caries and plaque indices. Significant correlation was found between the amount of decayed permanent tooth surfaces (D-S) and the type of the asthma medication (p=0.023, Figure 1). Children receiving both inhaled corticosteroids and long-acting ß2-agonist had significantly higher PI (p=0.001) and more D-S than those who received only inhaled corticosteroids (Figures 2, 3). The duration of the asthma medication had a significant effect on decayed permanent tooth surfaces after 3 years (p=0.003). Inhaled dry power medication caused significantly higher plaque and caries indices especially in the mixed and permanent dentition than the pMDI aerosols (p=0.001 and p<0.001, Figures 4, 5). Regular intake of carbohydrate containing drinks influenced the number of decayed primary tooth surfaces, while snacking significantly influenced the number of the decayed permanent tooth surfaces (p=0.033, Figures 6, 7). In case of the primary dentition significantly lower plaque indices were found than in the mixed or permanent dentitions (p=0.025, Figure 8). The correlation between PI and D-S was significant on population level (p<0.001).
Inhalative corticosteroids (budesonide, fluticasone, ciclesonide) are the most effective controller therapy, and are therefore suggested treatment for asthmatic children of all ages. They improve clinical symptoms, lung function and quality of life, and reduce the frequency of acute exacerbations and the number of hospital admissions16. If asthma is not controlled with low (100-200/μg) or medium (200-400/μg) daily doses and proper administration of inhaled corticosteroids alone, a combination of a long-acting ß2-agonist should be considered. Rapid-acting (formoterol) and long-acting (salmeterol) ß2-agonists are highly effective bronchodilators, and they should be used only in combination17. Although they are well tolerated in children, even after long-term use, systemic and oral side effects can occur18. A number of studies have shown that asthmatic children have higher caries rate than healthy subjects13,19,20, while other studies stated that there is no significant difference between asthmatic and non-asthmatic children21-23. Matthews after reviewing 18 scientific articles in this field suggests that asthma doubles the risk of caries in both primary and permanent dentition13. The increased risk of caries is associated with the decreased salivary flow especially caused by the long-acting ß2-adrenergic agonists24. Kargul et al found that the pH of the oral cavity decreased below 5.5 half an hour after the use of an asthma-inhaler25. In DPI formulations micron-size active ingredients are mixed with larger carrier particles, excipients. Excipients are used to enhance the physical and chemical stability of the active pharmaceutical ingredient, its mechanical and/or pharmaceutical properties, such as dissolution and permeation. Excipients provide bulk, which improves handling, dispensing and metering of the drug, furthermore mask the original, unpleasant taste of the drug26. Currently, lactose is the more commonly used excipient. DPIs are containing 12.5-25 mg lactose/dose. Other, less common alternatives are mannitol and glucose27,28. Lactose, though it’s considered less cariogenic than glucose, is rapidly fermented by streptococci, including Streptococcus mutans and may cause a decrease in the oral pH29. The low pH value together with the reduced salivary flow makes asthmatic children more susceptible to dental caries30. Ryberg et al concluded after their 4-year follow-up study that asthmatic patients treated with beta 2-adrenoceptor agonists have increased caries susceptibility due to an impaired saliva secretion caused by the anti-asthma medication31.





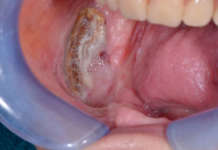



[…] stomatologica, ma a differente base eziologica. È infatti un dato comune nelle diverse forme di candidosi, e anche in tali casi l’odore sarà caratteristico. Nella maggior parte dei casi la diagnosi […]