Sedation in dentistry: definition and recommendations for clinical use of intravenous sedation
Dopo un rapido inquadramento delle tecniche sedative utilizzate in odontoiatria viene trattata la sedazione e.v., moderata e profonda, tecnica di grandissima utilità in un gran numero di prestazioni sia diagnostiche che chirurgiche, che deve tuttavia essere inquadrata con la stessa dignità di ogni altra prestazione anestesiologica, richiedendo un rispetto totale degli usuali livelli di sicurezza.
Riassunto
Molte procedure odontoiatriche possono essere effettuate con la sola anestesia locale; in alcuni casi può essere utile associare all’anestesia locale la somministrazione di farmaci per ottenere ansiolisi. Il livello di sedazione richiesto deve essere adeguato individualmente per ottenere un giusto equilibrio fra le esigenze del paziente, dell’operatore e la sicurezza della procedura. In questo contributo è trattata la tecnica sedativa e.v. dopo un rapido ma indispensabile inquadramento delle tecniche sedative utilizzate in odontoiatria.
Summary
Many dental procedures can be performed with local anesthesia.To improve the operating conditions of certain clinical situation it can be useful to associate local anesthesia with the administration of drugs to achieve anxiolysis. The level of sedation required must be adjusted individually to achieve the right balance between the patient and the operator needs and the safety of the procedure.In this paper we will discuss the technical sedative i.v. after a quick but necessary introduction to sedative techniques used in dentistry.

È specialista in Anestesiologia e rianimazione e responsabile del Servizio di Anestesiologia dell’Istituto Stomatologico Italiano di Milano. Si occupa da oltre 15 anni di anestesia in chirurgia maxillo facciale e in odontoiatria.In precedenza è stato primario del Servizio di Anestesia e terapia intensiva cardio-toraco-vascolare dell’Ospedale San Raffaele di Milano e del Servizio di Anestesia e rianimazione dell’Ospedale San Giuseppe di Milano. Autore di oltre 100 pubblicazioni scientifiche su riviste nazionali e internazionali, è stato professore a contratto presso la Scuola di specializzazione in Anestesia e rianimazione dell’Università degli Studi di Milano dal 1988 al 2007.

Laureato in Medicina e chirurgia e specializzato in Odontoiatria e in Chirurgia maxillo-facciale, si è perfezionato in Ortodonzia intercettiva nel 1994 e in Ortodonzia pre e post-chirurgica presso l’Università di Parma nel 1995. Ha frequentato corsi di formazione presso l’Università di Gotenburg nel 1995 e Umea nel 1997, dedicandosi in maniera particolare alle problematiche chirugiche dei soggetti in crescita.
È direttore del Dipartimento di Odontoiatria materno-infantile dell’Istituto Stomaltologico di Milano. È nel comitato scientifico de Il Dentista Moderno dal 1995. È vice-presidente della Società Italiana di Odontoiatria Infantile ed editor in chief dell’European Journal of Paediatric Dentistry.

Laureata in Odontoiatria e protesi dentaria nel 1991 presso l’Università Cattolica del Sacro Cuore di Roma, è specialista in Ortognatodonzia.Dal 2002 dirigente medico I livello presso l’UO di Odontoiatria e dal 2012 responsabile della SSD di Odontostomatologia dell’Ospedale Pediatrico Bambino Gesù di Roma. Dal 2009 referente JCI (Joint Commision International) per il reparto di Odontoiatria. Professore a contratto dal 1996 al 2004 di Cefalometria clinica e dal 2004 al 2006 di Ortognatodonzia nella Scuola di specializzazione di Ortognatodonzia dell’UCSC. Dal 2012 è libera docente presso la Scuola di Ortognatodonzia dell’Università degli Studi di Napoli Federico II.

Laureato in Medicina e chirurgia nel 1970 presso l’Università Cattolica del Sacro Cuore di Roma, si è specializzato in Anestesiologia e rianimazione nel 1973 presso l’Università degli Studi La Sapienza. Dal 2013 dirige il Dipartimento DEA ARCO dell’Ospedale Pediatrico Bambino Gesù di Roma. È professore a contratto di Anestesia pediatrica e neonatale presso la Scuola di specializzazione in Anestesiologia e rianimazione dell’Università Campus BioMedico di Roma. Dal 2012 è coordinatore del Gruppo di lavoro sul trasporto pediatrico della Società Italiana di Medicina di Emergenza e Urgenza pediatrica.

Laureato in Odontoiatria e protesi dentaria nel 1990 e dottore di ricerca nel 1995 in Biotecnologie dei materiali dentari.
È professore a contratto di Odontoiatria pediatrica presso l’Università degli Studi di Napoli Federico II e l’Università degli Studi de l’Aquila. Incaricato del Servizio di Odontoiatria pediatrica in sala operatoria presso l’Azienda Ospedaliera Universitaria Federico II di Napoli. Membro del Consiglio direttivo della Società Italiana di Odontoiatria Infantile. Associate editor dell’European Journal of Paediatric Dentistry. Segretario nazionale dell’Accademia Italiana di Odontoiatria pediatrica.

Ricercatore confermato presso il Dipartimento di Scienze mediche, orali e biotecnologiche dell’Università G. D’Annunzio di Chieti-Pescara, dove dirige l’UO di Pedodonzia. È titolare della cattedra di Pedodonzia del Corso di laurea magistrale in Odontoiatria e protesi dentaria e del Corso di laurea in Igiene dentale e docente presso la Scuola di specializzazione in Ortognatodonzia del Dipartimento di Scienze mediche, orali e biotecnologiche dell’Università G. D’Annunzio di Chieti. Membro del Consiglio direttivo della SIOI (Società Italiana Odontoiatria Infantile). Responsabile scientifico della SIOS (Società Italiana Odontostomatologia dello Sport).
Nonostante molte procedure odontoiatriche possano essere effettuate con la sola anestesia locale o loco-regionale, in alcuni casi può essere utile associare alla anestesia locale oppure alla loco-regionale la somministrazione di farmaci per ottenere essenzialmente ansiolisi, allo scopo di migliorare le condizioni operatorie1. Il livello di sedazione richiesto è differente a seconda di diversi fattori, e deve essere adeguato individualmente per ottenere un giusto equilibrio fra esigenze del paziente, dell’operatore e la sicurezza della procedura. Alcuni farmaci dell’anestesia si prestano particolarmente a questa tecnica, e sono a buon punto nuovi farmaci con caratteristiche ancora più interessanti.In questo contributo tratteremo la tecnica sedativa e.v. dopo un rapido ma indispensabile inquadramento delle tecniche sedative utilizzate in odontoiatria.
Definizione di coscienza (e dei suoi vari gradi di alterazione)
Chi pratica l’anestesia e la sedazione non può non rimanere affascinato dal “potere” di agire, sia in maniera empatica che farmacologica, sulle emozioni, sulla memoria, sulla attenzione, su quella che nell’accezione più comune viene indicata come coscienza, dei suoi simili, e dalla possibilità di servirsi di questi suoi “poteri” per aiutarli in momenti particolarmente impegnativi della loro vita. Se poi volesse approfondire l’azione dei farmaci da impiegare, superando le pur indispensabili e utilissime nozioni di farmacocinetica e di farmacodinamica che sono alla base dell’utilizzo di questi farmaci e desidera scavare più nel profondo, potrebbe scoprire l’affascinante mondo, in continua evoluzione, della neurochimica e della neurobiologia molecolare.
La giunzione sinaptica
L’azione dei farmaci dell’anestesia, siano essi ipnotici (cioè induttori del sonno) che sedativi (cioè ansiolitici), avviene mediante l’interferenza a livello delle giunzioni sinaptiche del sistema nervoso centrale, occupando i recettori specifici dei neurotrasmettitori2 responsabili dell’attività cerebrale.
L’entità dell’azione di questi farmaci è dose-dipendente, in quanto l’entità dell’effetto dipende dal grado di occupazione di questi recettori.
Per meglio comprendere quanto appena detto è necessario approfondire alcuni concetti: innanzitutto cosa si intende per coscienza dal punto di vista della neurochimica e della neurobiologia molecolare, e quali sono i meccanismi farmacologici legati alla sua progressiva depressione, e inoltre attingere alle informazioni legate ai recentissimi (degli ultimi due decenni) sviluppi nello studio della neurotrasmissione a livello della corteccia cerebrale e delle strutture che ne attivano o che ne deprimono le molteplici funzioni3.
Fu il fisiologo tedesco Otto Loewi a dimostrare sperimentalmente, nel 1921, la natura chimica della neurotrasmissione, provando che i neuroni sono collegati fra di loro attraverso strutture dette giunzioni sinaptiche, e che a livello di queste strutture la comunicazione avviene tramite la liberazione, da parte del neurone precedente, di sostanze chimiche, che agiscono su recettori specifici presenti sul neurone successivo. Il primo neurotrasmettitore scoperto fu proprio l’acetilcolina, che, come si sa oggi, stimola, nei neuroni del tronco cerebrale, il sonno RapidEyeMovements (REM), durante il quale è presente l’attività onirica.
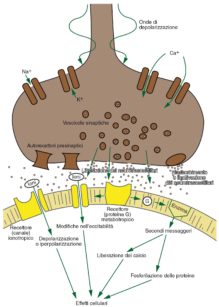
Nella figura 1 è rappresentato, in maniera molto schematica, il punto di contatto e di trasmissione tra il terminale di una cellula nervosa (parte superiore della figura) e la successiva (parte inferiore) lungo una via neuronale. Il segnale nervoso, arrivato come segnale elettrico fino al terminale della cellula precedente, provoca la liberazione di un neurotrasmettitore (contenuto e immagazzinato nelle vescicole visibili nel terminale) che fuoriesce nello spazio sinaptico e si fissa ai suoi specifici recettori presenti sulla superficie della cellula successiva, che, a sua volta, venendo stimolata, riprende la trasmissione elettrica del segnale fino alla ulteriore cellula successiva, e così via lungo tutta la via neuronale.
I neurotrasmettitori implicati nella neurochimica del sistema sonno-veglia sono tre:
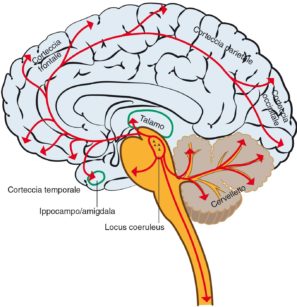
- noradrenalina: è sintetizzata a livello del locus ceruleus (LC), collocato nel ponte, e attiva una amplissima rete neuronale che si proietta su tutta la corteccia cerebrale (Figura 2). L’attività di tale rete è massima durante la veglia e la coscienza, diminuisce durante il sonno non rapid eye movements (NREM) ed è al suo minimo durante il sonno REM;
2. Sistema noradrenergico 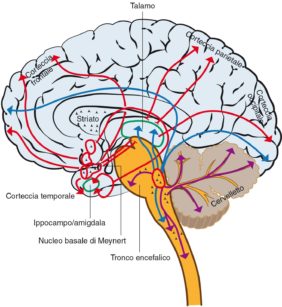
3. Sistema colinergico 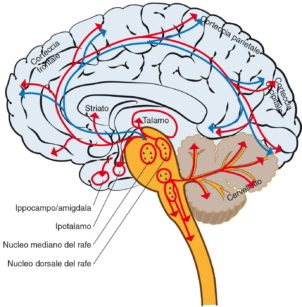
4. Sistema GABAergico - acetilcolina: è sintetizzata anch’essa a livello del ponte (Figura 3), e anch’essa attiva un’altra amplissima rete neuronale la cui attività è massima, come per la rete noradrenergica, durante la veglia e la coscienza, diminuisce durante il sonno non REM, ma, diversamente dalle due altre vie neuronali, è attiva durante il sonno REM, ed è quindi responsabile dell’attività onirica, tipica di questa fase del sonno;
- acido gamma-aminobutirrico (GABA): è sintetizzato a livello della sostanza reticolare ascendente (SRA), situata nel ponte cerebrale (Figura 4). Svolge un importante ruolo nel mantenimento dell’attivazione cerebrale, ed è il principale neurotrasmettitore inibitorio. La perdita di coscienza indotta dagli anestetici si associa ad alterazioni della concentrazione di GABA a livello della SRA, confermando così, per via indiretta, l’azione inibitoria svolta dal GABA sulla corteccia cerebrale, e fa supporre che esista una sede specifica, dal punto di vista neuroanatomico e neurochimico, in grado di svolgere un ruolo unico nel meccanismo della coscienza e della anestesia
Le reti neuronali
Il cervello contiene una gamma di reti neuronali di incredibile complessità, e ognuno dei circa 100 miliardi di neuroni che compongono un cervello umano è connesso con gli altri con messaggi il cui segnale cambia con una frequenza di circa 200 volte al secondo. Nella Figura 5 sono appunto indicate le reti neuronali più ricche dei neurotrasmettitori menzionati (noradrenalina, acetilcolina e GABA), e quindi coinvolte nell’attivazione della coscienza e del sonno nelle fasi REM e non REM. Sono indicate le variazioni dell’attività delle vie neuronali aventi come neurotrasmettitori la noradrenalina (in rosso), l’acetilcolina (verde) e l’acido gamma-aminobutirrico(blu), durante il ciclo sonno-veglia.
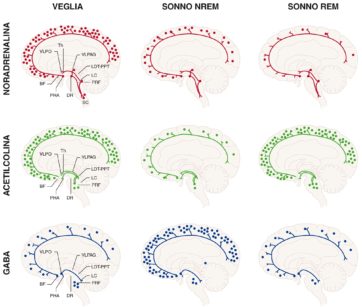
BF, basal forebrain (proencefalo); DR, dorsal raphe (rafe dorsale); LC, locus ceruleus; LDT-PPT, laterodorsal and pedunculopontine tegmentum (tegmento laterodorsale e peducolo pontino); PHA, posterior hypothalamic area (area ipotalamica posteriore); PRF, pontine reticular formation (formazione reticolare pontina); SC, spinal cord (midollo spinale); Th, thalamus (talamo); VLPAG, ventral periaqueductal gray (sostanza grigia periacqueduttale); VLPO, ventrolateral preoptic nucleus (nucleo preottico ventrolaterale) (modificata da: Brady S et al. Basic neurochemistry, Elsevier,Oxford, UK, 2012).
La densità dei punti ai terminali dei sistemi neuronali riflette le condizioni di maggiore o minore attivazionelegateall’attività dello specifico neurotrasmettitore. L’adrenalina ha un picco di attività durante la veglia, con un decremento durante il sonno non REM e il suo nadir durante il sonno REM. La trasmissione colinergica è invece associata con l’attivazione corticale durante la veglia e il sonno REM. Acetilcolina e GABA hanno una relazione inversa durante il ciclo sonno-veglia, data l’azione eccitatoria dell’acetilcolina e la neuromodulazione inibitoria del GABA (attività massima dei sistemi GABAergici durante il sonno senza sogni (NREM) e loro silenzio durante la veglia e il sonno con sogni (REM) L’attività del sistema GABAergico è quindi esattamente opposta a quella dell’acetilcolina.
Sito d’azione dei farmaci dell’anestesia
Alla fine degli anni novanta, in epoca quindi piuttosto recente – e vedremo in seguito perché proprio in quegli anni – si cominciò a ipotizzare che l’azione di soppressione della coscienza da parte dei farmaci anestetici avvenisse agendo sui nuclei sotto-corticali che controllano il ritmo sonno-veglia. Questi nuclei presenti nel tronco cerebrale e nell’ipotalamo, le parti dal punto di vista evolutivo più antiche dell’encefalo, tramite la liberazione di specifici neurotrasmettitori a livello di precise reti sinaptiche, controllano appunto tale ritmo. La condizione che comunemente indichiamo come coscienza è generata dalla sincronizzazione di una enorme rete neuronale, all’interno della quale i messaggi sono appunto mediati dai neurotrasmettitori, e che coinvolge tutte le strutture encefaliche. La condivisione dei circuiti da parte di sonno e anestesia suggerisce che i farmaci dell’anestesia esercitino i loro effetti agendo, a livello recettoriale, sulla rete neuronale avente come neurotrasmettitori i tre implicati nel controllo del ciclo sonno-veglia.
La coscienza
A questo punto, solo dopo questa ampia premessa, che ha condensato in poche righe le scoperte della neurochimica degli ultimi vent’ anni, è sufficientemente possibile definire dal punto di vista neurobiologico cosa si può intendere per coscienza e per il suo opposto, cioè la narcosi, e tentare di definire meglio le molteplici e sfaccettate alterazioni della coscienza indotte dai farmaci. Non c’è pertanto motivo di stupirsi se nel non lontano 1990 l’inglese Stuart Sutherland affermasse l’impossibilità di definire in maniera scientifica appunto il termine coscienza4. Ancora nell’anno 2000, nel trattato The new cognitive neuroscience, Christof Koch e Francis Crick (il premio Nobel 1962 per la medicina, scopritore insieme a Watson della doppia elica del DNA) concludevano: “un tentativo di precisa definizione della coscienza è ancora prematuro” e suggerivano (suggerimento rivelatosi più che giusto negli anni successivi): “l’approccio empirico più promettente è approfondire la scoperta delle correlazioni neuronali della coscienza”5. Una importante spinta alle ricerche in questa direzione fu la proclamazione della Decade of the Brain (1990–1999) da parte dell’allora presidente George H.W. Bush che mise a disposizione della Library of Congress e del National Institute of Mental Health risorse straordinarie “to enhance public awareness of the benefits to be derived from brain research”, allo scopo anche di incoraggiare un interscambio culturale sulle implicazioni etiche, filosofiche e umanistiche che stavano emergendo appunto dalle scoperte scaturite dagli studi neurobiologici e neurochimici. Il primo trattato esclusivamente dedicato a questo argomento (Neurochemistry of Consciousness: neurotransmitters in mind) uscì appunto nel 2002. Importanti argomenti a favore dell’importanza relativa di specifiche aree cerebrali (corteccia, tronco cerebrale, sistema reticolare ascendente, nuclei talamici) e delle vie neuronali attivate dagli specifici mediatori neuromodulatori vennero dalle immagini PET che evidenziarono aumenti di flusso cerebrale in alcune regioni e decremento in altre, con correlazioni significative con i dati dello studio dell’attivazione neuronale da parte degli specifici neurotrasmettitori e con gli studi neurofisiologici, con segnali EEG disincronizzazione e desincronizzazione nelle diverse fasi dell’attività corticale durante il sonno o la veglia.
È chiaro che questi pur enormi progressi nelle conoscenze della neurobiologia e della neurochimica sono ben lontani dallo spiegare le svariate sfaccettature della coscienza, dalla consapevolezza di se stessi all’attenzione, la memoria, la motivazione, il sonno, i sogni, la veglia. Le alterazioni indotte dai farmaci, tra cui quelli dell’anestesia, e quelle indotte dagli stati patologici aggiungono importanti linee di ricerca sui meccanismi associati al mantenimento oppure all’abolizione dei vari aspetti della coscienza (a puro titolo di esempio alcune benzodiazepine possono abolire la memoria pur mantenendo il paziente cosciente).
Alterazioni della coscienza farmacologicamente indotte
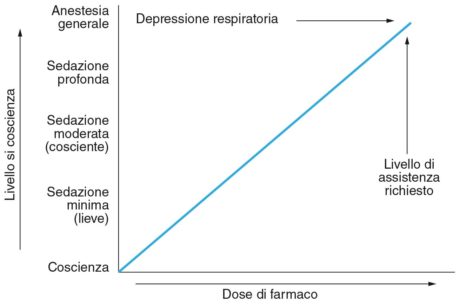
Dalla pienezza della coscienza alla sua perdita totale esiste un continuum di progressiva depressione dell’attenzione che è oggi possibile percorrere gradino per gradino utilizzando tutta una serie di farmaci. Come indicato nella Figura 6, definendo coscienza come l’associarsi della pienezza della vigilanza e della consapevolezza soggettiva di questa condizione, possiamo definire, all’estremo opposto, l’anestesia generale (e il suo sinonimo narcosi) come uno stato farmacologicamente indotto, temporaneo e totalmente reversibile, di perdita totale della coscienza, con soppressione di ogni tipo di sensibilità, allo scopo di eseguire interventi chirurgici. Lungo questo continuum i farmaci agiscono anche su altri aspetti della funzione del sistema nervoso centrale, come la memoria, il controllo della funzione cardiovascolare, respiratoria, ecc.
Utilizzando quindi i vari farmaci in grado di deprimere, con una relazione dose-effetto, il livello di coscienza, possiamo passare gradualmente, oppure in tempi molto rapidi, dalla condizione di un paziente perfettamente sveglio alla perdita totale della coscienza. Nella stessa Figura 6 è indicato come, di pari passo con la diminuzione progressiva del livello di attenzione, aumenta altresì progressivamente la depressione della funzione respiratoria, con necessità di un suo supporto esterno.
I vari livelli appartenenti a questo continuum, ben lontani dall’essere rigidamente separati nella loro attuazione clinica, nonostante la già citata relazione dose-effetto, possono essere raggiunti in maniera non pienamente prevedibile, e pertanto dalla pienezza della coscienza, e quindi dalla perfetta efficienza dell’attività respiratoria e dei riflessi protettivi delle vie aeree, si può passare in tempi anche rapidi, e non voluti, alla eccessiva depressione del livello di coscienza, e quindi alla perdita, totale o parziale, dei riflessi di protezione delle vie aeree e dell’efficienza della ventilazione (con conseguenti ipossia e ipercapnia).
Sedazione in odontoiatria: definizione e raccomandazione all’uso clinico
Rifacendoci alla Figura 6 possiamo, come prima grossolana definizione, individuare come sedazione un livello intermedio di depressione della coscienza senza interferenze con l’autonomia respiratoria.
Possiamo però dare una definizione clinica più precisa e, avendo approfondito le basi neurochimiche, una definizione neurochimica.
Definizione clinica
La American Society of Anesthesiology (ASA) definisce tre livelli di sedazione6, basati sulla “reattività” dei pazienti:
- sedazione minima (o lieve): il paziente ha un buon livello di ansiolisi, ma è perfettamente responsivo e collaborante e ha perfetta efficienza sia dell’attività respiratoria che dei riflessi di protezione delle vie aeree;
- sedazione moderata (cosciente): il paziente è più sedato, e quindi ha una riduzione del livello di vigilanza, ma risponde in maniera adeguata agli stimoli tattili o verbali. La ventilazione spontanea è usualmente adeguata, i riflessi di protezione delle vie aeree sono mantenuti e quindi non sono richiesti interventi per mantenerne l’efficienza e la pervietà;
- sedazione profonda: il paziente non è più vigile, può rispondere in maniera adeguata solo a stimoli ripetuti o dolorosi e può richiedere un certo grado di assistenza per mantenere una adeguata ventilazione e/o la pervietà delle vie aeree.
In riferimento alle diverse tecniche sedative utilizzabili in ambito odontoiatrico riteniamo si debba distinguere nettamente la sedazione RA Sec. Langa (basse % di N2O e alte di O2), la cui sicurezza è garantita dalle sedation-machines (e dove il paziente può essere dimesso dopo 15-20 minuti) e che è una sedazione lieve, dalla sedazione moderata ottenibile con farmaci e.v. la cui sicurezza dipende oltre che dalla buona professionalità dell’operatore e del team anche dalla maneggevolezza del farmaco utilizzato e dalla sua capacità o meno che ha lo stesso come vedremo di interferire con i riflessi tutelari del paziente (Figura 7).
La sedazione enterale usata in dose singola non superiore alla dose massima consigliabile è anch’essa sicura, anche se necessita di accompagnamento post-operatorio del paziente che può essere dimesso dopo 30 minuti e viene definita nelle classificazioni analizzate, in particolare quella dell’American Association of Dentistry e dall’American Society of Anestesiologist (ASA), come sedazione lieve.
Si ritiene che in un uso ambulatoriale la tecnica sedativa prescelta debba garantire il mantenimento dei riflessi tutelari del paziente per poter essere eseguita con la necessaria sicurezza. La possibilità che vengano meno in maniera predicibile i riflessi tutelari di tosse e deglutizione deve imporre la presenza di personale specializzato e di un ambiente protetto e questa è la situazione che si verifica nella sedazione moderata per via parenterale e nella sedazione profonda.
Ciò premesso si ritiene che, rimanendo nell’ambito della sedazione lieve, non sia necessario un ambiente operatorio apposito. In buona sostanza possono essere considerate sicuramente sedazioni lievi quella ottenuta con N2O/O2 e la sedazione con benzodiazepine per via enterale in un’unica dose che non superi la dose massima consigliata per il paziente che si sta trattando. Si ritiene invece che le forme di sedazione per e.v., siano esse moderate o profonde, possano determinare una perdita di coscienza del paziente con perdita dei riflessi e richiedano quindi servizi di supporto da parte di personale specialistico che si dedichi alla sicurezza extra-odontoiatrica del paziente.
Si ritiene che la sedazione moderata parenterale Vs l’anestesia generale siano un continuum e non sempre sia possibile prevedere come ogni paziente risponderà alla somministrazione dei farmaci. Per tale motivo l’operatore che somministra un livello di sedazione deve essere in grado di gestire la sicurezza e trattare le complicanze dei pazienti anche del livello successivo.
Per tutti i livelli di sedazione l’operatore deve avere training, abilità, capacità di utilizzare farmaci e attrezzature per identificare precocemente e trattare eventuali emergenze sino all’arrivo di soccorsi o sino a quando il paziente non ritorna al livello programmato di sedazione senza complicazioni cardiovascolari o respiratorie.
Per i nostri scopi potremmo distinguere, come previsto dall’American Accademy of Pediatric Dentistry, dall’American Dental Association e dall’American Society of Anestesiologist 4 diversi livelli di sedazione/anestesia che richiedono differenti livelli di competenza del team e di caratteristiche dell’ambiente operatorio.
Per quanto riguarda la Classificazione ASA si ritiene che la classe 1 sia trattabile in ambulatorio, la classe 2 deve essere valutata caso per caso e necessita spesso di una sedazione per ridurre il rischio operatorio, mentre la classe 3 necessiti di ambiente protetto indipendentemente dal tipo o meno di sedazione utilizzata.
Possiamo, in base a quanto sinora specificato, individuare 4 livelli clinico-operativi che attengono gli aspetti clinici raggiunti e non quelli prevedibili con la somministrazione anche combinata di farmaci ad azione non solo sedativa “pura” ma analgesica maggiore o addirittura propriamente anestetica. Queste ultime classi di farmaci, per possibili variazioni individuali dose-effetto, possono fare variare molto rapidamente il livello di sedazione raggiunto lungo un continuum che può condurre fino all’anestesia generale. Gli standard organizzativi proposti dovranno quindi tenere conto di tutti questi elementi per agire in sicurezza.
1. Sedazione lieve – Livello ambulatoriale
È uno stato di alterata coscienza in cui il paziente è in grado di rispondere a ordini semplici e di mantenere i riflessi tutelari spontaneamente. La funzione respiratoria e cardiocircolatoria è nella norma. Il paziente ha un buon livello di ansiolisi ma è perfettamente rilassato e collaborante. Nel nostro campo è in genere sinonimo della sedazione con protossido d’azoto a basse percentuali e alte di ossigeno; non richiede particolari attenzioni e può essere eseguita dal dentista che lavora da solo in ambito ambulatoriale.
Altra via per questa forma di sedazione in odontoiatria è a via enterale con l’utilizzo di farmaci in una dose singola che non superi la dose massima raccomandata.
Si ritiene non necessario ma comunque consigliabile il monitoraggio tramite pulsi-ossimetro in questa forma di sedazione anche in relazione al tipo di terapia da praticare; noi usiamo il pulsiossimetro in tutte le terapie chirurgiche al di là della necessità di sedare il paziente ( http://www.aisod.info/miscellanea/).
2. Sedazione moderata – Livello ambulatoriale Vs Ambiente protetto
È uno stato di alterata coscienza durante il quale il paziente risponde a comandi verbali semplici in maniera appropriata ed è in grado di mantenere la pervietà delle vie respiratorie spontaneamente. Le funzioni respiratoria e cardiocircolatoria sono usualmente nella norma.
Questa tecnica prevede normalmente l’impiego di dosi titolate di un solo farmaco, abitualmente una benzodiazepina. In particolari circostanze si può ricorrere a iniezioni continue e ripetute o a infusione continua del farmaco. Quest’ultima procedura deve essere utilizzata da anestesisti e/o sedazionisti esperti che operino in un ambiente protetto (http://www.aisod.info/miscellanea/). La via di somministrazione dei farmaci è quella parenterale. Se il paziente non è in grado di mantenere aperta la bocca spontaneamente deve essere considerato in sedazione profonda (http://www.aapd.org/media/Policies_Guidelines/G_Sedation.pdf).
3. Sedazione profonda – Ambiente protetto
È uno stato di alterata coscienza durante il quale il paziente non risponde a comandi verbali semplici o a stimoli dolorosi in maniera appropriata. La possibilità di mantenere la pervietà delle vie respiratorie spontaneamente può essere alterata e quindi il paziente può necessitare di assistenza respiratoria. Le funzioni cardiovascolari sono generalmente mantenute. Questo stato è accompagnato da perdita parziale o totale dei riflessi protettivi.
La via di somministrazione dei farmaci è normalmente quella parenterale. L’ambiente operatorio deve essere protetto ed è richiesta la presenza di un anestesista.
4. Anestesia generale – Ambiente operatorio dedicato
È uno stato in cui la coscienza del paziente viene persa. Il paziente è insensibile agli stimoli dolorosi. La sua capacità di mantenere la funzione respiratoria è alterata. Normalmente il paziente è assistito da appositi macchinari per assicurare una corretta ventilazione. La funzionalità cardiovascolare può essere deficitaria.
Necessita di ambienti e operatori dedicati.
Definizione neurochimica
L’intensità dell’effetto clinico dei farmaci utilizzati per la sedazione è correlata al grado di occupazione (percentuale di fissazione) dei recettori coinvolti nel ciclo sonno-veglia, e quindi al grado di inibizione delle reti neuronali aventi come neurotrasmettitori noradrenalina, acetilcolina e GABA:
- effetto ansiolitico: percentuale attorno al 20%;
- effetto sedativo e amnesizzante: percentuale tra il 30 e il 50%;
- effetto ipnotico: valori superiori al 60%.
Come già sottolineato ci occuperemo in questo contributo di analizzare i problemi connessi con la pratica della sedazione e.v. moderata o profonda lasciando ad altri lavori l’analisi della sedazione lieve. Per una serie di motivi. che di seguito approfondiremo, infatti durante la sedazione da moderata a profonda di un paziente non è possibile in realtà rimanere perfettamente stabili sul livello di sedazione considerato ottimale, ma si ha un continuo oscillare attorno a questo livello, con fasi di alleggerimento del livello di sedazione e fasi di approfondimento.
Quali sono i motivi di questa difficoltà e quali sono le ricadute in termini di sicurezza della procedura di sedazione per via e.v.?
1. Grande variabilità della risposta individuale ai farmaci utilizzati nella sedazione endovenosa
Nella maggior parte delle specialità mediche i farmaci possono essere somministrati a dosi molto standardizzate, e sono a queste dosi efficaci, senza essere tossici, nella maggioranza dei pazienti. In anestesia le cose vanno diversamene, in quanto la gamma delle dosi è decisamente più ampia, avendo ogni farmaco dell’anestesia una finestra terapeutica differente, a seconda, tra l’altro, dell’entità del risultato che si vuole ottenere. È d’altronde intuibile che mentre normalmente i farmaci hanno un bersaglio unico e ben preciso, i farmaci dell’anestesia vanno a colpire una rete di intercomunicazione neuronale estremamente complessa e che non può che essere peculiare del singolo individuo.
Nella Tabella 1 sono riportati i dosaggi dei farmaci normalmente utilizzati per la sedazione endovenosa; è possibile notare che il range delle dosi raccomandate è estremamente ampio e prevede una variabilità rispetto alla dose minima del doppio (ad es. diazepam), del triplo (ad es. midazolam) o addirittura del quadruplo (propofol).
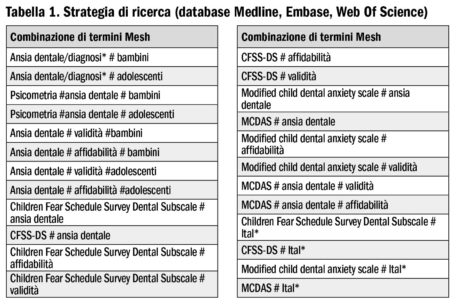
Una sedazione, come anche una anestesia generale, è tanto più profonda quanto sono più alte sono le dosi somministrate, ma a parità di dosi la stessa profondità non è ottenuta in tutti i singoli pazienti, a seconda non solo della loro età, peso, patologie associate, farmaci utilizzati, ecc. In realtà la risposta individuale ai farmaci della sedazione è talmente differente nei singoli pazienti da rendere assolutamente non affidabile e intrinsecamente insicura una somministrazione basata esclusivamente sul tradizionale dosaggio in base al peso.
In effetti la grande variabilità interindividuale nella risposta ai farmaci è uno dei principali inconvenienti della metodica della sedazione cosciente per via endovenosa; ciò impone una attenta modalità di somministrazione dei farmaci stessi e un continuo monitoraggio dei parametri emodinamici e respiratori, e la possibilità di una immediata assistenza respiratoria.
2. Impossibilità di reale monitoraggio della profondità della sedazione
L’intensità dell’effetto clinico dei farmaci utilizzati per la sedazione endovenosa è correlata con il grado di occupazione dei recettori, e quindi è strettamente dipendente dai livelli plasmatici di farmaco ottenuti con la dose somministrata. Non è purtroppo possibile, al momento, sia con l’osservazione clinica che con quella strumentale, monitorare in maniera attendibile il livello di occupazione recettoriale, unico modo certo per valutare il piano anestesiologico. L’osservazione clinica è utile ma assolutamente empirica, e i dati strumentali non sufficientemente precisi. Anche il monitoraggio dei parametri neurofisiologici (elettroencefalogramma, analisi bispettrale, entropia, potenziali evocati), molto promettente per il futuro, al momento, come risultato in numerosi trials, non è considerato sufficientemente affidabile per questo aspetto della pratica anestesiologica. L’indice bispettrale (BIS)8, 9, l’unico sistema di monitoraggio neurofisiologico effettivamente utilizzato in clinica, considerato particolarmente utile per evitare i problemi di risveglio in corso di anestesia 10,11 (Figura 8), non si è rivelato sufficientemente sensibile e discriminante in corso di sedazione, pur esistendo sicuramente una relazione assolutamente valida fra l’indice indicato dallo strumento e il grado di depressione della coscienza.
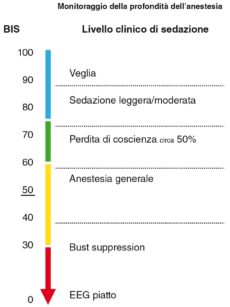
Perché un parametro neurofisiologico possa diventare veramente un metodo routinario di sorveglianza del livello di coscienza durante una sedazione è necessario che esso venga espresso in termini di valori quantitativi in tempo reale, che dei valori soglia ben definiti e fortemente correlati al livello clinico di anestesia vengano descritti e validati dalla letteratura, che essi siano riproducibili nelle varie categorie di pazienti e di contesti chirurgici, e che quindi permettano di creare protocolli di anestesia affidabili. Inoltre le modificazioni del segnale neurofisiologico devono essere soprattutto sensibili e discriminanti nella gamma di concentrazioni dei farmaci abitualmente utilizzati in clinica, e il segnale deve variare in maniera specifica con il livello di anestesia, cioè non deve risentire di artefatti legati a fattori esterni. Nonostante tutta questa serie di ostacoli ancora da affrontare, le aspettative per il futuro sono grandi, tant’è vero che già si parla di closed loop anesthetic delivery systems (CLAD), cioè di sistemi di somministrazione dei farmaci anestetici automatizzati e pilotati da una rilevazione certa dell’attività cerebrale. Questi sistemi, utilizzando un parametro neurofisiologico del livello di depressione dello stato di coscienza, potranno pilotare la somministrazione automatica del farmaco anestetico, modificandola in continuazione, basandosi sulla differenza fra il livello di depressione del livello di coscienza impostato come obiettivo e l’analisi computerizzata del segnale attuale.
Farmaci della sedazione
L’introduzione del thiopental (Pentothal) nella pratica clinica, nell’anno 1934, ha segnato l’inizio della moderna anestesia endovenosa12. Oggi gli anestetici endovenosi sono utilizzati sia per l’induzione e il mantenimento dell’anestesia generale sia appunto per la sedazione endovenosa, in una larga gamma di circostanze.
Il farmaco ideale per l’utilizzo per una sedazione per via endovenosa dovrebbe possedere una serie di caratteristiche specifiche:
- rapidità nell’inizio dell’azione;
- relazione dose-effetto lineare e ben prevedibile nelle diverse classi di pazienti;
- breve emivita (rapido risveglio alla sospensione);
- minimi effetti eccitatori;
- minimi effetti di depressione respiratoria e cardiaca.
Propofol
L’anestetico endovenoso più comunemente usato in anestesia è il propofol (Diprivan). Questo farmaco permette una rapida induzione e un rapido risveglio; l’emivita di eliminazione è di circa 10 minuti dopo un’infusione di durata non superiore alle 3 ore. Il suo meccanismo d’azione è legato alla sua attività sui recettori del GABA, di cui abbiamo visto prima la potente azione inibitoria sulla corteccia cerebrale. Dopo la somministrazione di una dose ipnoinducente di propofol si verifica un’apnea incirca il 25% – 30% dei pazienti, di incidenza e durata variabile a seconda della dose somministrata, della velocità di iniezione e di una eventuale premedicazione. A causa della larga finestra del dosaggio (Tabella 1), nel caso lo si utilizzi per una sedazione necessita di una somministrazione particolarmente attenta alla risposta del paziente per rimanere nell’ambito della depressione della coscienza desiderata.
Benzodiazepine
Le benzodiazepine sono particolarmente utilizzate per la sedazione cosciente, essendo caratterizzate da proprietà ansiolitiche, sedative, amnesizzanti, anticonvulsivanti e miorilassanti. Anch’esse agiscono selettivamente a livello dei recettori del GABA, e quindi svolgono un effetto inibitorio sull’attività della corteccia cerebrale (Figura 5).
Le differenze nei loro effetti clinici sono legate anche al differente grado di affinità delle diverse molecole rispetto ai recettori GABAergici. Le sottounità alfa di questo recettore giocano un ruolo importante nell’azione delle benzodiazepine, e le loro caratteristiche farmacologiche ne vengono modificate in termini di effetti clinici e di effetti indesiderati.
La sedazione, l’amnesia anterograda e le proprietà anticonvulsivanti sono soprattutto mediate dalle sottounità alfa uno del recettore GABA, mentre l’ansiolisi e il rilasciamento muscolare sono mediate soprattutto dalle unità alfa due. Come tutti gli anestetici endovenosi producono una depressione, a livello centrale, dell’attività respiratoria, correlata con la dose somministrata.
La loro biodisponibilità a livello dei siti di azione recettoriale è legata al tasso di albuminemia plasmatico (infatti solo la quota non legata all’albumina, e quindi libera nel plasma, può agire sul bersaglio d’azione, cioè sui recettori); sono metabolizzate dai microsomi epatici ed eliminate in seguito per via renale. Il maggior inconveniente anche di queste molecole rimane la grande variabilità della risposta interindividuale, condizionante una somministrazione, un monitoraggio e la disponibilità immediata della possibilità di assistenza respiratoria durante il loro utilizzo.
Svolgono un’ottima attività ansiolitica ed evitano il ricordo di eventi spiacevoli durante le procedure chirurgiche minori; è naturalmente indispensabile una altrettanto valida anestesia locale o loco-regionale. Durante una sedazione cosciente permettono di avere un paziente sostanzialmente tranquillo, collaborante e orientato, e che rimarrà amnesico, per quanto si riferisce alla procedura eseguita 11.
Per questo scopo è necessaria una attenta somministrazione continua, allo scopo di mantenere la sedazione nell’ambito della profondità desiderata. L’inizio dell’azione è rapido con il midazolam, raggiungendo usualmente l’effetto desiderato in circa due-tre minuti dall’inizio dell’infusione.
La possibilità di ottenere, con una ben monitorata somministrazione, un livello di sedazione relativamente stabile, con il mantenimento di una funzione respiratoria spontanea soddisfacente, e di ottenere altresì una efficace amnesia, rendono attualmente il midazolam il farmaco più usato nella sedazione cosciente.
Le benzodiazepine effettivamente utilizzate in anestesia sono sostanzialmente due: midazolam (Ipnovel), e diazepam (Valium) e in base alla loro durata d’azione vengono classificate come:
- a breve durata di azione(midazolam);
- a lunga durata di azione (diazepam).
Il diazepam fu la prima benzodiazepina utilizzata per la sedazione cosciente, caratterizzato però da un’emivita molto lunga, da una elevatissima variabilità della risposta individuale, dalla frequenza di reazioni paradosse (confusione, agitazione, aggressività, più frequentemente osservate nel bambino iperattivo, nell’anziano e nei pazienti già in terapia cronica con questi farmaci). Un’ altra caratteristica negativa è la capacità di provocare irritazione della parete venosa con possibilità di tromboflebiti, problema correlato alla sua insolubilità in acqua.
Il midazolam, commercializzato in Italia per uso esclusivamente ospedaliero, di introduzione più recente, ha totalmente sostituito il diazepam nella sedazione cosciente, sia per il suo più rapido inizio d’azione dopo bolo, sia per la sua maggiore potenza in termini di ansiolisi, amnesia, sedazione, sia per la sua emivita più breve, che ne permette una più rapida eliminazione, se paragonata ad altre benzodiazepine 13. Se confrontato però con quello del propofol e dei barbiturici, il tempo d’inizio del midazolam è più lento, e la sua eliminazione, specialmente dopo dosi elevate o una infusione prolungata, è considerevolmente più lunga.
Il remimazolam, ancora nella fase sperimentale del suo sviluppo, è la più recente delle benzodiazepine. La sua durata d’azione molto breve, grazie alla sua rapida eliminazione da parte delle esterasi plasmatiche ne fa una molecola di sicuro grande interesse per il futuro.
Altri farmaci utilizzati nella sedazione
Remifentanil (Ultiva) analgesico morfinico.
Flumazenil (Anexate), antagonista specifico delle benzodiazepine.
Naloxone (Narcan), antagonista dei morfinici.
Peculiarità della sedazione in odontoiatria
L’intervento odontoiatrico ha come sede il primo tratto delle vie aeree e quindi impedisce una pronta assistenza dell’attività respiratoria da parte dell’anestesista. Ciò impone una ancor più attenta calibrazione del livello di sedazione e una scelta particolarmente medittata dei farmaci utilizzati e del loro dosaggio.
Scelta dei farmaci
La scelta dei farmaci da utilizzare per una buona riuscita di una sedazione deve tener conto di:
- tipo di intervento;
- capacità dell’operatore nel praticare una efficace anestesia locale;
- caratteristiche del singolo paziente e sue aspettative.
È da tener ben presente che la scelta e la dose totale somministrata sono influenzate grandemente dalla possibilità di avere con il paziente un approccio corretto in ogni momento della procedura, sia in fase preoperatoria ascoltando le sue aspettative e spiegando quello che accadrà, sia nei momenti che precedono la sedazione farmacologica vera e propria13.
Midazolam. Produce ansiolisi e un livello di sedazione dose correlato. Produce inoltre una marcata amnesia anterograda. È largamente preferito alle altre benzodiazepine sia perché, per la sua idrosolubilità, non causa irritazione della parete venosa, sia per la sua relativamente breve emivita di circa 2–4 ore, sia per la sua rapidità di azione. È da tener presente che la risposta individuale è altamente variabile.
Propofol. È essenzialmente un eccellente ipnotico; le sue proprietà farmacocinetiche consentono un rapido risveglio sia dopo un bolo singolo che dopo una perfusione continua. È privo di qualunque attività analgesica e produce solo una moderata amnesia 13; anche a dosi sedative può rapidamente provocare apnea ancor prima della perdita di coscienza, e presenta il rischio costante di passaggio non intenzionale a condizioni di anestesia generale 15.
Modalità di somministrazione
Ansiolisi, ipnosi, amnesia e analgesia devono essere combinate fra di loro per “confezionare” una sedazione che ben si adatti al tipo di procedura, al paziente e all’operatore; questo obiettivo è reso ancor più difficile da raggiungere a causa della già vista grande variabilità della risposta individuale a questo tipo di farmaci.
È quindi necessaria una loro somministrazione accurata, ben dosata e stabilmente continua; si rende pertanto indispensabile l’utilizzo degli appositi dispositivi per l’infusione (pompe siringa).
Conclusioni
All’atto pratico, quali considerazioni possiamo trarre da tutta questa serie di dati?
La considerazione fondamentale è che la sedazione cosciente endovenosa è sicuramente una tecnica di grandissima utilità in un gran numero di prestazioni sia diagnostiche che chirurgiche, utilizzabile sia nella tradizionale sala operatoria sia in sedi alternative adeguatamente attrezzate.
Deve però essere inquadrata con la stessa dignità di ogni altra prestazione anestesiologica, richiedendo quindi un rispetto totale degli usuali livelli di sicurezza.
Sfortunatamente un’opinione largamente diffusa tra i medici e i pazienti è che la sedazione debba essere considerata una tecnica intrinsecamente più sicura rispetto all’anestesia generale14. In realtà il database dell’ASA relativo ai risarcimenti accordati in via definitiva dalle compagnie di assicurazione (Closed Claims Database) ha indicato che i rischi di morte o di danno cerebrale permanente nella sedazione cosciente per via endovenosa sono simili a quelli dell’anestesia generale. Nella citata rewiew dell’ASA si sottolinea che, probabilmente, il maggiore rischio di danno debba essere collegato alla depressione respiratoria dei farmaci della sedazione endovenosa, e che molti casi avversi sarebbero stati evitati con un miglior monitoraggio e una più attenta vigilanza 16.
Ne consegue quindi che lo standard di cura dei pazienti sottoposti a sedazione endovenosa debba essere il medesimo di quello disponibile e utilizzato per i pazienti sottoposti ad anestesia generale, e comprendere quindi tutti gli aspetti del monitoraggio e dell’assistenza cardiovascolare e respiratoria della comune pratica anestesiologica 17.
Corrispondenza
Luigi Paglia
luigipaglia@hotmail.com
Bibliografia
- Raeder J, Mulroy M, White P.Perioperative care for the outpatient undergoing ambulatory surgery. Anesth Analg 2009; 108:704-709.
- Lajtha A, Descarries L, Mechawar M. Neurotransmitters Systems. Handbook of Neurochemistry and Molecular Neurobiology 2008; 5:1-20.
- Stenberg D. Neuroanatomy and neurochemistry of sleep. Cell.Mol.LifeSci 2007; 64:1187-1204.
- Perry E, Ashton H, Young A. Advances in consciousness research. Neurochemistry of consciousness: neurotransmitters in mind 2002; 36:12-16.
- Koch C, Crick F. Neuronal correlates of consciousness. The new cognitive neurosciences 2000; 1:3-24.
- American Society of Anesthesiologists. Continuum of depth of sedation: definition of general anesthesia and levels of sedation/analgesia. Amended October 21,2009. <http://www.asahq.org/For-Members/Standards and Guidelines/2012/continuum of depth of sedation 442012.ashx.
- Kearse LA Jr, Manberg P, Chamoun M, deBros F. Byspectral analysis of the electroencephalogram correlates with patient movement to skin incision during propofol/nitrous oxide anesthesia. Anesthesiology 1994; 81:1365-1370.
- Glass PS, Bloom M, Kearse L, Rosow C. Byspectral analysis measures sedation and memory effects of propofol, midazolam, isoflurane and alfentanil in healty volunteers. Anesthesiology 1997; 86:836-847.
- Myles PS, Leslie K, Mc Neil J. Bispectral index monitoring to prevent awareness during anaesthesia: the B-Aware randomized controlled trial. Lancet 2004; 363:1757-1763.
- Avidan MS, Jacobson E. Prevention of intraoperative awareness in a high risk surgical population. N Engl J Med 2011; 365:591-600.
- Kalkman J, Drummond J. Monitors of depth of anesthesia, Quo Vadis? Anesthesiology 2002; 96:784-787.
- Vuyk J, Sitsen E, ReekersMarije. Intravenous Anesthetics.Miller’s Anesthesia 2015; 1:821-863.
- Bauer KP, Dom PM, Ramirez A, O’Flaherty J. Preoperative intravenous midazolam: benefits beyond anxiolysis. J ClinAnesth 2004; 16:177-183.
- Ahuja M, Armstrong I. Sedation. Oxford specialist handbook of day surgery, 2011; 1:6-18.
- Bhananker SM, Posner KL, Cheney FW, Caplan RA, Lee LA, Domino KB. Injury and liability associated with monitored anesthesia care: a closed claims analysis. Anesthesiology 2006; 104:228-234.
- Hug CC Jr. MAC should stand for maximum anesthesia caution, not minimal anesthesiology care. Anesthesiology 2006; 104:221-223.
- American Society of Anesthesiologists. ASA position on monitored anesthesia care. Amended September 2, 2008. <http://www.asahq.org/For-Members/Clinical-Information/-/media/For-Members/documents/Standards Guidelines Stmts/Monitored Anesthesia Care.ashx.>





Bell’articolo che descrive la sedazione cosciente endovenosa in clinica medica ma non quella eseguita in Odontoiatria.
La Scuola di Padova, con il suo master in Sedazione cosciente ed emergenze in Odontoiatria, ci insegna invece, con casistiche amplissime, che seguendo il protocollo del prof. Manani, prevedente l’uso di clordemetildiazepam per os seguito da una titolazione SOGGETTIVA di una emulsione di Diazepam a dosi refratte fino alla valutazione di perfetta tranquillità dichiarata dal paziente stesso, si può ottenere una perfetta ansiolisi senza il rischio di continuum verso la narcosi.
In Italia, ci sono circa 300 colleghi formati presso l’Università di Padova più altri formati in corsi organizzati da associazioni scientifiche che praticano, da ann, in piena sicurezza questa modalità di sedazione lieve senza aver mai causato per questo danni al paziente.
Buongiorno a tutti.
Concordo pienamente con quanto scritto nel post precedente dal dott. Ferruccio Morandi, esperto sedazionista odontoiatra.
Suggerisco a tutti i lettori della vostra prestigiosa rivista di leggere le “Raccomandazioni per il controllo dell’ansia e del dolore in odontoiatria” pubblicate sul nostro sito AISOD (http://www.aisod.info/wp-content/uploads/Raccomandazioni.pdf). Risulterà chiaro a tutti che il “protocollo Manani” da noi proposto, prevedendo il raggiungimento dell’ansiolisi mediante titolazione soggettiva è una metodica sicura nelle mani dell’odontoiatra moderno che si aggiorna e vuole adeguarsi agli standard europei.
Giovanni Battista Grossi
Presidente AISOD
Buongiorno a tutti i convenuti:
1) Il dr. Morandi ha centrato il problema:
per quanto riguarda la sedazione cosciente in odontoiatria, esiste da più di 100 anni in UK (grazie alle iniziative del General Dental Council, di SAAD, DSTG etc.) e da circa 35 anni in Italia (grazie alle iniziative della Scuola di Anestesia Odontoiatrica di Padova incarnata nell’opera del prof. Giovanni Manani e coll., di AINOS prima e AISOD ora) una filosofia molto diversa rispetto a quella insegnata ed utilizzata in nord America. Nella filosofia odontoiatrica europea non è previsto l’uso di farmaci quali barbiturici, propofol, oppioidi, gas alogenati utilizzati invece in Nord America, da anestesisti ma anche da odontoiatri. Questi farmaci vengono impiegati, in Europa, solo dagli anestesisti per via dei rischi connessi, largamente descritti nell’articolo. Unica eccezione è l’uso del midazolam da parte degli odontoiatri – sedazionisti inglesi ma non italiani.
2) la filosofia italiana, essenzialmente quella della scuola di anestesia odontoiatrica di Padova, espressa nel suo decennale Master ( http://www.unipd.it/sedazione-emergenza-odontoiatria ) che ha formato ad oggi 125 sedazionisti, ha alla sua base il detto “primum non nocere”; è sufficente scorrere le 1140 pagine del testo di Manani e coll. “Anestesia Odontoiatrica ed Emergenze” III° edizione, Idelson-Gnocchi, Napoli, 2011, per capire che le tecniche comportamentali e farmacologiche insegnate agli ed impiegate dagli odontoiatri – sedazionisti italiani non hanno nulla a che fare con quelle impiegate dagli anestesisti nel loro ambiente. Insomma, le tecniche di ansiolisi e sedazione cosciente diffuse in Italia rispettano completamente i seguenti principi fondamentali:
I° Il paziente ha il diritto di ricevere, e l’odontoiatra ha il dovere di garantire, un percorso diagnostico -terapeutico privo di ansia e dolore.
II° Le tecniche ansiolitiche impiegate permettono di ottenere una modificazione minimale della coscienza, capace di rassicurare il paziente e di permettere che l’intervento possa essere effettuato con livelli minimali di stress psico-fisico. Deve essere conservata la possibilità di comunicare in ogni momento attraverso messaggi verbali o non verbali.
III° Le tecniche impiegate devono rendere assolutamente improbabile la perdita di coscienza.
IV° Di conseguenza, l’odontoiatra deve garantire anche una ALR efficace e duratura, mentre in nessun caso i farmaci sedativi possono essere utilizzati per compensare una carenza dell’ALR.
3) Chi vuole capire a fondo l’anestesia odontoiatrica (non l’anestesia medica) nella sua parte che riguarda l’ansiolisi farebbe bene a seguire il consiglio del dr. Grossi, attuale presidente di AISOD.
Porgo cordiali saluti ed il mio personale invito a studiare a fondo l’anestesia ODONTOIATRICA, disciplina fondante dell’odontoiatria, lasciata in disparte ormai da troppi anni …
Gastone Zanette
Direttore del Master “Sedazione ed emergenza in odontoiatria. Human Centered Project (HCP): il trattamento olistico del paziente odontoiatrico”. Università di Padova.
Past- president di AISOD