La capacità di ottenere un’efficace detersione e decontaminazione dello spazio endodontico e di rimuovere significativamente smear layer, batteri e loro prodotti dal sistema canalare rappresenta lo scopo della terapia endodontica. Moritz afferma che1 vi sono tre fattori principali che ostacolano il raggiungimento di un ambiente sterile in endodonzia: la configurazione dell’anatomia radicolare, la particolare flora batterica dell’endodonto, la difficoltà degli irriganti canalari a penetrare efficacemente in profondità nei tubuli dentinali. La complessità anatomica dell’endodonto è ben conosciuta: dai canali principali si dipartono numerosi canali laterali, di varie dimensioni e molteplici ramificazioni apicali. Un recente studio ha evidenziato la presenza di queste strutture anatomiche nel 75% dei denti analizzati e la presenza di residui pulpari infetti al termine della preparazione chemo-meccanica, sia nei canali laterali che nelle ramificazioni apicali di denti vitali e necrotici, con associata flogosi periradicolare2.
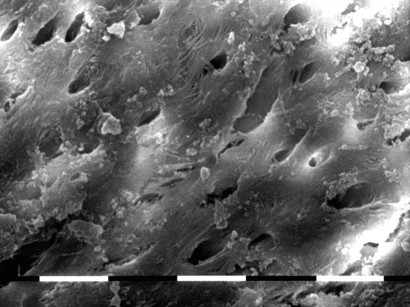
L’esistenza dei tubuli dentinali, inoltre, rappresenta una riserva per la sopravvivenza dei microrganismi che possono proliferare senza venire a contatto con il sistema immunitario3-5. La presenza di batteri nell’endodonto è limitata a un numero ristretto di specie che, tuttavia, mostrano una elevata patogenicità: possono infatti produrre o indurre la produzione di sostanze tossiche (leucotossine, endotossine, enzimi proteolitici\fibrinolitici)1,6. È stato inoltre dimostrato che, a causa di un’elevata tensione superficiale, gli irriganti endocanalari possono penetrare per 100-300 μm nei tubuli dentinali mentre i batteri possono colonizzare fino a 1100 μm partendo dal lume canalare verso l’interno dei tubuli7. Un lavaggio con EDTA o acido citrico è tuttavia in grado di rimuovere lo smear layer e di permettere all’ipoclorito di penetrare meglio nei tubuli dentinali8.
Laser in endodonzia
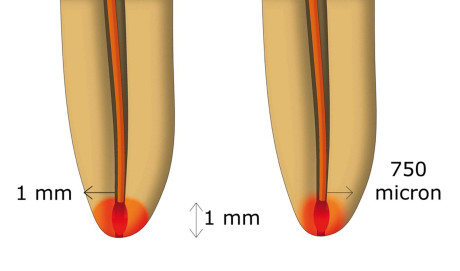
La tecnologia laser è stata introdotta nei primi anni Sessanta9, e in endodonzia la possibilità di decontaminare i canali radicolari grazie a energie molto concentrate si è iniziata a investigare dal 197010. Solo l’introduzione di fibre ottiche sottili e flessibili ha reso però possibile un’efficace penetrazione della luce nel terzo apicale. Differenti sono le lunghezze d’onda che si sono dimostrate efficaci nel ridurre notevolmente la carica batterica nei canali infetti e importanti studi hanno avvalorato “in vitro” questi risultati11. I laser a diodi (da 810 nm a 980 nm) e il Nd:YAG (1064 nm) che appartengono alla regione del “near infrared” dello spettro elettromagnetico della luce, hanno un’interazione prevalentemente per diffusione nei tessuti molli, più in profondità opera il laser Nd:YAG (fino a 4-5 mm), più superficialmente quelli a diodi (fino a 3 mm). La loro luce viene elettivamente assorbita da emoglobina, ossiemoglobina e melanina. In endodonzia rappresentano a oggi il migliore sistema di decontaminazione, grazie alla loro capacità di penetrare in profondità dentro i tubuli dentinali (fino a 750 micron i laser a diodi, fino a 1 mm il Nd:YAG11 (figura1) e per l’affinità di queste lunghezze d’onda con i batteri, che vengono distrutti per effetto fototermico12.
Schoop et al. (2004) hanno dimostrato su modello sperimentale come i laser diffondano la propria energia in profondità nella parete dentinale, dimostrandosi fisicamente più efficaci dei tradizionali sistemi irriganti chimici nel decontaminare le pareti dentinali in profondità11. Il laser Nd:YAG (1064 nm) ha mostrato riduzione batterica dell’85% a 1 mm, mentre il laser a diodi 810 nm del 63% a 750 micron e inferiore per il diodo 980 nm. Questa spiccata e differente penetrazione è dovuta alla scarsa e diversa affinità di queste lunghezze d’onda per i tessuti duri e per la tipica capacità di diffusione non uniforme che permette alla luce di raggiungere e distruggere per effetto termico i batteri anche in profondità (figure 2 e 3). Molti altri studi microbiologici hanno confermato la forte azione battericida dei laser a diodi e Nd:YAG, con decontaminazione fino al 100% della carica batterica nel canale principale13-16. Uno studio in vitro di Benedicenti et al. ha riportato come l’utilizzo di un laser a diodi 810 nm associato all’uso di irriganti chimici chelanti come acido citrico ed EDTA porti a una riduzione pressoché assoluta della carica batterica (99.9%) di Enterococcus faecalis dal sistema endodontico17. I laser Erbium (2780 nm e 2940 nm) appartengono alla regione del “medium infrared”, la loro luce è prevalentemente assorbita superficialmente nel tessuto molle, tra 100 e 300 micron e fino a 300-400 micron nelle pareti dentinali11,18; il cromoforo bersaglio è l’acqua, per questo il loro utilizzo in odontoiatria è esteso dai tessuti molli a quelli duri, per il contenuto in acqua di mucosa, gengiva, dentina e tessuto cariato che vengono vaporizzati per effetto termico.

Quando utilizzati in soluzione acquosa, l’esplosione delle molecole dell’acqua genera anche un certo grado di effetto fotomeccanico che partecipa al processo ablativo e di detersione19-21. Laser a Erbium con impulsi di durata molto corta (inferiore a 150 microsecondi) permettono con l’utilizzo di energie molto basse (meno di 50 mJ) il raggiungimento di potenze di picco assai elevate. L’utilizzo di energia minimamente ablativa riduce gli indesiderati effetti termici a vantaggio di fenomeni di esplosione delle molecole d’acqua (cromoforo bersaglio), con successiva produzione di effetti fotomeccanici e fotoacustici (shock wave) delle soluzioni irriganti introdotte nel lume canalare, sulle pareti dentinali. Questi effetti sono risultati estremamente efficaci nell’azione di detersione dello smear layer dalle pareti dentinali, nella rimozione del biofilm batterico e nella decontaminazione canalare22-25.
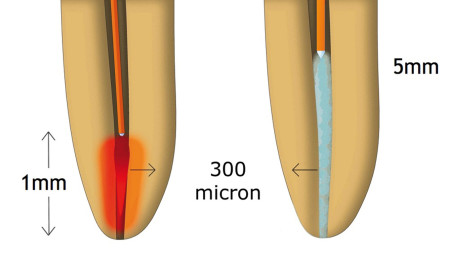
La decontaminazione tridimensionale del sistema endodontico eseguita con i laser Erbium non è ancora comparabile a quella dei laser near infrared. L’energia termica sviluppata da questi laser è infatti assorbita prevalentemente in superficie (elevata affinità per i tessuti dentinali ricchi di acqua), dove esercitano il più elevato potere battericida su E. coli, Gram- e E. faecalis gram+; a 1,5 W Moritz et al. (1999) hanno ottenuto una eradicazione quasi totale, del 99,64%, di questi batteri26; questi sistemi non sono però in grado di esercitare effetto battericida in profondità nei canali laterali, raggiungendo i 300 microns di profondità, nello spessore della parete radicolare11 (figura 4). Ulteriori studi (2007) hanno investigato l’efficacia dell’Er,Cr:YSGG laser nella decontaminazione di canali tradizionalmente preparati; utilizzando bassa potenza (0,5 W 10 Hz 50 mJ con 20% air/water spray) non si è ottenuta l’eradicazione completa dei batteri27, mentre risultati migliori per l’Er:YAG si sono ottenuti con una riduzione del 77% a 1 W e del 96% a 1,5 W15.
Un nuovo filone di ricerca (2006) ha investigato l’efficacia del laser Erbium nella rimozione del biofilm batterico a livello apicale28 e un recente studio in vitro (2008) ha ulteriormente validato la capacità del laser Er:YAG di rimuovere un biofilm endodontico formato da numerose specie batteriche (Actinomyces naeslundii, Enterococcus faecalis, Lactobacillus casei, Propionibacterium acnes, Fusobacterium nucleatum, Porphyromonas gingivalis, Prevotella nigrescens), con considerevole diminuizione delle cellule batteriche e disgregazione del biofilm, a eccezione di quello formato da L. casei29. Studi in corso stanno valutando l’efficacia di una nuova tecnica laser che utilizza una punta a emissione radiale a bassa energia, con produzione di elevato effetto fotomeccanico e fotoacustico per la rimozione oltre che dello smear layer25 anche del biofilm batterico. I risultati sono molto promettenti (figure 5-9). I laser Erbium hanno utilizzato sinora punte “end firing”, cioè con emissione frontale alla parte terminale della punta, e hanno dimostrato una scarsa penetrazione laterale nella parete dentinale. Nuove punte a emissione radiale sono state proposte nel 2007 per il laser Er,Cr:YSGG. Gordon et al.30 e Schoop et al.31,32 hanno studiato gli effetti morfologici e decontaminanti di questo nuovo sistema. I primi hanno utilizzato una punta da 200 microns a emissione radiale, a 20 Hz con spray aria/acqua (34% e 28%) e a secco, a 10 mJ e 20 mJ, 20 Hz (0,2 W e 0,4 W rispettivamente); i tempi di irradiazione erano variabili da 15 secondi sino a 2 minuti.
5-7. Immagini al SEM di dentina irradiata con radial firing tip, a 50 mJ, 10 Hz per 20 e 40 secondi in un canale irrigato con EDTA. Notevole detersione della dentina da detriti e smear layer. Esposizione della struttura collagenica. Immagini riprodotte per cortesia del dottor E. DiVito, Scottsdale, Arizona-USA.
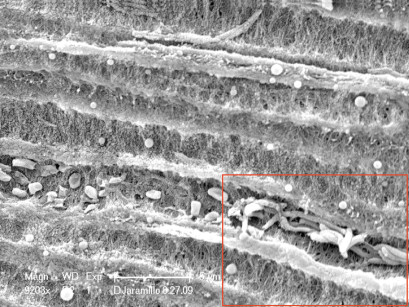

Il massimo potere battericida si è ottenuto alla massima potenza (0,4 W), con il tempo di esposizione più lungo e nella modalità senz’acqua, con una eradicazione del 99,71% di effetto battericida; il minimo tempo di irradiazione di 15 secondi alla potenza più bassa (0,2 W) con acqua ha ottenuto il 94,7%30. I secondi hanno utilizzato una punta da 300 microns di diametro a due differenti parametri di emissione, 1 W e 1,5 W, 20 Hz, irradiando 5 volte per 5 secondi con un tempo di raffreddamento di 20 secondi ogni passaggio. Il livello di decontaminazione ottenuto è stato significativamente elevato senza importanti differenze tra 1 W e 1,5 W, con rialzo termico contenuto tra 2,7 °C e 3,2 °C31. Lo stesso gruppo di Vienna ha studiato anche i parametri 0,6 W e 0,9 W che producevano un rialzo termico molto contenuto rispettivamente di 1,3 °C e 1,6 °C, mantenendo un elevato effetto battericida su E. coli e E. faecalis32. L’effetto termico dei laser, utilizzato per l’effetto battericida, deve essere controllato per evitare danni sulle pareti dentinali: l’irradiazione a parametri corretti produce, infatti, oltre alla vaporizzazione dello smear layer (solo i medium infrared laser) e della struttura organica dentinale (fibre collagene) anche aspetti di fusione superficiale più o meno marcati a seconda della lunghezza d’onda (near e medium infrared laser). I soli laser Erbium producono anche fenomeni ablativi superficiali della dentina, più prevalenti nelle aree intertubulari più ricche in acqua che in quelle peritubulari più mineralizzate. I danni termici, quando si utilizzano parametri o modalità di utilizzo scorretti, si manifestano con estese aree di fusione (melting), di ricristallizzazione della matrice minerale (bubble), con microfratture superficiali con segni di carbonizzazione radicolare interna ed esterna.
Decontaminazione con near infrared laser
La decontaminazione canalare laser-assistita eseguita con laser near infrared richiede che i canali vengano preparati in maniera tradizionale (preparazione apicale con strumenti ISO 25/30) non avendo questa lunghezza d’onda nessuna affinità e quindi capacità ablativa sui tessuti duri. L’irradiazione viene eseguita come passaggio finale per decontaminare il sistema endodontico prima dell’otturazione. La fibra ottica di 200 micron precedentemente attivata su una superficie scura (figura 10) è inserita a 1 mm dalla lunghezza di lavoro e azionata con movimento elicoidale in direzione apico-coronale per 5-10 secondi, avendo cura di non indugiare all’apice per più di 1 secondo (figura 11).
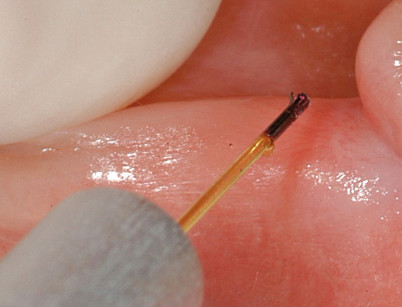
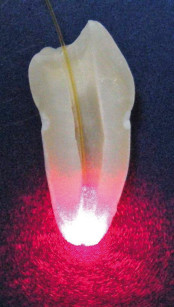
I parametri di utilizzo del laser a diodi 810 nm sono: 2,5 W di potenza in modalità pulsate con 10 ms di azione e 10 ms di pausa. Per il diodo 980 nm le potenze vanno ridotte a 1,5 W sempre in modalità pulsata. Per il laser Nd:Yag i parametri sono 1,5 W di potenza e 15 Hz di frequenza. Dopo aver eseguito per tre volte la decontaminazione con il canale “in bagno” di ipoclorito, si irriga con acido citrico al 10% o EDTA al 17% e si esegue nuovamente la decontaminazione laser. Al lavaggio di ipoclorito ne segue un’ulteriore di ipoclorito e un successivo passaggio per tre volte con laser alle potenze e secondo i tempi precedentemente descritti (figure 12-16).
12-13. Ritrattamento di 46 con estesa lesione apicale e mobilità grado 2. La radiografia pre-operatoria ci consente di apprezzare le dimensioni della lesione e l’importante indebolimento del setto interradicolare. È stata effettuata decontaminazione endocanalare laser-assistita con laser a diodi 810 nm secondo il protocollo descritto nel testo. La radiografia di controllo mostra una rapida risposta tissutale - dovuta anche all’azione fisica della luce laser - e remissione quasi completa della lesione.
14-16. Trattamento endodontico di 46 in giovane paziente con pulpite sintomatica. La sagomatura del canale MV si presenta alquanto difficoltosa per la presenza di una curva severa al terzo apicale, come dimostrato dall’rx della prova dei coni. Viene eseguita decontaminazione del sistema dei canali radicolari con laser Nd:Yag seguendo il protocollo descritto nel testo. La radiografia di controllo mostra una corretta otturazione tridimensionale del SCR.
Decontaminazione con medium infrared laser
Considerata la scarsa efficacia nella preparazione e sagomatura canalare, anche l’utilizzo dei laser Erbium per la decontaminazione in endodonzia prevede una preparazione canalare eseguita con tecnica tradizionale, con canali preparati all’apice con strumenti ISO 25-30; il passaggio finale con il laser è reso possibile grazie all’utilizzo di punte lunghe e sottili (200 e 320 micron), disponibili per alcune apparecchiature Erbium, in grado di raggiungere facilmente la lunghezza di lavoro (1 mm dall’apice). Anche in questo caso la tecnica tradizionale prevede un movimento elicoidale di retrazione della punta (in 5-10 secondi), da ripetersi 3-4 volte a seconda dei protocolli, alternando l’irradiazione all’irrigazione con i comuni prodotti chimici, eseguendo la procedura in un canale bagnato (ipoclorito di sodio e/o EDTA); lo spray integrato va mantenuto chiuso.
I parametri a oggi accettati e utilizzati per i laser Er:YAG sono: potenza 1,125 W, energia 75 mJ e frequenza 15 Hz, mentre per i laser Er,Cr:YSGG sono: potenza 1,5 W, energia 75 mJ, frequenza 20 Hz. Recentemente è stata introdotta per i laser Er:YAG una nuova metodica. La tecnica Photon Initiated Photoacustic Streaming (PIPS) prevede l’utilizzo del laser Erbium (Fidelis III AT/HT - Ligthwalker ST-E/AT Fotona, Lubiana, Slovenia) e della sua interazione con le soluzioni irriganti (17% EDTA o 5,5% NaOCl)25. La tecnica si propone con un meccanismo diverso rispetto ai precedenti; essa sfrutta esclusivamente i fenomeni fotoacustici e fotomeccanici che risultano dall’utilizzo di energia minimamente ablativa di 20 mJ a 15 Hz, con impulsi di soli 50 microsecondi.
A fronte di una potenza media di soli 0,3 W, ogni impulso interagisce con le molecole d’acqua con una potenza di picco di 400 W, in grado di creare esplosione e successivo “shock waves” con formazione di un forte flusso di fluidi all’interno del canale, senza generare gli indesiderati effetti termici; questi, misurati con termocoppie sulla superficie radicolare, sono risultati essere 1,2 °C e 1,5 °C rispettivamente a 20 e a 40 secondi. Questa sistematica, per la minima energia applicata e la ridotta potenza sviluppata, può essere considerata più una tecnica di irrigazione canalare che una procedura di irradiazione laser. Gli effetti fisici (fototermici) indesiderati vengono ridotti o annullati, mentre sono implementati gli effetti chimici (decontaminante e/o detergente) propri dei vari irriganti utilizzati che vengono spinti nel sistema endodontico tridimensionalmente, con maggiore efficacia. Altro considerevole vantaggio deriva dall’inserimento della tip in camera pulpare all’imbocco canalare, senza avere problemi nell’inserimento delle punte a 5 mm o a 1 mm dall’apice come previsto per le altre tecniche. Vengono utilizzate punte di nuovo disegno di 12 millimetri di lunghezza, di 300-400 micron di diametro, con terminale “radial firing”; i 4 millimetri finali sono liberati dalla pellicola di rivestimento in modo tale da permettere una maggiore emissione laterale di energia, rispetto a quella frontale; questa modalità di emissione porta a un migliore utilizzo dell’energia laser che a soglia minimamente ablativa eroga una potenza di picco molto elevata per ogni singolo pulse (400 W), producendo così “shock wave” sugli irriganti, con un effetto fotoacustico e fotomeccanico importante sulla parete dentinale25. La tecnica PIPS utilizza i seguenti parametri: energia 20 mJ, 15 pps, con impulso di 50 microsecondi e la specifica punta da 400 micron (lunga 14 mm) a emissione laterale, privata della guaina esterna negli ultimi 4 mm (tapered and stripped tip) (figure 17 e 18).
17-18. Punte endodontiche per tecnica PIPS.
Il protocollo operativo prevede un’irrigazione/irradiazione con ipoclorito di sodio al 5,5% con tecnica PIPS, per 20 secondi, dopo ogni strumentazione canalare e passaggio finale con irrigazione/irradiazione con EDTA al 17% per 20 secondi prima dell’otturazione (figure 19-30).
19-21. Denti 31e 41: ritrattamento canalare richiesto per sintomatologia dolora alla pressione degli elementi dentari. L’rx pre-operatoria evidenzia riempimento canalare incompleto, mancato trattamento del secondo canale e radiolucenza periapicale. I canali linguali sono stati trovati dopo ispezione microscopica e lavaggi con irriganti e laser Erbium con tecnica PIPS (Er:YAG Fidelis III, Fotona, Slovenia). Canali ritarati e otturati con guttaperca e minima estrusione di cemento all’apice (Endoreze, Ultradent, USA).
22-23. Dente 33: l’esame radiografico mostra ampia lesione periapicale in dente non vitale, di probabile origine endoparodontale.Trattamento dei due distinti canali, con otturazione con guttaperca e cemento che si riunificano all’apice, dopo trattamento con laser con tecnica PIPS (Er:YAG Fidelis III, Fotona, Slovenia). Estrusione di cemento resinoso all’apice (Endoreze, Ultradent, USA).
24-26. Dente 17: la radiografia mostra radiolucenza per lesione periapicale del secondo molare; la vicinanza dell’impianto endo-osseo inserito in sede 1.6 indica la necessità di ritrattamento del secondo molare, seppur asintomatico. Dopo rimozione del materiale di otturazione preesistente, si irriga con tecnica PIPS (Er:YAG Fidelis III, Fotona, Slovenia) ed EDTA 17%; otturazione immediata, con riempimento dell’intero lume, sino all’apice con riempimento di un canale laterale. Il controllo a 4 mesi evidenzia il riassorbimento del cemento resinoso (Endoreze, Ultradent, USA) oltre apice.
27-28. Dente 26: primo molare superiore con pulpita acuta.Trattamento “one visit” con decontaminazione e detersione con NaOCl ed EDTA attivati con tecnica PIPS (Er:YAG Fidelis III, Fotona, Slovenia). Preparazione minimale dei canali vestibolari e MB2 a ISO 25/04 e 25/06 per il palatino. Otturazione con guttaperca e cemento resinoso (Endoreze, Ultradent, USA).
29-30. Dente 47: secondo molare inferiore destro con ascesso periapicale acuto e radiolucenza all’esame radiografico. Trattamento in due sedute con medicazione intermedia con Ca(OH)2. Detersione e decontaminazione con NaOCl ed EDTA attivate con tecnica PIPS (Er:YAG Fidelis III, Fotona, Slovenia). Otturazione dei canali laterali delle radici mesiale e distale, con modica estrusione di cemento (Endoreze, Ultradent, USA).
Discussione e conclusioni
Scopo del trattamento endodontico è pulire e disinfettare il sistema dei canali radicolari e nel sigillarlo tridimensionalmente ma, sfortunatamente, questo obiettivo non è sempre raggiunto. È raro per un trattamento ortogrado superare il 90% di successo33. Molti studi hanno dimostrato che trattamenti endodontici su denti vitali senza radiotrasparenze apicali hanno possibilità di successo migliori, con percentuali di insuccesso inferiori al 4% laddove la percentuale di fallimento per denti non vitali con radiotrasparenze apicali sale al 20%34. Molti fattori possono compromettere il risultato finale del trattamento endodontico, primo fra tutti la complessità anatomica del sistema dei canali radicolari e la conseguente difficoltà a far agire efficacemente gli irriganti nel terzo apicale35. I laser Nd:Yag e a diodi da 810 nm a 980 nm si sono dimostrati efficaci nel ridurre la carica batterica endocanalare; recentemente anche i laser Er:Yag e Er,Cr:Ysgg si sono dimostrati efficaci nel potenziare l’azione degli irriganti comunemente utilizzati, costituendo oggi un prezioso alleato per diminuire la carica batterica endocanalare e migliorare la rimozione dello smear layer prodotto dalla strumentazione. Il continuo miglioramento della tecnologia sta portando a un’evoluzione dell’interazione laser con il tessuto bersaglio, a interazione laser-irrigante-tessuto, con diminuzione degli effetti fisici indesiderati (termici) e aumentata perfusione ed efficacia degli effetti chimici (decontaminanti e chelanti) degli irriganti canalari. Come ogni presidio tecnologico il loro utilizzo non può prescindere da una necessaria curva di apprendimento e dall’applicazione di parametri rigorosi acquisiti dalla letteratura scientifica internazionale.
Bibliografia
1. Moritz A, Schoop U, Kluger W, Jakolitsch S, Sperr W. Laser in endodontology. Journal of Oral Laser Applications 2001;2:87-97.
2. Ricucci D, Siqueira JF Jr. Fate of the tissue in lateral canals and apical ramifications in response to pathologic conditions and treatment procedures. J Endod 2010 Jan;36(1):1-15.
3. Nagaoka S et al. Bacterial invasion into dentinal tubules of human vital and non vital teeth. J Endod 1995;21:70-73.
4. Ramachandran PN. Light and electron microscopic studies of root canal flora and periapical lesions. J Endod 1987;13:29-39.
5. Shovelton DS. The presence and distribution of microrganisms within non vital teeth. Br Dent J 1964;117:101-107.
6. Meryon SD et al. Penetration of dentine by three oral bacteria in vitro and their associated cytotoxixity. Int Endo J 1990;23:196-202.
7. Berutti E et al. Penetration ability of different irrigants into dentinal tubules. J Endod 1997;23:725-727.
8. Ghoddusi J, Rohani A, Rashed T, Ghaziani P, Akbari M. An evaluation of microbial leakage after using MTAD as a final irrigation. JOE 2007;vol 33,2:173-6.
9. Maiman TH. Stimulated optical radiation in ruby. Nature 1960;187:4493-494.
10. Weichmman JA. Laser use in endodontics. Oral Surgery 1972;31:416-20.
11. Schoop U, Kluger W, Moritz A, Nedjelik N, Georgopoulos A, Sperr W. Bactericidal effect of different laser systems in the deep layers of dentin. Lasers Surg Med 2004;35(2):111-6.
12. Moritz A. Oral Laser Application. Berlin: Quintessence Verlags-GmbH, 2006, 258-277.
13. Moritz A, Gutknecht N, Goharkhay K, Schoop U, Wernisch J, Sperr W. In vitro irradiation of infected root canals with a diode laser: results of microbiologic, infrared spectrometric, and stain penetration examinations. Quintessence Int 1997, Mar;28(3):205-9.
14. Schoop U, Kluger W, Dervisbegovic S, Goharkhay K, Wernisch J, Georgopoulos A, Sperr W, Moritz A. Innovative wavelengths in endodontic treatment. Lasers Surg Med 2006 Jul;38(6):624-30.
15. Wang QQ, Zhang CF, Yin XZ. Evaluation of the bactericidal effect of Er,Cr:YSGG, and Nd:YAG lasers in experimentally infected root canals. J Endod 2007 Jul;33(7):830-2. Epub 2007 May 7.
16. de Souza EB, Cai S, Simionato MR, Lage-Marques JL. High-power diode laser in the disinfection in depth of the root canal dentin. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 2008 Jul;106(1):e68-72.
17. Benedicenti S, Cassanelli C, Signore A, Ravera G, Angiero F. Decontamination of root canals with the gallium-aluminum-arsenide laser: an in vitro study. Photomed Laser Surg 2008 Aug;26(4):367-70.
18. Hibst R, Stock K, Gall R, Keller U. Controlled tooth surface heating and sterilization by Er:YAG laser radiation. Proc. SPIE; vol. 2922:119-1261.
19. Rizoiu IM, DeShazer GL. New laser-matter interaction concept to enhance hard tissue cutting efficiency. Laser Tissue. San Josè, California: Interaction V, Vol. 2134A, 309-317, 1994
20. Meister J, Franzen R, Forner K, Grebe H, Stanzel S, Lampert F, Apel C. Influence of the water content in dental enamel and dentin on ablation with erbium YAG and erbium YSGG lasers. J Biomed Opt 2006 May-Jun;11(3):34030.
21. Chen Z, Bogaerts A, Vertes A. Phase explosion in atmospheric pressure infrared laser ablation from water-rich targets. App Phys Letters 2006;89,041503:1-3.
22. De Moor RJ, Meire M, Goharkhay K, Moritz A, Vanobbergen J. Efficacy of ultrasonic versus laser-activated irrigation to remove artificially placed dentin debris plugs. J Endod 2010 Sep;36(9):1580-3.
23. de Groot SD, Verhaagen B, Versluis M, Wu MK, Wesselink PR, van der Sluis LW. Laser-activated irrigation within root canals: cleaning efficacy and flow visualization. Int Endod J 2009 Dec;42(12):1077-83.
24. Hmud R, Kahler WA, George R, Walsh LJ. Cavitational effects in aqueous endodontic irrigants generated by near-infrared lasers. J Endod 2010 Feb;36(2):275-8. Epub 2009 Dec 4.
25. DiVito E, Peters OA, Olivi G. Effectiveness of the Erbium:YAG laser and new design radial and stripped tips in removing the smear layer after root canal instrumentation. Lasers Med Sci 2010 Dec 1.
26. Moritz A, Schoop U, Goharkhay K, Jakolitsch S, Kluger W, Wernisch J, Sperr W. The bactericidal effect of Nd:YAG, Ho:YAG, and Er:YAG laser irradiation in the root canal: an in vitro comparison. J Clin Laser Med Surg 1999;17(4):161-4.
27. Eldeniz AU, Ozer F, Hadimli HH, Erganis O. Bactericidal efficacy of Er,Cr:YSGG laser irradiation against Enterococcus faecalis compared with NaOCl irrigation: an ex vivo pilot study. Int Endod J 2007 Feb;40(2):112-9.
28. Araki AT, Ibraki Y, Kawakami T, Lage-Marques JL. Er:Yag laser irradiation of the microbiological apical biofilm. Braz Dent J 2006;17(4):296-9.
29. Noiri Y, Katsumoto T, Azakami H, Ebisu S. Effects of Er:YAG laser irradiation on biofilm-forming bacteria associated with endodontic pathogens in vitro. J Endod 2008 Jul;34(7):826-9. Epub 2008 May 22.
30. Gordon W, Atabakhsh VA, Meza F, Doms A, Nissan R, Rizoiu I, Stevens RH. The antimicrobial efficacy of the erbium, chromium:yttrium-scandium-gallium-garnet laser with radial emitting tips on root canal dentin walls infected with Enterococcus faecalis. J Am Dent Assoc 2007 Jul;138(7):992-1002.
31. Schoop U, Goharkhay K, Klimscha J, Zagler M, Wernisch J, Georgopoulos A, Sperr W, Moritz A. The use of the erbium, chromium:yttrium-scandium-gallium-garnet laser in endodontic treatment: the results of an in vitro study. J Am Dent Assoc 2007 Jul;138(7):949-55.
32. Schoop U, Barylyak A, Goharkhay K, Beer F, Wernisch J, Georgopoulos A, Sperr W, Moritz A. The impact of an erbium, chromium:yttrium-scandium-gallium-garnet laser with radial-firing tips on endodontic treatment. Lasers Med Sci 2007 Nov 20 [Epub ahead of print].
33. Sjogren U et al. Factors affecting the long term results of endodontics treatment. J Endodon 1990;16:498-504.
34. Kerekes K, Tronstad L. Long term results of endodontic treatment performed with astandardized technique. J Endod 1979;5:83-90.
35. Kreisler M et al. Efficacy of NaOCl/H2O2 irrigation and GaAlAs laser decontamination of root canals in vitro. Lasers in surgery and Medicine 2003;32:189-196.