Riassunto
Obiettivo. Un’apicectomia viene spesso eseguita su denti necrotici che sono la conseguenza, nella maggior parte dei casi, di un processo infiammatorio determinato dalla diffusione di microrganismi. Per effettuare l’apicectomia sono noti più tipi di laser, ognuno con peculiarità specifiche e tutti con marcate proprietà antibatteriche. Scopo di questo lavoro è valutare l’utilizzo dei laser Erbio:Ittrio-Alluminio-Granato (Er:YAG) ed Erbium-Cromo:Ittrio-Scandium-Gallio-Garnet (ErCr:YSGG) nell’ambito del trattamento endodontico retrogrado.
Materiali e metodi. Lo studio, effettuato tra gli anni 2002 e 2010, considera 45 apicectomie, 19 in uomini e 26 in donne, effettuate con vari tipi di laser ad Erbio, dei quali quello più utilizzato è stato il laser ErCr:YSGG. I laser usati nello studio hanno una lunghezza d’onda di 2940 nm per Er:YAG e di 2780 nm per ErCr:YSGG. Tutti i quadranti dell’arcata dentale sono stati interessati dagli interventi di resezione apicale (I quadrante 17 casi – 38%, II quadrante 21 casi – 41%, III quadrante 4 casi – 9%, IV quadrante 3 casi - 7% ). Il follow-up dei casi ha riguardato a 1 anno 23 casi, a 3 anni 16 casi, a >5 anni 6 casi .
Risultati. Dei sei casi con follow-up >5 anni in un caso si è verificata la perdita dell’elemento dentale dovuta a frattura dopo 4 anni della radice (elemento 13 del I quadrante). Si sono registrate 2 recidive con altrettanti reinterventi in due casi con follow-up oltre i 3 anni. Un altro fallimento si è verificato per frattura dell’elemento 46 trattato con doppia apicectomia su entrambe le radici e poi sostituito dopo 9 mesi con due impianti in titanio.
Conclusioni. Per le caratteristiche proprie, per la facilità di uso, per la capacità sterilizzante, per il minor danno provocato al paziente, i laser ad Erbio offrono un valido aiuto nella terapia endodontica. L’uso del laser per le apicectomie ha già oggi notevoli vantaggi e con il tempo il miglioramento delle tecnologie e la diminuzione dei costi potrà certamente affiancare i convenzionali metodi di chirurgia endodontica.
È noto che nell’elemento dentario la distruzione dello smalto e della dentina permette ai microrganismi di raggiungere la polpa, arrivando fino all’apice della radice dopo essersi insediati nel canale principale, avere invaso i tubuli dentinali e le ramificazioni del sistema canalare, sedi nelle quali proliferano1. Da ciò ne consegue che attorno all’apice della radice si forma un tessuto reattivo infiammatorio carico di colonie batteriche2,3 che provoca la formazione di una lacuna più o meno grande di riassorbimento osseo. L’interessamento dell’apice radicolare da parte dei microrganismi propone un’adeguata terapia, per lo più rappresentata dall’apicectomia. Infatti la clinica suggerisce una simile condotta nelle seguenti situazioni:
• presenza di un granuloma apicale in un dente non trattabile in seguito a difficoltà anatomica insuperabile nel sondaggio del canale;
• insuccesso della terapia endodontica in un dente già trattato per presenza di un granuloma apicale;
• frattura trasversale del terzo apicale della radice dentale;
• perforazione dell’apice dentale con impossibilità di efficace chiusura endodontica;
• rottura accidentale di strumenti endodontici manuali o rotanti al terzo apicale dentale con ritenzione o fuoriuscita parziale degli stessi che impediscano la corretta chiusura apicale;
• difficoltà di chiusura legate ad anomalie apicali anatomiche (curvature, delta apicale, imbuto apicale ecc.);
• riacutizzazioni infettive croniche o drenaggi imperfetti di ascessi apicali;
• presenza in un dente con granuloma apicale di perni radicolari, che potrebbero fratturare la radice nel caso si tentasse la loro rimozione manuale o che non si riescano a rimuovere;
• presenza di apici dentali immaturi o apicolisi;
• rimozioni di cisti mascellari che coinvolgano più apici dentali all’interno o in prossimità delle cisti stesse;
• eccesso di materiale endodontico fuoriuscito dall’apice che causi infiammazione o infezione apicale cronica.
Più di una sono le modalità di effettuazione di una disinfezione apicale; non sempre però il trattamento adottato porta a risultati positivi, potendosi verificare delle complicanze che, spaziando in più condizioni, possono esitare in un insuccesso terapeutico conservativo, condizionando la successiva estrazione dell’elemento dentario, come suggerito da alcuni studiosi. Tra le cause di insuccesso va annoverata l’insorgenza di processi infiammatori per diffusione di microrganismi, anche se il procedimento terapeutico condotto abbia scrupolosamente seguito un’accurata preparazione meccanica, chimica e fisica. Secondo la letteratura1,2 le condizioni principali che inducono infezioni intraradicolari sono costituite da:
• difficoltà di apertura e di detersione del sistema canalare;
• diffusione di processi infettivi indotti da microrganismi provenienti da:
a. infiltrazioni coronali in denti ricoperti,
b. tragitti fistolosi tra regione periapicale e cavità orale,
c. tasche parodontali,
d. comunicazioni orosinusali1,2.
Studi microbiologici, condotti con tecniche anaerobiche, hanno rilevato che nei casi di insuccesso della terapia canalare ortograda la flora microbica differisce da quella presente nella polpa necrotica ed è costituita prevalentemente da flora anaerobica, sia Gram+ che Gram- distribuite in ugual misura. Inoltre, quantitativamente la flora microbica presenta un maggior numero di colonie rispetto a quelle che si rilevano nelle infezioni apicali, nelle quali vi sono anche microrganismi iatrogeni (Enterococcus faecalis, Actinomyces spp, Propionibacterium spp) pervenuti dalla strumentazione scanalare manuale o meccanica1-4. Se ne può, quindi, dedurre che nella terapia canalare ortograda, ma non solo, la presenza di infezioni batteriche può essere causa di insuccesso della terapia stessa, fenomeno reso ancor più manifesto se l’infiammazione diviene cronica. Si è notato, infatti, che i microrganismi sono in grado di formare uno strato polisaccaridico impenetrabile al trattamento chemioterapico rendendo così l’infiammazione di tipo cronico, la cui risoluzione avviene solo con la rimozione dello strato microbico, che può avvenire esclusivamente con un’azione meccanica. Quantunque la chirurgia endodontica risulti essere il trattamento di scelta in presenza di denti con lesioni periapicali, non sempre può essere adottata, soprattutto quando esistono situazioni che non rispondono o non possono essere risolte con la tradizionale endodonzia ortograda3,12.
Risulta quindi evidente che la sola terapia ortograda non è in grado di risolvere processi periapicali cronici. Tuttavia un discreto numero di fallimenti si verifica anche nella terapia endodontica retrograda, condizione che alcuni studiosi suggeriscono di risolvere con un reintervento anziché procedere all’estrazione dell’elemento dentario3. Un ritrattamento retrogrado eseguito con tecniche più moderne e con sigillanti più innovativi permetterebbe infatti la guarigione di un numero significativo di elementi dentari per i quali il primo trattamento si è rivelato fallimentare. In particolare, la maggior disinfezione della porzione terminale del canale radicolare e dell’area periapicale e un più adeguato sigillo del forame apicale garantirebbero un notevole incremento delle percentuali di successo della terapia3. È perciò utile, per confinare ancor più remotamente la possibilità di insuccesso, l’impiego di attrezzature e di mezzi che operino in condizioni di sempre più profonda sterilità, oltre a offrire i vantaggi propri della terapia chirurgica ed endodontica.
Materiali e metodi
Lo studio si avvale di 45 apicectomie in denti necrotici con lesioni apicali effettuate presso l’Istituto Stomatologico Italiano di Milano e il DISTBIMO dell’Università degli Studi di Genova nel periodo compreso tra il 2002 e il 2010. La resezione dell’apice dentale è avvenuto in 19 uomini e in 26 donne. Tutti i quadranti sono stati interessati dagli interventi di resezione apicale (I quadrante 17 casi – 38%, II quadrante 21 casi – 46,5%, III quadrante 4 casi – 9%, IV quadrante 3 casi - 6,5%). Il follow-up dei casi ha riguardato a 1 anno 23 casi, a 3 anni 16 casi, a più di 5 anni 6 casi. Riportiamo, qui di seguito, il protocollo del trattamento dei pazienti. Previa anestesia locale con carbocaina 2% e adrenalina 1:100.000 gli interventi sono stati eseguiti con i seguenti laser:
• Fidelis Plus II, Fotona, Er:YAG 2940 nm, conduzione in braccio articolato, manipolo R05-Ti con tip da 400 micron con i seguenti parametri: Apertura del lembo mucoperiosteo in modalità VSP, Potenza 250 mJ, Frequenza 12 Hz, spray aria/acqua 80ml/min. Osteotomia e rimozione apice radicolare con manipolo R05-Ti e tip da 600 micron, modalità VSP, Potenza 400 mJ, Frequenza 15 Hz, spray aria /acqua 100ml/min.
• Opus Duo, Lumenis Er:YAG 2940 nm, conduzione in fibra cava, manipolo curvo, tip HPX da 400 micron tronco conica con i seguenti parametri: Apertura del lembo mucoperiosteo, Potenza 250 mJ, Frequenza 12 Hz, spray aria /acqua 80ml/min. Osteotomia e rimozione apice con tip HPX da 600 micron, Potenza 400 mJ, Frequenza 15 Hz, spray aria/acqua 100ml/min.
• Waterlase Biolase, ErCr:YSGG 2780 nm, conduzione in fibra ottica, manipolo diritto, tip T4 lunghezza 6 mm da 400 micron con i seguenti parametri: Apertura del lembo mucoperiosteo, Potenza 2.0 W, Frequenza 15 Hz, spray aria 60%, acqua 40%. Osteotomia e rimozione apice con tip G6 lunghezza 6 mm da 600 micron, Potenza 4.0 W, Frequenza 20 Hz, spray aria 55%, acqua 45%.
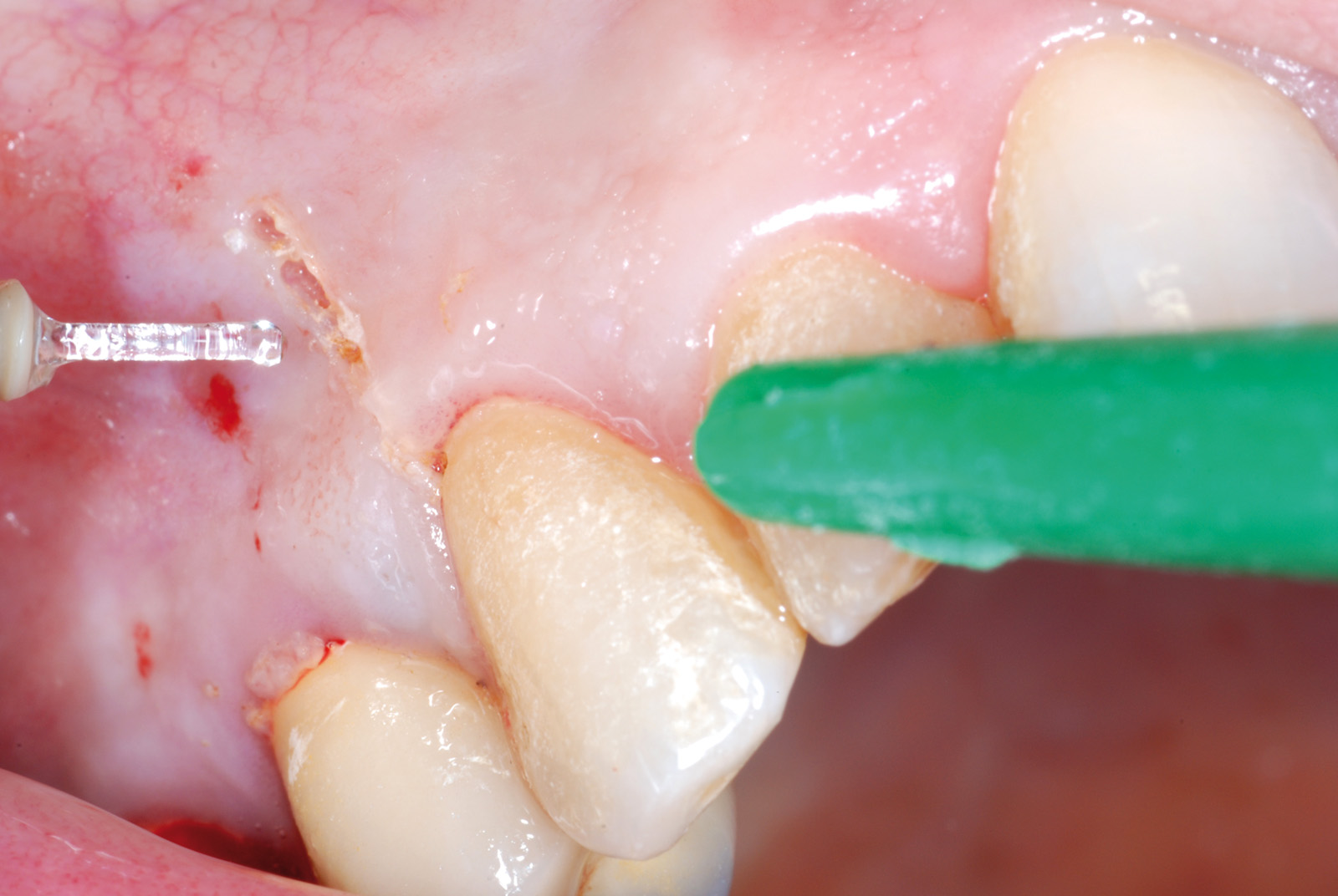
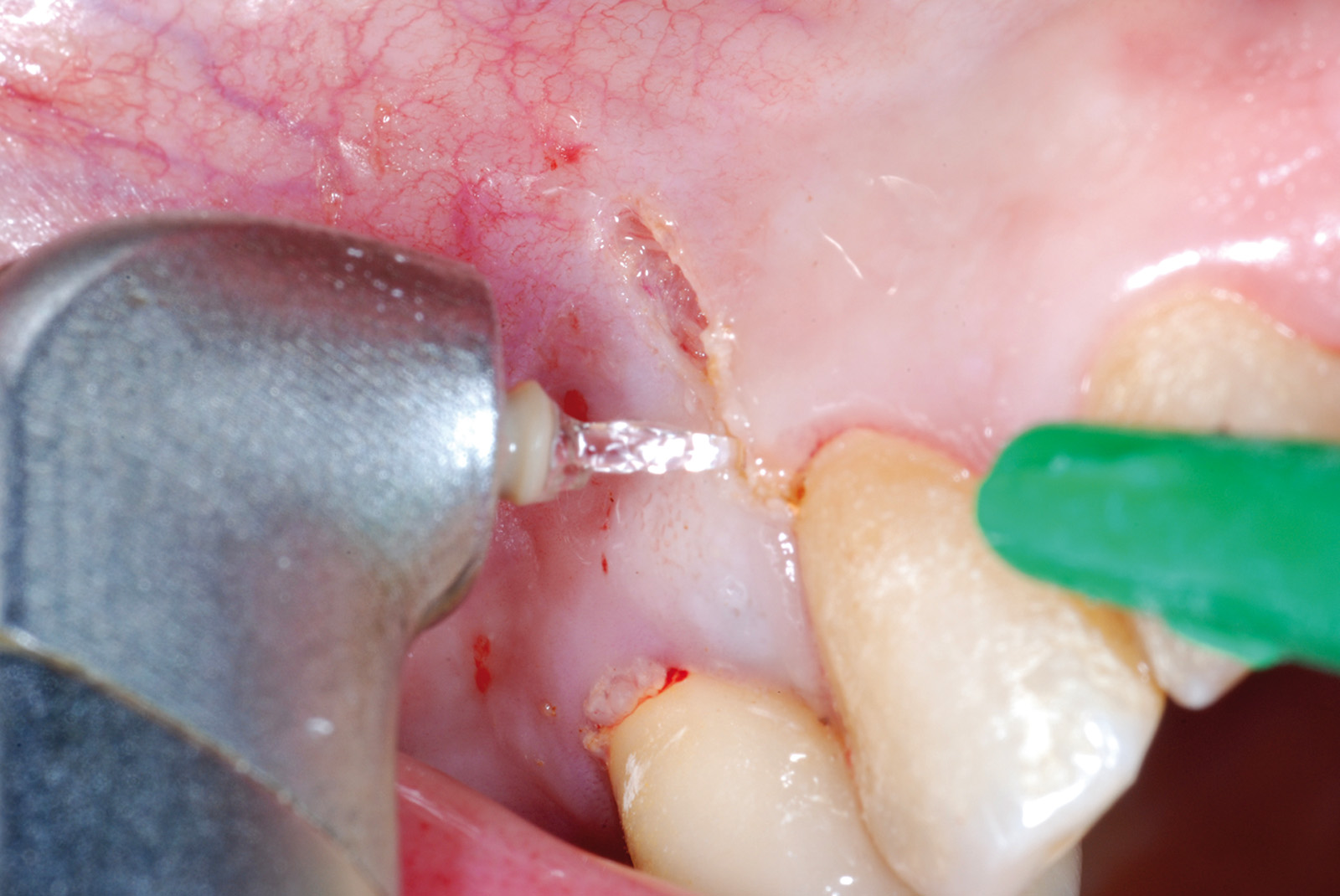
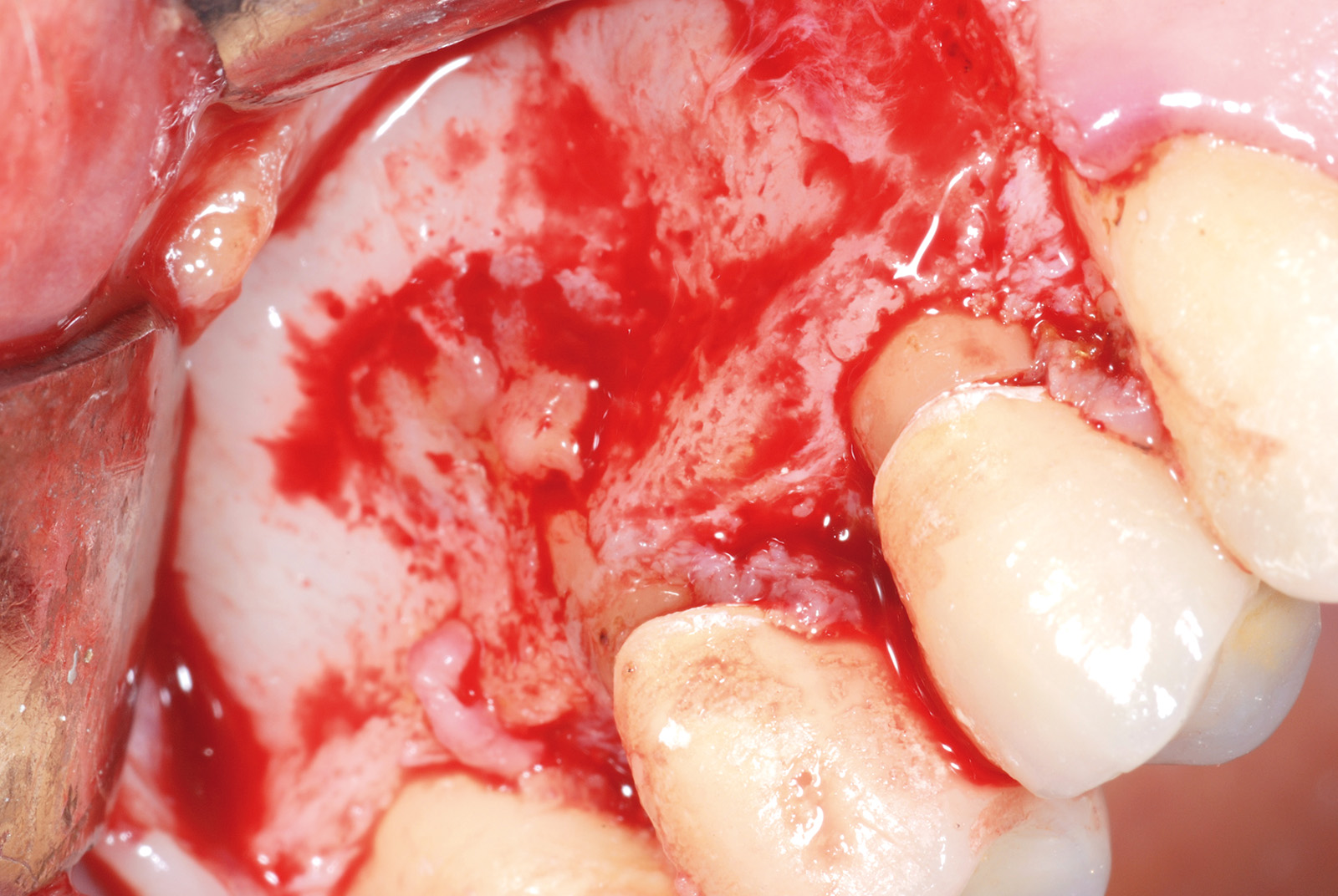
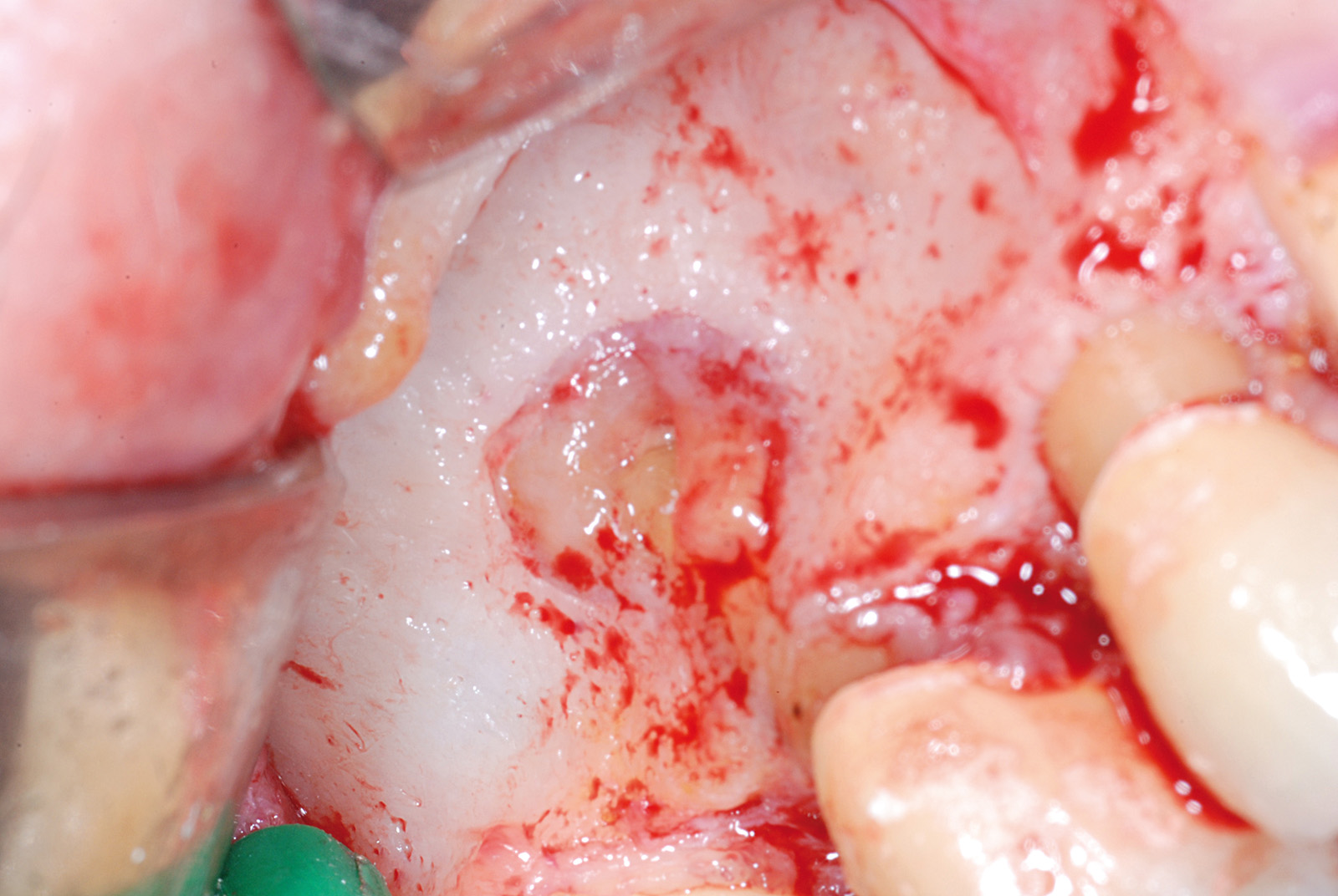
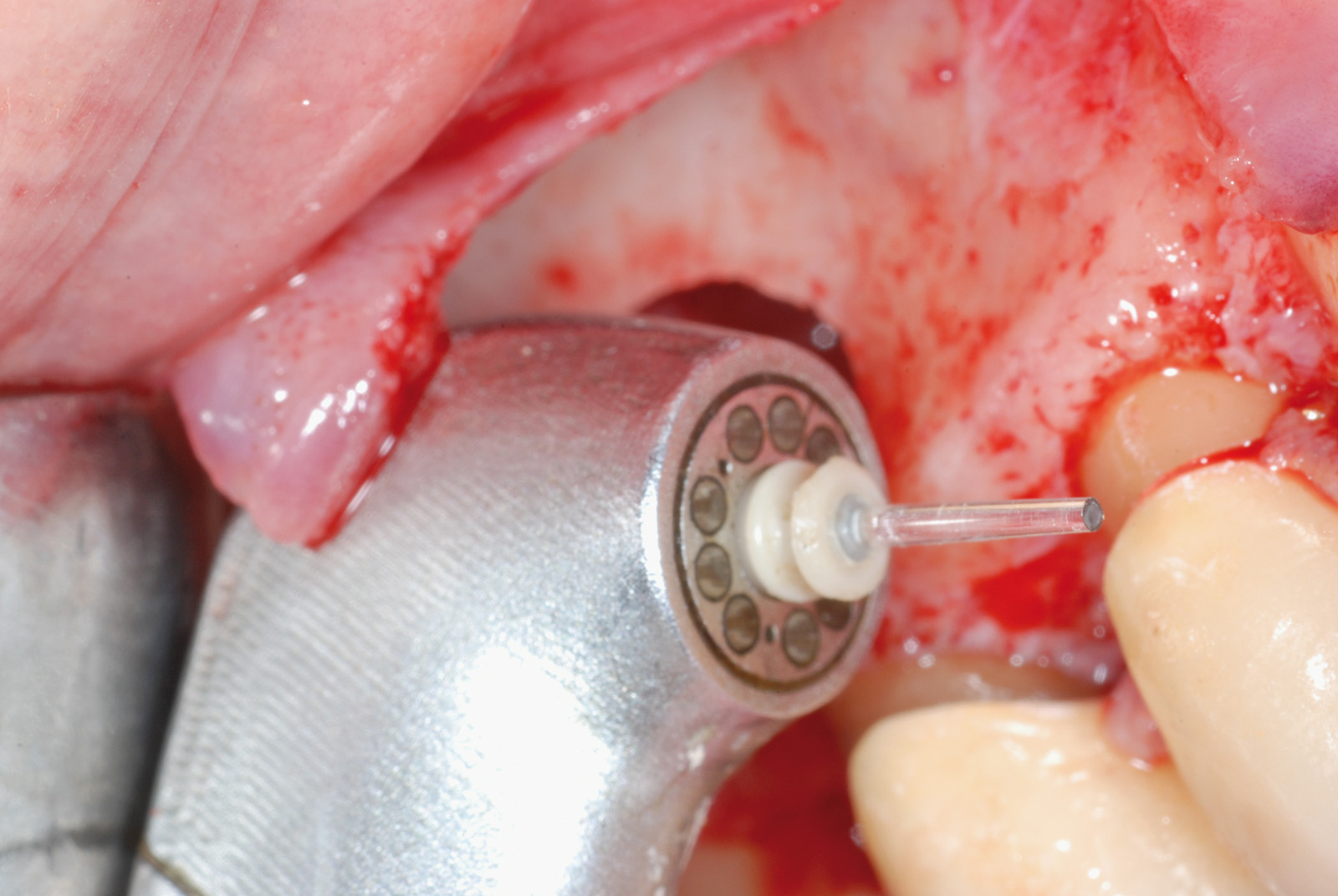
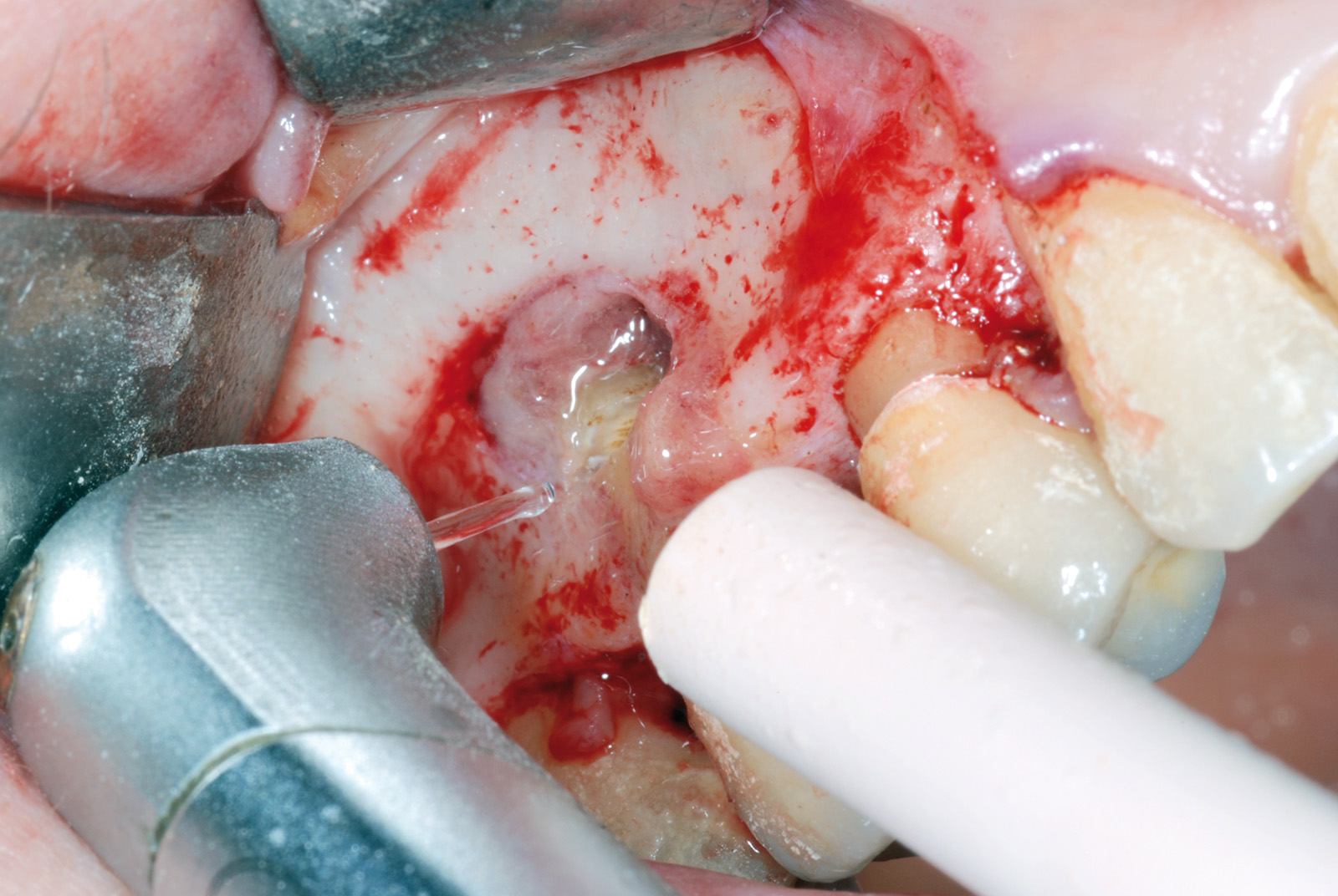
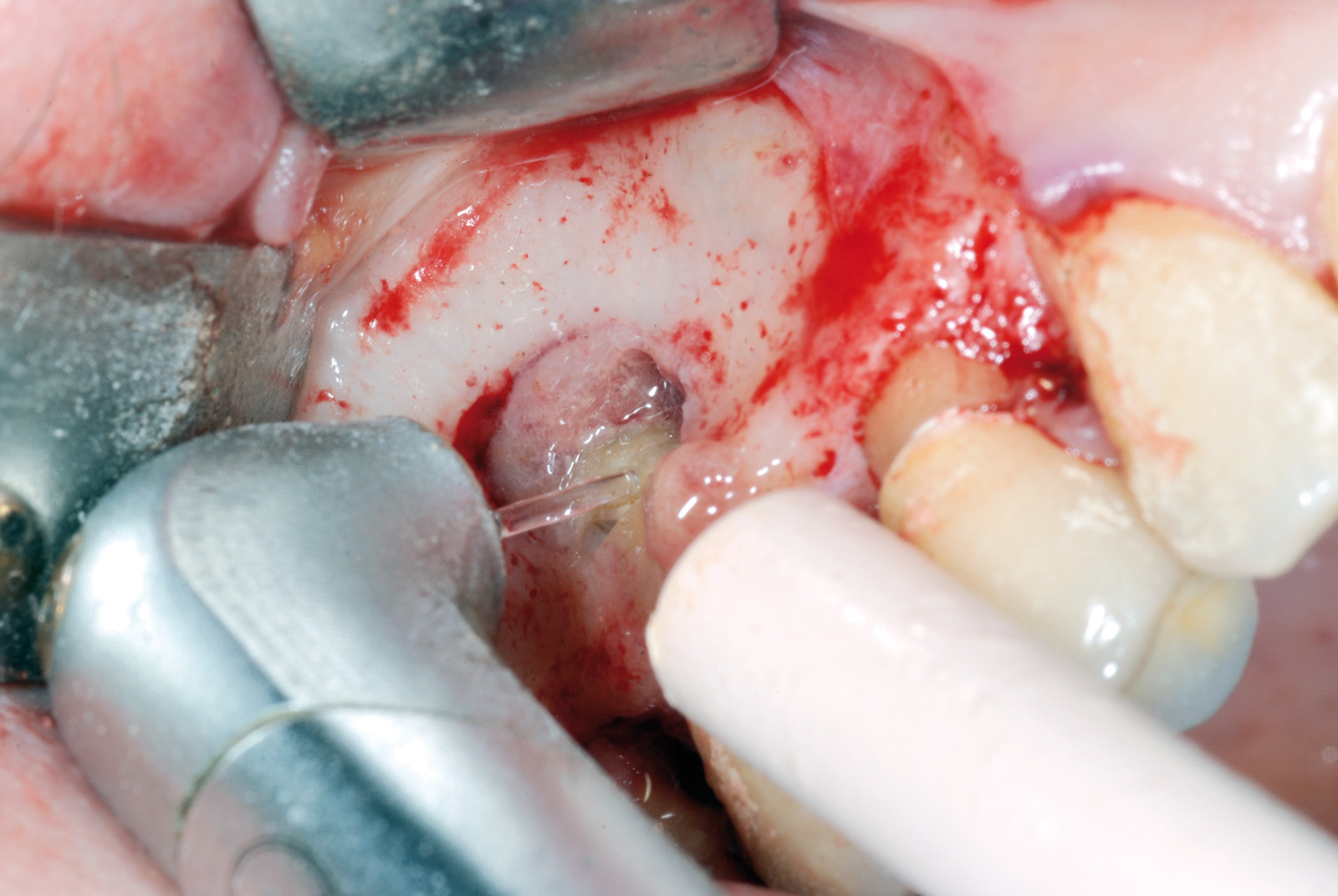
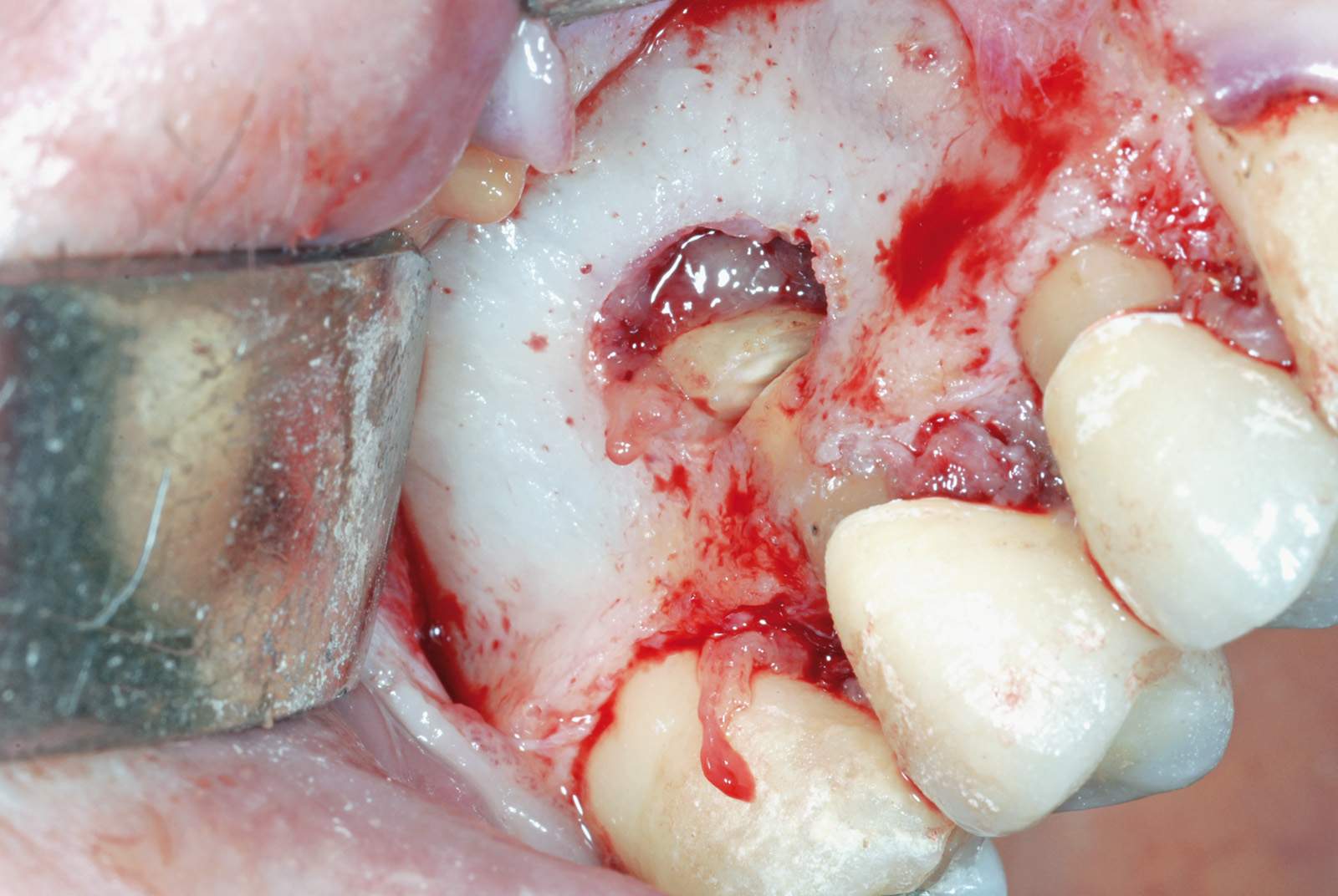
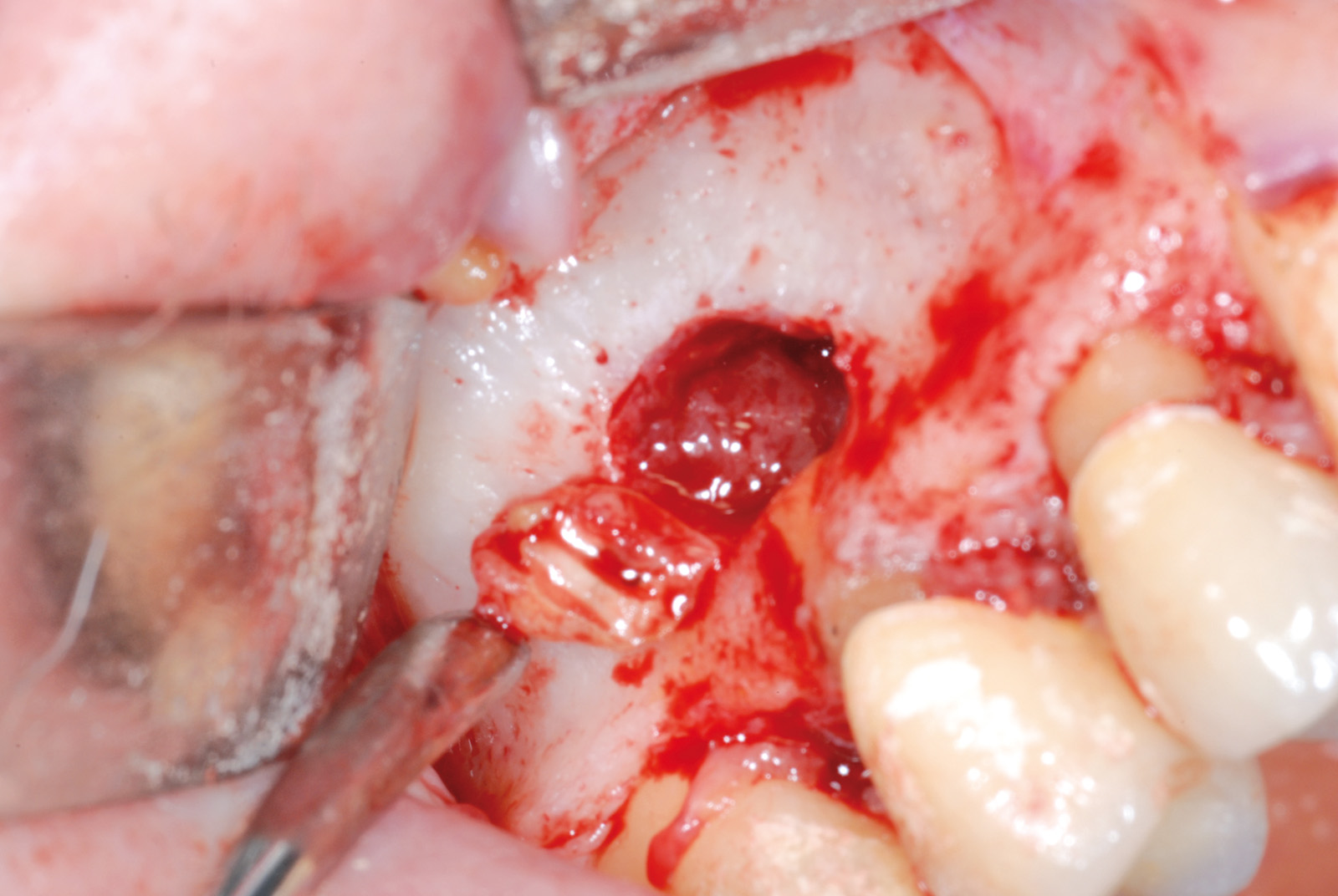
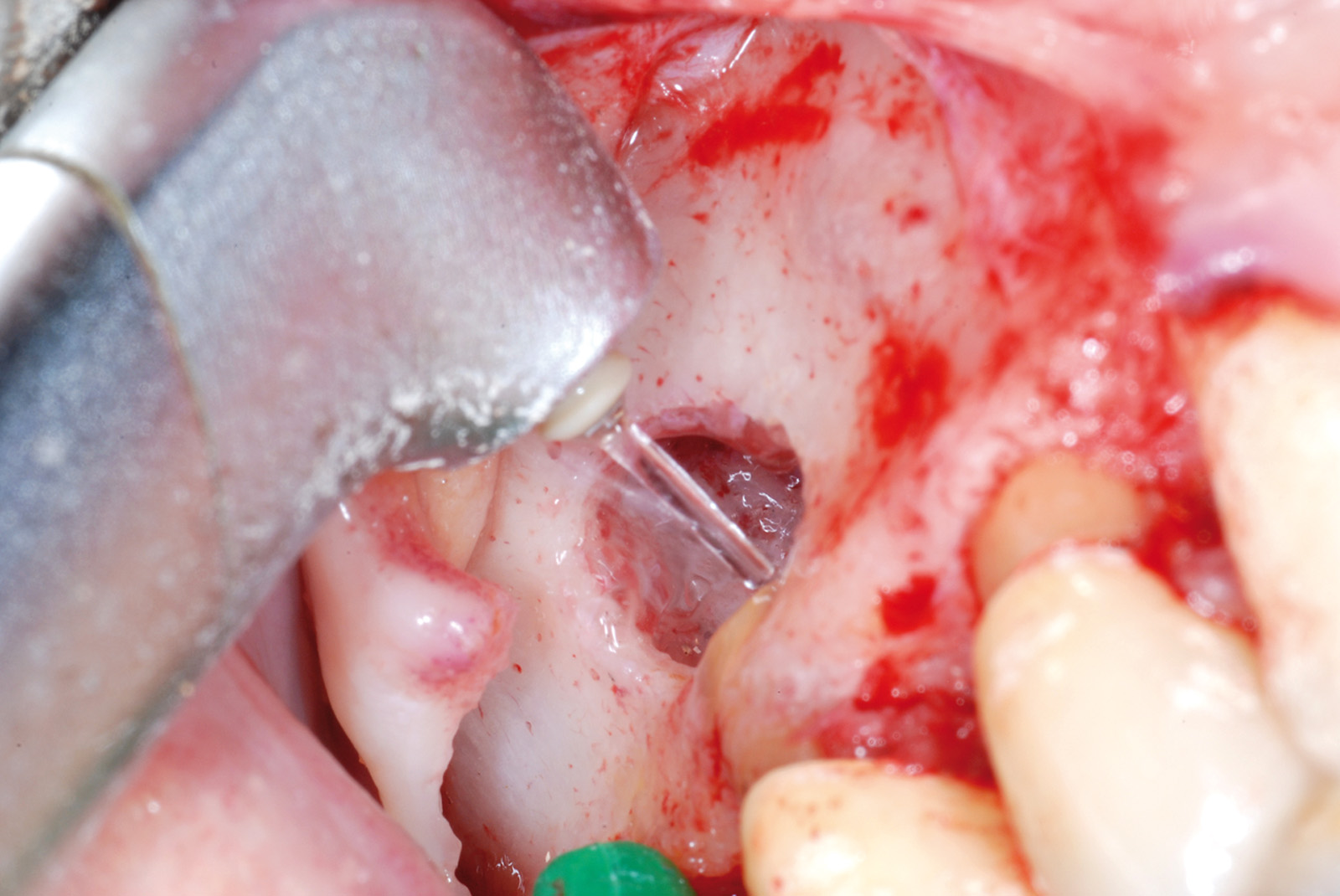
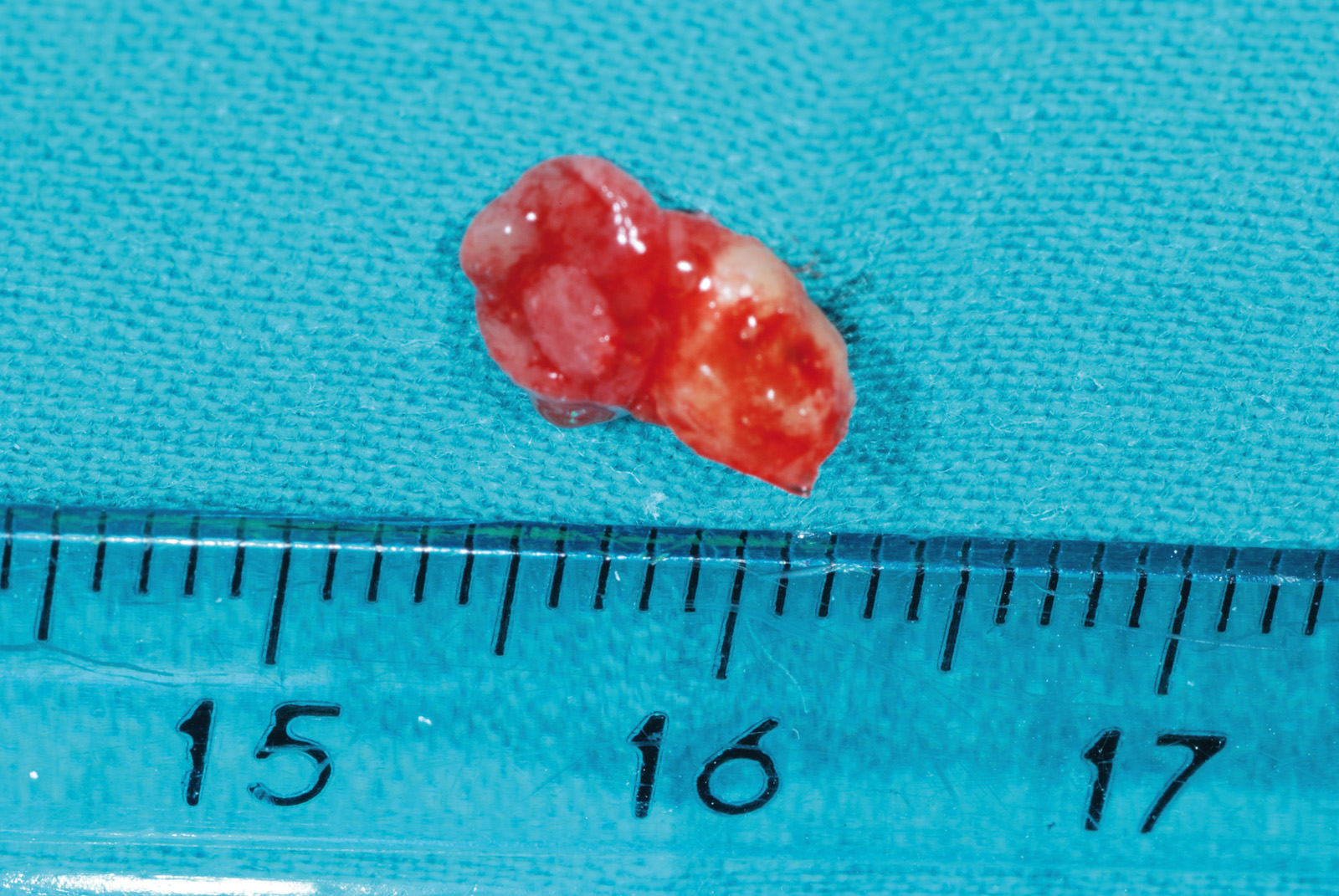
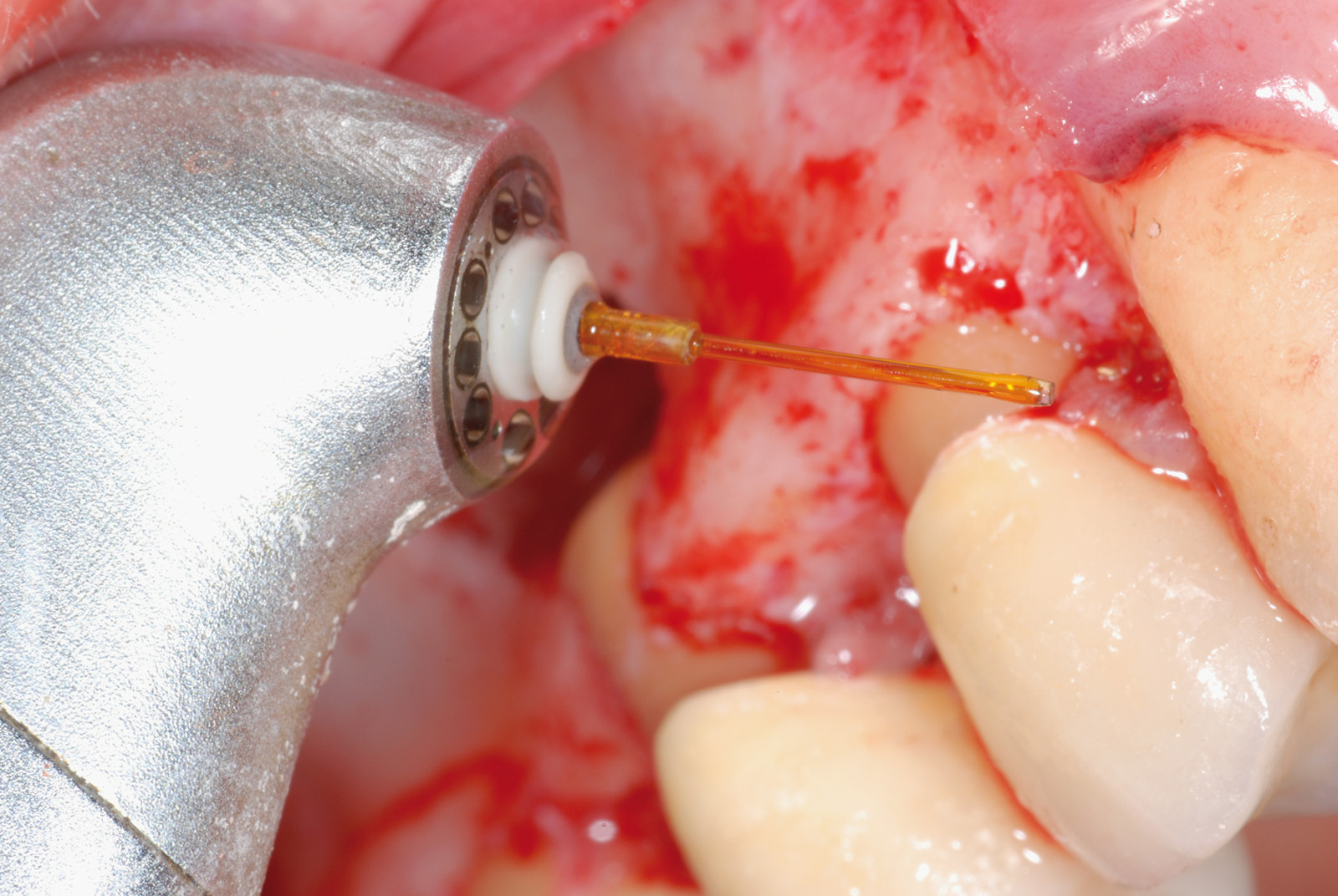
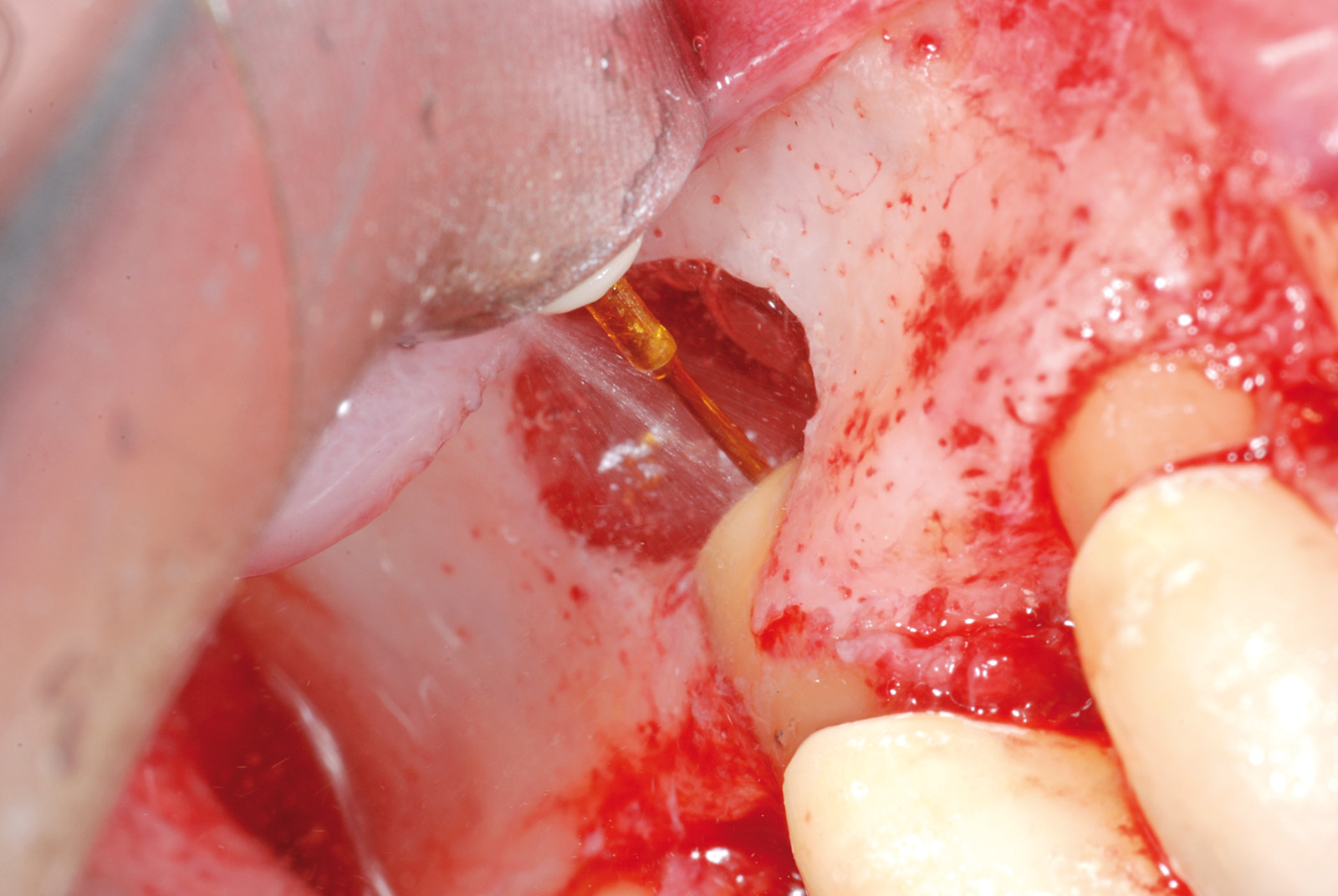
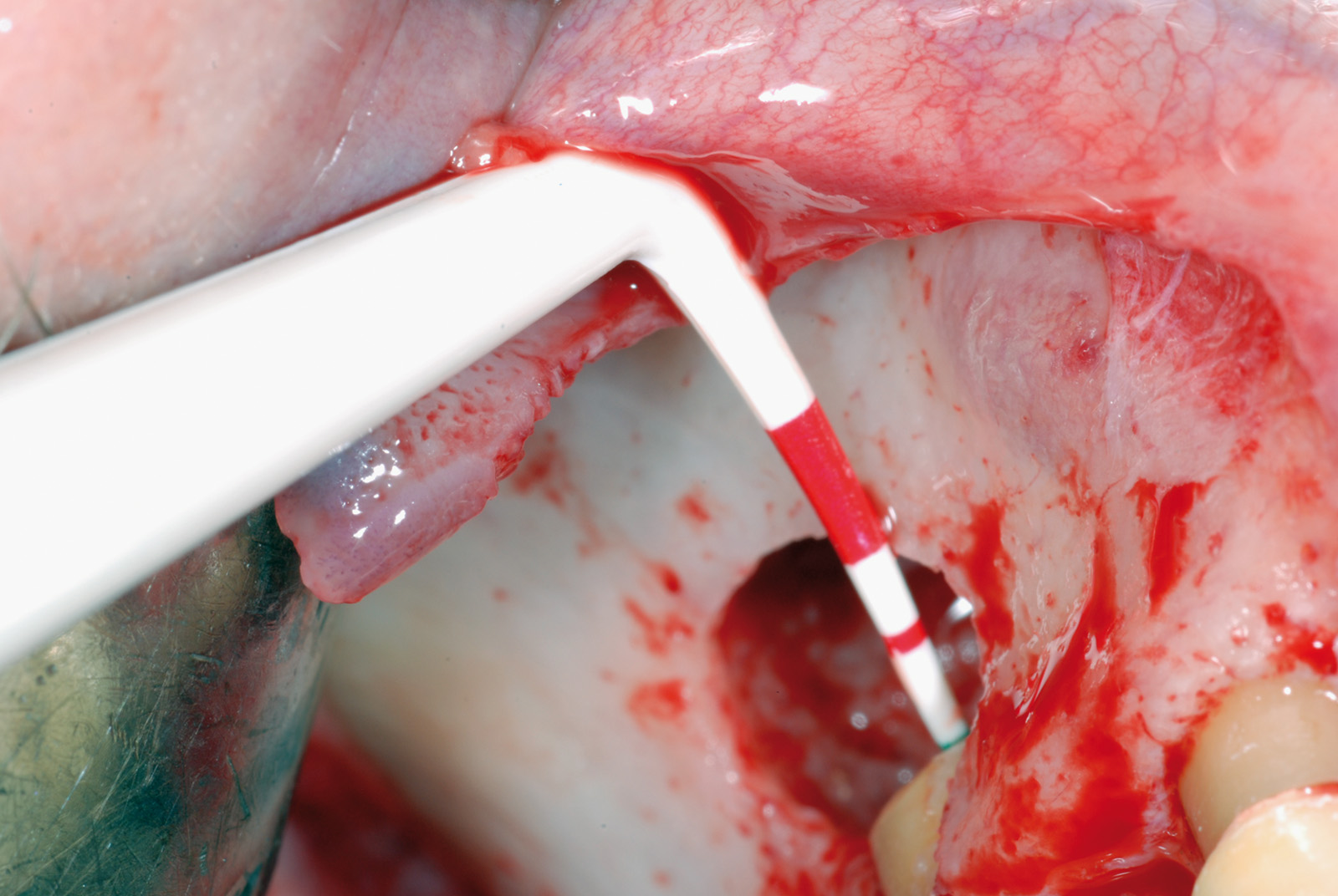
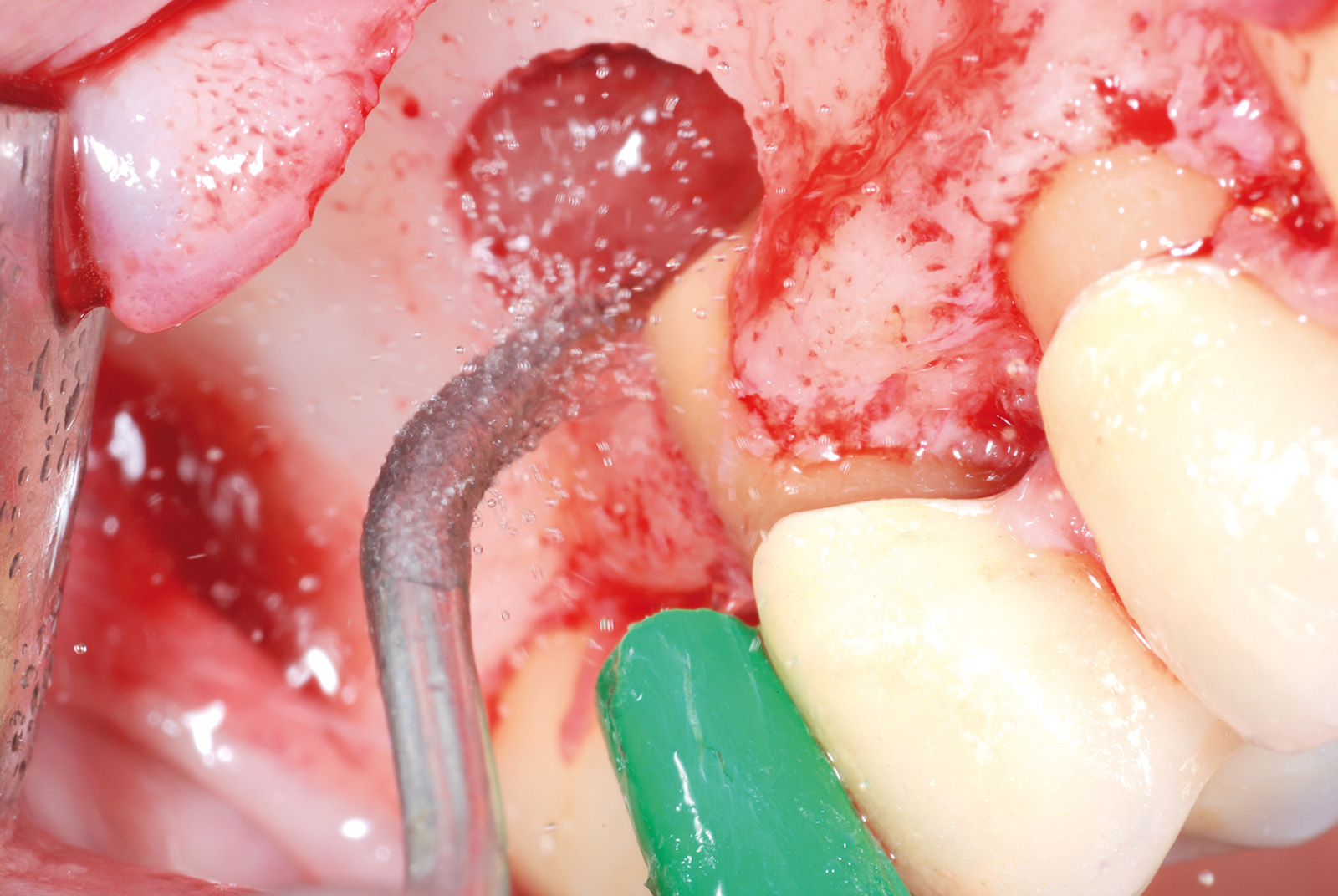
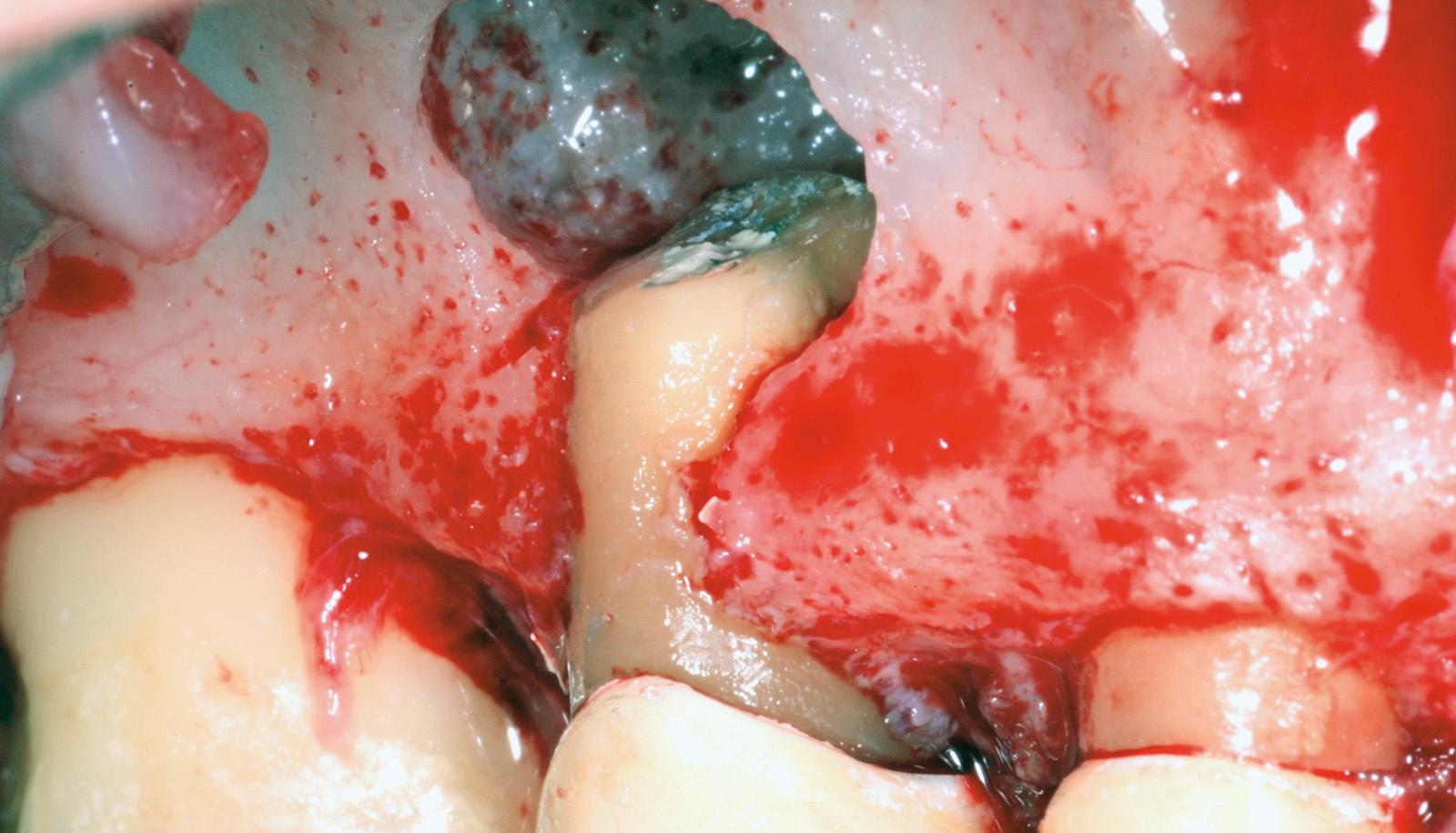
• Waterlase Biolase MD, ErCr:YSGG 2780 nm, conduzione in fibra ottica, manipolo curvo, tip MT4, lunghezza 6 mm da 400 micron tronco conica con i seguenti parametri: Apertura del lembo muco periosteo (figure 1, 2, 3, 4, 5, 6), Potenza 2,5 W, Frequenza 15 Hz, spray aria 60%, acqua 40%, modalità S (Soft tissue); Osteotomia e rimozione apice con tip MG6, lunghezza 6 mm, da 600 micron, Potenza 4.0 W, Frequenza 20 Hz, spray aria 55%, acqua 45% modalità H (Hard Tissue). Decontaminazione del canale con tip MZ3 da 320 micron, lunghezza 9 mm, Potenza 2.0W, spray aria 70%/acqua 30% (figure 7, 8, 9, 10, 11, 12, 13).
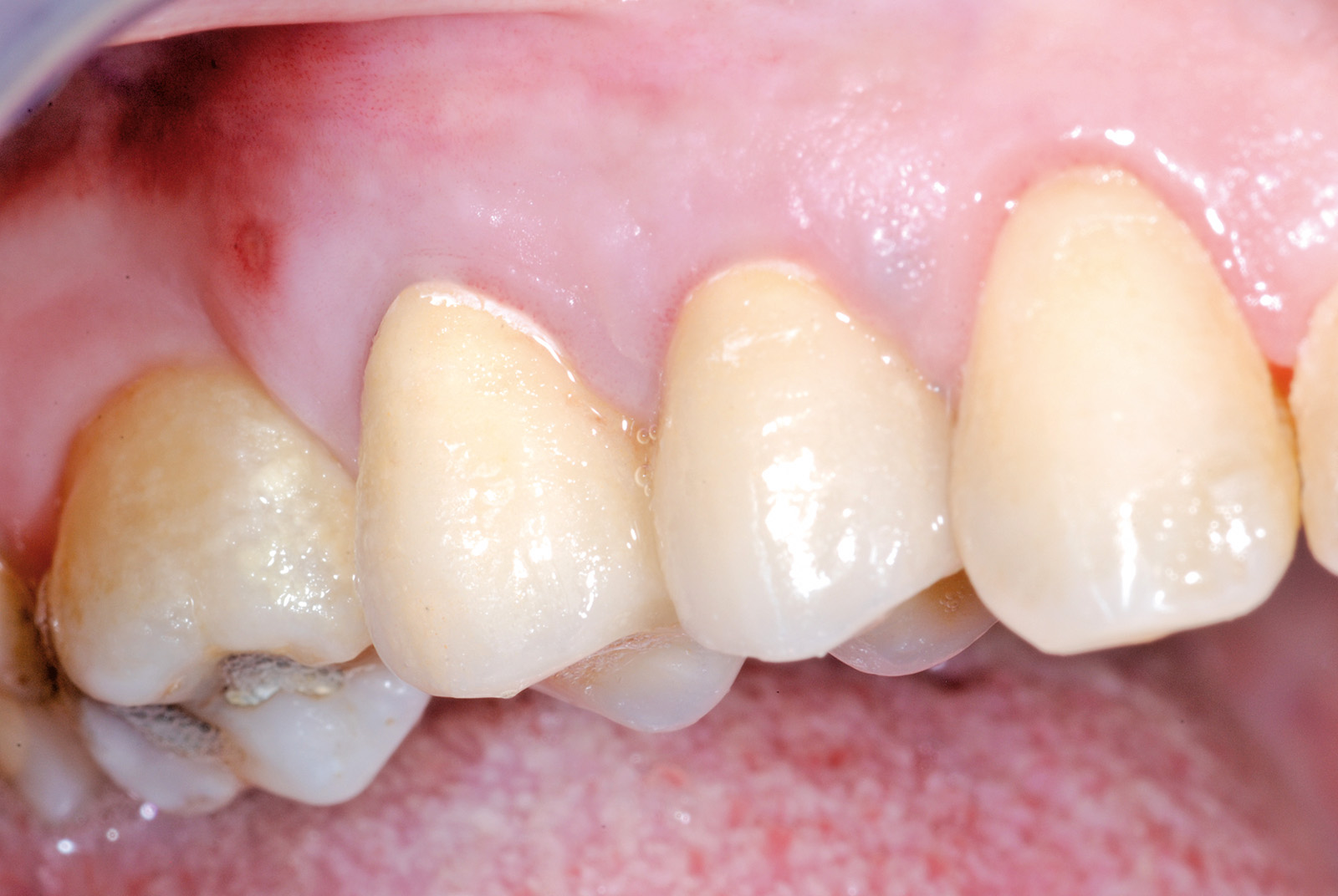
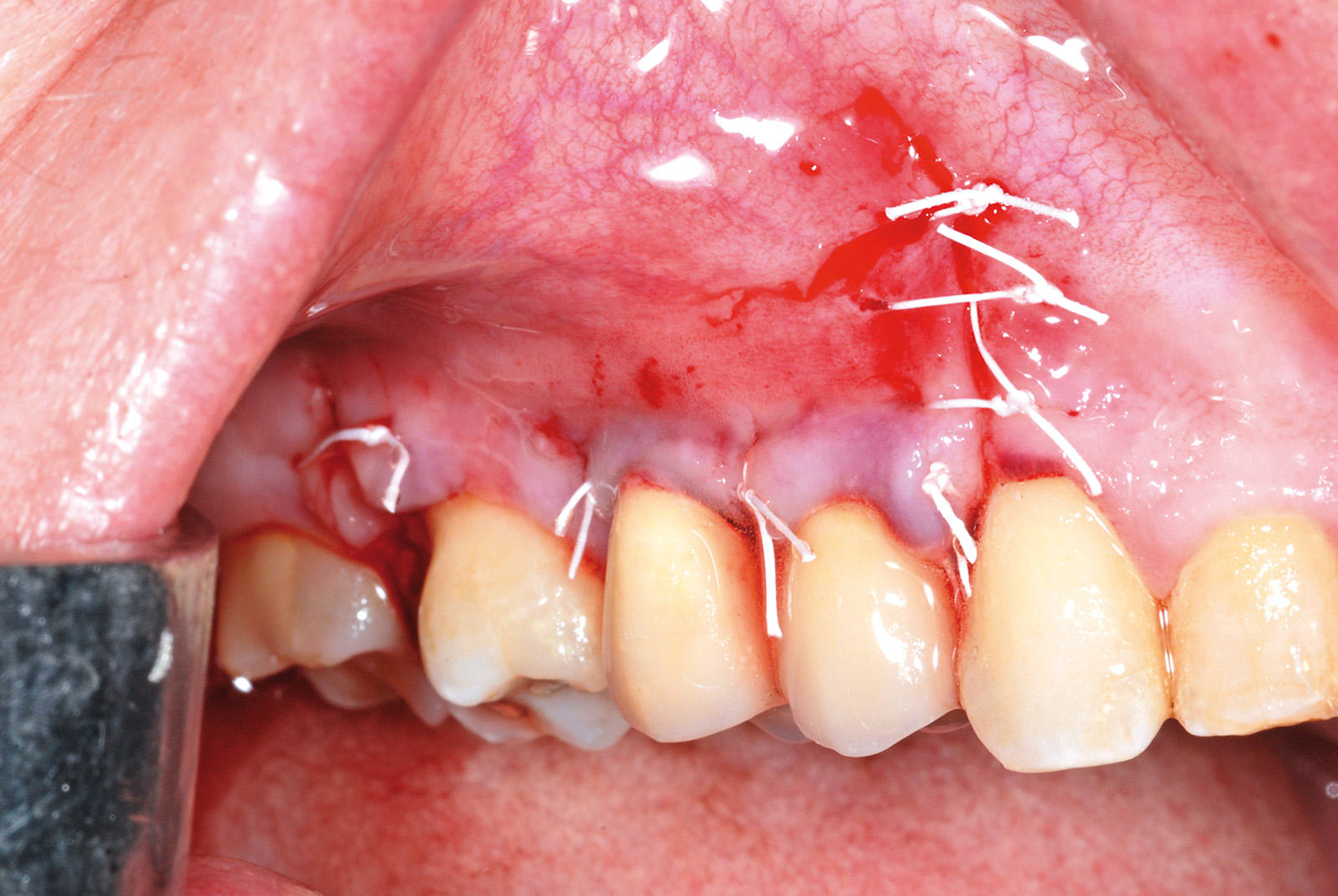
La decontaminazione del canale è stata eseguita mediante le tips stesse (quando l’anatomia lo permetteva) per una lunghezza minima di 3 mm dopo la resezione (misurata con sonda millimetrata) e, in caso di accesso sfavorevole e complesso, con manipolo a ultrasuoni (figure 14, 15, 16, 17). La decontaminazione dell’area osteotomica e periapicale è stata effettuata con il laser e nelle zone sottosquadrate e impossibili da raggiungere con punte ricurve a ultrasuoni e courettes chirurgiche. L’ultimo lavaggio dell’area infetta è stato eseguito mediante 20 ml di soluzione fisiologica (50%) e acqua ossigenata (50%) come adiuvante alla rimozione di eventuali altri detriti derivati dalle manovre chirurgiche. La sutura del lembo è stata realizzata con punti staccati con filo in seta intrecciata 3/0, ago v-5 Ethicon e con filo in PTFE 3/0, ago 3/8 Gore-tex (figure 18, 19).
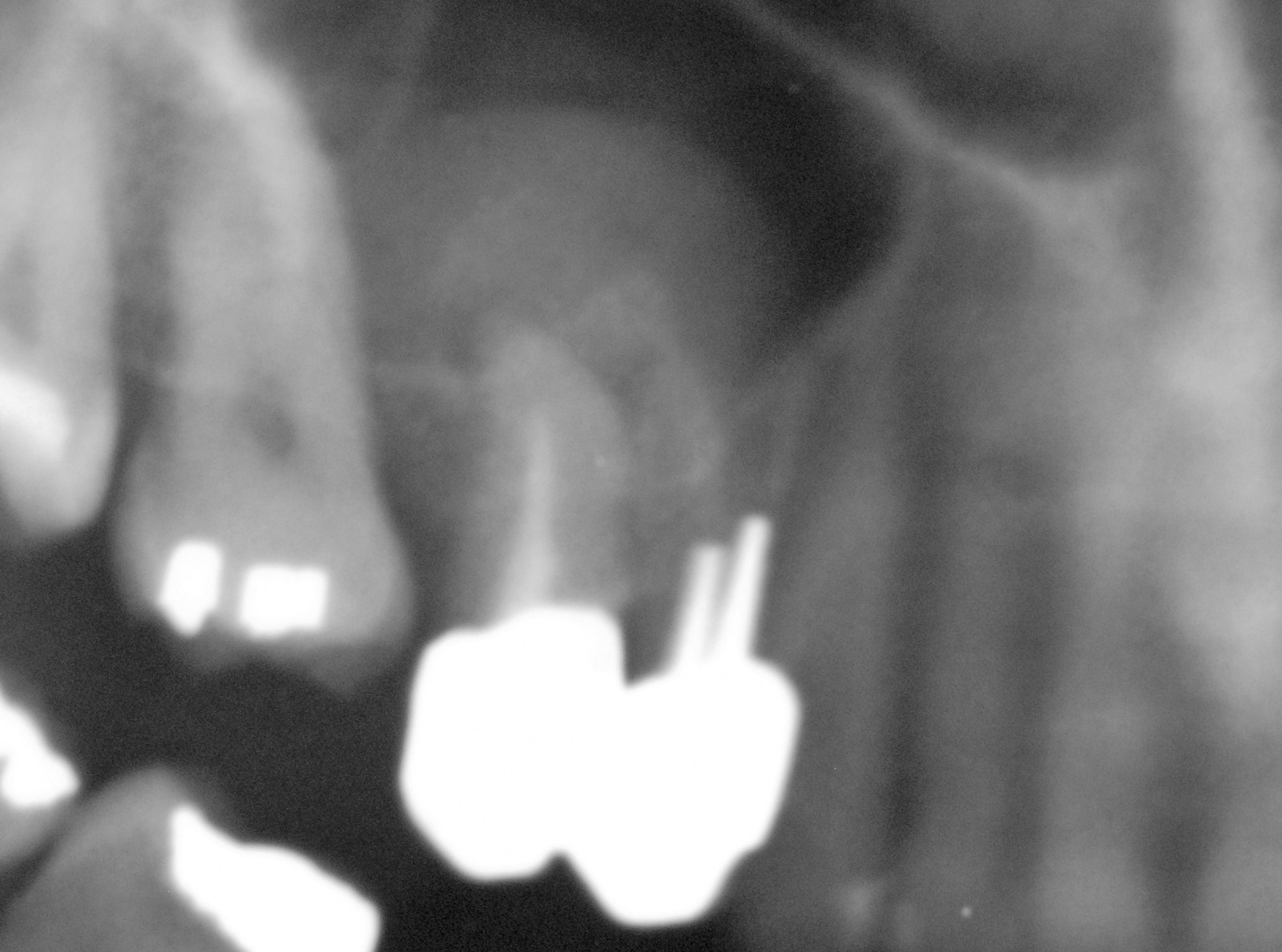
In 4 casi con lesione apicomarginale di classe I di Dietrich21, è stata posizionata una membrana riassorbibile Gore Resolut XTW1. Tutti gli apici resecati sono stati sigillati mediante cemento SuperEba Bosworth. I pazienti trattati sono stati monitorati mediante Rx ortopantomografia, Rx endorale pre-operatoria, Rx endorale post-operatoria (figura 20), Rx endorale a 3 mesi, a 6 mesi e a ogni anno dall’intervento chirurgico. Il trattamento farmacologico post-operatorio è stato effettuato attraverso somministrazione di Amoxicillina cp 1g, 2 cps al dì per 5 giorni o, nel caso di intolleranza alle penicilline, Spiramicina cp da 3.000.000 U, 2 cps al dì per 5 giorni oppure Azitromicina cp 500 mg, 1 cp al dì per 3 giorni. In tutti i casi è stata indicata l’applicazione sulla zona trattata di gel a base di clorexidina 0,2% con trays porta gel per 5 minuti 2 volte al dì per il periodo di permanenza della sutura chirurgica.
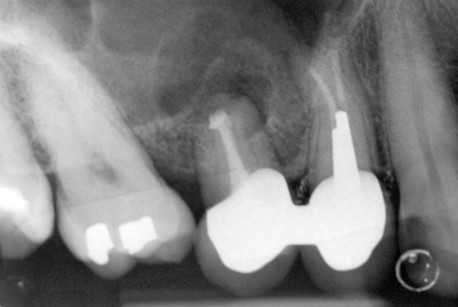
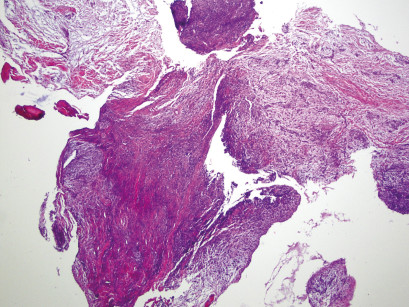
Risultati
Dei 45 casi oggetto dello studio solo in 6 si è verificato un insuccesso avvenuto in epoche diverse. Nel follow-up immediato si è constatata la formazione, in due casi di denti monoradicolati apicectomizzati, di una fistola al terzo medio radicolare curata con successo attraverso la decontaminazione e biostimolazione con laser a Diodi 980 nm, fibra da 320 micron, Potenza 2.0 W in modalità pulsata 50 ms On e 50 ms Off in un‘unica seduta, accompagnata da irrigazione nel tragitto fistoloso di polivinilpirrolidone iodio (1%), acqua ossigenata 12 Vol (50%) mista a soluzione fisiologica (50%). Nel follow-up a tre anni di distanza dall’apicectomia si sono verificate due recidive, seguite da reintervento, e una frattura dell’elemento 46, oggetto di doppia apicectomia su entrambe le radici e, quindi, sostituito dopo 9 mesi con due impianti in titanio. Nel follow-up dopo i 5 anni si è verificata la frattura della radice apicectomizzata con successiva perdita del dente monoradicolato al primo quadrante apicectomizzato. In tutti gli altri casi si è avuta un’ottima guarigione.
Discussione
Dopo che Weichman & Johnson nel 197131 per primi hanno dimostrato la possibilità di utilizzo del laser in endodonzia, numerosi studi sono stati condotti sul tipo e sulle modalità di uso del laser stesso nella sterilizzazione dei canali radicolari 24-25. A tal proposito si ricordano i laser a CO26-30, il laser Nd:YAG7-8, il laser XeCl7, il laser a diodi17, l’Er:YAG laser10,18,19 e l’Nd:YAP laser28, tutti dotati anche di un notevole potere battericida, evidenziato a potenze diverse in ogni singolo tipo di laser. Nel 1983 Eriksson & Albrektsson29 hanno introdotto un altro concetto indispensabile per un corretto uso del laser e per avere quindi un successo nel suo impiego sul tessuto osseo. Infatti i due studiosi hanno focalizzato l’attenzione sul fatto che l’osso sottoposto a trattamento con laser non deve subire, per la sua sopravvivenza, un riscaldamento superiore ai 47 °C per 1 minuto e che potenze troppo elevate possono causare insulti termici danneggiando anche il tessuto parodontale, fenomeno che viene evitato con l’uso della modalità pulsata. Essendo differenti le peculiarità specifiche di ogni tipo di laser5, si è potuto osservare che l’Er:YAG determina superfici radicolari lisce, prive di impurità e di zone di carbonizzazione, condizione che si realizza, ovviamente, con modalità pulsata a livelli energetici tra 50 e 90 mJ. Inoltre, il laser Er:YAG rimuove meglio lo smear layer rispetto all’Nd:YAG, mentre quest’ultimo esalta il potere antinfiammatorio riducendo l’infiltrazione batterica all’interno di radici sezionate dopo apicectomia e otturazione retrograda7-9 e, inoltre, appare specifico per questo tipo di intervento essendo dotato di una fibra ottica di trasporto molto sottile.
Queste caratteristiche apportano un valido aiuto nella terapia endodontica ortograda tradizionale e proprio per questo motivo viene consigliato nella suddetta terapia. Valutando le caratteristiche dei vari tipi di laser, l’Er:YAG risulta essere il più adatto per la resezione radicolare e l’apicectomia migliorando la guarigione e aumentando la compliance post-operatoria5-19, dopo che nel 1988 Miserendino6 aveva tentato di effettuare delle resezioni apicali con il laser CO2 senza ottenere il successo sperato. Sebbene nel laser Er:YAG (350 mJ e 6 Hz) la velocità di taglio sia leggermente inferiore ai metodi chirurgici tradizionali (strumenti rotanti), nella sua applicazione clinica riduce il rischio di contaminazione del sito chirurgico e il rischio di trauma dei tessuti adiacenti18-20. Inoltre con questo tipo di laser la preparazione della cavità retrograda è significativamente più rapida e più netta che con gli ultrasuoni, mentre non si dimostrano differenze significative nella sigillatura delle cavità retrograde preparate19,20. Sembra doveroso ricordare che nell’apicectomia gestita sia con laser Er:YAG che con Nd:YAG uno studio condotto sia al microscopio elettronico a scansione (SEM) che al microscopio ottico tradizionale ha dimostrato che la migliore sigillatura apicale avviene utilizzando il primo per l’apicectomia e il secondo per la preparazione della retrocavità, ottenendo così una riduzione della permeabilità dentinale11. Da quanto sinora scientificamente evidenziato appare chiaro che l’utilizzo della chirurgia laser assistita aumenta la gamma di approcci terapeutici nell’ambito del trattamento endodontico retrogrado5-23.
Conclusioni
Tutte le fasi che caratterizzano la chirurgia endodontica (incisione mucosa, osteotomia, resezione apicale, preparazione cavitaria) sono eseguibili in luce laser. In particolare alcuni laser a Erbio dispongono di terminali flessibili di varia lunghezza che permettono la pulizia del canale per alcuni millimetri con effetto paragonabile a quello degli ultrasuoni utilizzati per la detersione dei canali dopo la loro resezione22-24. La chiusura dei canali detersi è eseguibile utilizzando i più comuni sigillanti con particolare riferimento ai cementi SuperEba3-25. I vantaggi per l’operatore nell’utilizzare i laser ad Erbio per le apicectomie sono quelli di operare in un campo esangue, decontaminato e ricco degli effetti della biostimolazione tessutale generata dalla luce laser5. I vantaggi per il paziente sono legati a una riduzione dei disagi causati dalla vibrazione delle frese, a una guarigione più rapida e alla formazione di un edema post-operatorio significativamente ridotto e alla luce delle evidenze scientifiche si può affermare che l’utilizzo della chirurgia laser assistita aumenta la gamma di approcci terapeutici nell’ambito del trattamento endodontico retrogrado5-23.
Corrispondenza
Rolando Crippa
rolcrip@tin.it
Bibliografia
1. Siqueira JF Jr, Lopes HP. Bacteria on the apical root surfaces of untreated teeth with periradicular lesions: a scanning electron microscopy study. International Endodontic Journal 2001;34:216-20.
2. Ferreira FBA, Ferreira AL, Gomez BPFA, Souza-Filjo FJ. Resolution of persistent periapical infection by endodontic surgery. International Endodontic Journal 2004;37:61-69.
3. Gagliani MM, Gorni, FGM, Strohmenger L. Periapical resurgery versus periapical surgery: a 5-year longitudinal comparison. International Endodontic Journal 2005;38:320-327.
4. Sundqvist G, Figdor D, Persson S, Sjogren U. Microbiologic analysis of teeth with failed endodontic treatment and the outcome of conservative re-treatment. Oral Surgery, Oral Medicine and Oral Pathology 1998;85:86-93.
5. Reyhanian A, Parker S, Moshonov J. The use of the erbium Yttrium Aluminium garnet (2,940 nm ) in a laser-assisted apicectomy procedure. Br Dent J 2008 Sep 27;205(6):319-23.
6. Miserendino LJ. The laser apicectomy: endodontic application of the CO2 laser for pariapical surgery. Oral Surgery Oral Medicine Oral Pathology Oral Radiolog and Endodontics 1988; 66:615-9.
7. Stabholz A, Khayat A, Weeks DA, Neev J, Torabinejad M. Scanning electron microscopic study of the apical dentine surfaces lased with Nd:YAG laser following apicectomy and retrofill. International Endodontic Journal 1992; 25:288-91.
8. Stabholz A, Khayat A, Ravenshad SH, McCarthy DW, Neev J, Torabinejad M. Effects of Nd:YAG laser on apical seal of teeth after apicoectomy and retrofill. Journal of Endodontics 1992;18:371-5.
9. Wong WS, Rosemberg PA, Boylan RJ, Schulman A. A comparison of the apical seals achieved using retrograde amalgam fillings and the Nd:YAG laser. Journal Of Endodontics 1994;20:595-7.
10. Paghdiwala AF. Root resection of endodontically treated teeth by Erbium:Yag laser radiation. Journal Of Endodontics 1993;19:91-4.
11. Oliveira RG, Gouw-Soares S, Baldochi SL, Eduardo CP. Scanning electron microscopy (SEM) and optical microscopy: effects of Er:YAG and Nd:YAG lasers on apical seals after apicoectomy and retrofill. Photomed Laser Surg 2004;22:533-6.
12. Danin J, Stromberg T, Forsgren H, Linder LE, Ramskold LO. Clinical management of nonhealing periradicular pathosis. Surgery versus endodontic retreatment. Oral Surgery Oral Medicine Oral Pathology Oral Radiolog and Endodontics 1996;82:213-7.
13. Del Fabbro M, Taschieri S, Testori T, Francetti L, Weinstein RL. Surgical versus non-surgical endodontic re-treatment for periradicular lesions. Cochrane Database Syst Rev 2007 Jul 18;(3):CD005511.
14. Bosnev Ivan Hiristov. Terminologia Stomatologica Polyglotta. Dizionario odontostomatologico in otto lingue, Elsevier, 1991.
15. Harnisch H. Apicectomia. Milano: Scienza e tecnica dentistica, 1981.
16. Barnes M. Apicectomia. Milano: Scienza e Tecnica dentale, 1986.
17. Moritz A, Schoop U, Goharkhay K, et al. The bactericidal effect of Nd:YAG, Ho:YAG and Er:YAG laser irradiation in the root canal: an in vitro comparison. J Clinic Laser Med Surg 1999;17(4):161-64.
18. Komori T, Yokoyama K, Takato T, Matsumoto K. Clinical application of the Erbium:YAG laser for apicoectomy. J Endod 1997 Dec;23(12):748-50.
19. Komori T, Yokoyama K, Matsumoto Y, Matsumoto K. Erbium:YAG and Holmium:YAG laser root resection of extracted human teeth. J Clin Laser Med Surg 1997 Feb;15(1):9-13.
20. Francischone CE, Padovan LA, Padovan LE, Duarte MA, Fraga Sde C, Curvello VP. Apicectomy with the Er:YAG laser or bur, followed by retrograde root filling with zinc oxide/eugenol or sealer 26. Photomed Laser Surg 2005 Aug;23(4):395-8.
21. Karlovic Z, Pezelj-Ribaric S, Miletic I, Jukic S, Grgurevic J, Anic I. Erbium:YAG laser versus Ultrasonic in Preparation of Root-End Cavities. J Endod 2005 Nov;31(11):821-823.
22. Dietrich T, Zunker P, Dietrich D, Bernimoulin JP. Apicomarginal defects in periradicular surgery: classification and diagnostic aspects. Oral Surg Oral Med Oral Path Oral Radiol Endod 2002;94:233-239.
23. Rahimi S, Yavari HR, Shahi S, Zand V, Shakoui S, Reyhani MF, Pirzadeh A. Comparison of the effect of Er, Cr-YSGG laser and ultrasonic retrograde root-end cavity preparation on the integrity of root apices. J Oral Sci 2010;52(1):77-81.
24. Kimura Y, Wilder-Smith P, Matsumoto K. Laser in endodontics: a review. International Endodontic Journal 2000;33:173-185.
25. George R, Walsh LJ. Thermal effects from modified endodontic laser tips used in the apical third of root canals with erbium-doped yttrium aluminium garnet and erbium, chromium-doped yttrium scandium gallium garnet lasers. Photomed Laser Surg 2010 Apr;28(2):161-5.
26. Baek SH, Lee WC, Setzer FC, Kim S. Periapical bone regeneration after endodontic microsurgery with three different root-end filling materials: amalgam, SuperEBA, and mineral trioxide aggregate. J Endod 2010 Aug;36(8):1323-5.
27. Benedicenti S, Cassanelli C, Signore A, Ravera G, Angiero F. Decontamination of root canals with the gallium-aluminum-arsenide laser: an in vitro study. Photomed Laser Surg 2008 Aug;26(4):367-70.
28. Blum JY, Michailesco P, Abadie MJ. An evaluation of the bactericidal effect of the Nd:YAP laser. J Endod 1997 Sep;23(9):583-5.
29. Eriksson AR, Albrektsson T. Temperature threshold levels for heat-induced bone tissue injury: a vital-microscopic study in the rabbit. J Prosthet Dent 1983 Jul;50(1):101-7.
30. Bader G, Lejeune S. Prospective study of two retrograde endodontic apical preparations with and without the use of CO2 laser. Endod dent Traumatol 1998 Apr;14(2):75-8.
31. Weichman JA, Johnson FM. Laser use in endodontics. A preliminary investigation. Oral Surg Oral Med Oral Pathol 1971 Mar;31(3):416-20.








Maravillo post. Gracias por compartirlo…Espero màs…
Saludos