Riassunto
Il presente lavoro si prefigge di fornire un quadro sintetico e di immediata applicazione pratica di quelle nozioni e linee-guida che consentono di effettuare una efficace anestesia locale nel paziente pediatrico. L’anestesia rappresenta il momento più stressante della seduta odontoiatrica sia per il bambino sia per l’operatore e un eventuale insuccesso nel controllo del dolore pregiudica tutti gli step successivi della terapia. Le conoscenze e l’abilità tecnica dell’odontoiatra sono importanti al pari di un delicato approccio psicologico al piccolo paziente, la cui collaborazione deve essere talvolta conquistata e faticosamente mantenuta durante tutta la seduta. Verranno analizzate le più importanti variabili che differenziano la pratica dell’anestesia locale nel bambino da quella nell’adulto. È auspicabile che ogni odontoiatra sia in grado di ottenere risultati predicibili e costanti e che l’anestesia locale nel bambino possa essere impiegata routinariamente come avviene nell’adulto.
Il controllo del dolore nel paziente pediatrico rappresenta per l’odontoiatra un obiettivo delicato e complesso quanto fondamentale al fine di poter attuare una terapia corretta ed efficace1,2. I soggetti pediatrici che riferiscono esperienze dolorose nel setting odontoiatrico hanno un’elevata probabilità di sviluppare una negligenza o un rifiuto nella cura del cavo orale in età adulta2,3. L’anestesia locale (A.L.) in odontoiatria infantile acquista pertanto un’importanza particolare e presenta alcuni aspetti peculiari che la contraddistinguono dall’A.L. nell’adulto. Se nel trattamento di pazienti adulti l’A.L. è ormai considerata una pratica banale e meccanica, questo non vale per il bambino e la sua esecuzione richiede un approccio psicologico più delicato e attento. La causa di ciò risiede nella natura contraddittoria e quasi paradossale dell’A.L., che è un atto chirurgico e di per sé traumatico finalizzato all’abolizione di un più marcato e prolungato discomfort durante la terapia vera e propria. Mentre l’adulto è in grado di accettare razionalmente il trauma legato all’iniezione (seppur con reazioni emotive molto variabili) e anzi generalmente richiede espressamente l’A.L. ben conoscendo per precedenti esperienze l’estrema reattività del cavo orale alle manovre odontoiatriche, il bambino non è in grado di contestualizzare l’evento “iniezione” in termini di durata e di rapporto costo/beneficio, opponendo in genere un più o meno marcato rifiuto. A questa mancanza di compliance da parte del piccolo paziente si aggiunge lo stress prodotto nell’operatore dal dover effettuare una manovra dolorosa che inconsciamente contrasta con l’istinto di protezione che l’adulto nutre nei confronti del bambino; studi dimostrano che lo stress da iniezione è maggiore nel dentista che nel piccolo paziente. Numerosi fattori influenzano e caratterizzano l’impatto emotivo, la traumaticità, l’efficacia e quindi il successo dell’A.L. in odontoiatria infantile e devono pertanto essere ben noti all’operatore; essi possono essere suddivisi in fattori legati al paziente (tabella 1) e fattori relativi all’operatore in termini di tecniche, strumentario e gestione del piccolo paziente (tabella 2). Valutiamo di seguito analiticamente i fattori che possono influenzare l’efficacia dell’A.L. nel trattamento del paziente pediatrico.
Particolarità anatomiche del bambino
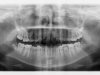
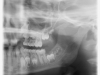
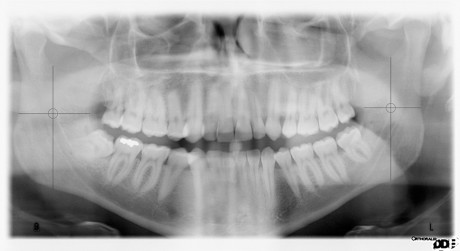
I mascellari del bambino presentano dimensioni ridotte rispetto all’adulto e si dovranno pertanto superare le difficoltà di accesso e visibilità derivanti dal maggior ingombro della siringa. Rispetto all’adulto, le corticali dei mascellari sono più sottili e attraversate da un maggior numero di canalicoli vascolari, cosa che rende l’infiltrazione plessica quasi sempre sufficiente per perseguire l’anestesia dei denti decidui e permanenti del bambino, anche in sede mandibolare. A tale scopo, occorre tener presente che le radici dei denti decidui sono relativamente corte e pertanto la sede dell’iniezione dovrà essere più coronale rispetto a quella indicata per i denti permanenti. In caso di terapie endodontiche o exodontiche a carico dei molari inferiori sarà tuttavia talvolta necessario ricorrere ad anestesia tronculare del n. alveolare inferiore: in questo caso è necessario sapere che nel bambino la spina di Spix è situata al di sotto del piano occlusale mandibolare e non al di sopra, pur mantenendo durante la crescita una posizione intermedia tra i margini anteriore e posteriore della branca ascendente (figure 1e 2). In caso sia richiesto il blocco del n. infraorbitario, occorre fare attenzione all’estrema sottigliezza e fragilità della parete anteriore del mascellare superiore.
Particolarità metaboliche e fisiologiche
Il bambino possiede un metabolismo più rapido rispetto all’adulto ed è logico pertanto aspettarsi una minore emivita del farmaco iniettato. Inoltre, dato il minor volume di fluidi corporei, il divario tra dose terapeutica e dose tossica di anestetico si restringe4. In ogni caso sarà necessario evitare di superare, per ogni 15 kg di massa corporea , la dose di 2 tubofiale da 1,8 ml di carbocaina 2% per seduta e per giorno. Da evitare mediante adeguate prove di aspirazione sarà il rischio di iniezione intravasale, frequente causa di tossicità a livello nervoso centrale e cardiaco. Per quanto riguarda la fase di permuta, gli studi condotti da Zerosi hanno dimostrato come anche in fase avanzata di riassorbimento delle radici dei denti decidui (stadi 2º o 3º di Fortier) i residui di polpa camerale possono mantenere la vitalità e richiedere pertanto un’adeguata somministrazione di A.L.5. Infine, proprio per la stretta contiguità del germe del permanente e delle radici del predecessore deciduo è da sconsigliarsi in modo assoluto l’anestesia intraligamentosa a carico dei decidui, per il rischio di provocare ipoplasie dello smalto o altri effetti collaterali a carico del permanente in formazione (figura 3).
Età
L’età del piccolo paziente non influisce sulla procedura di A.L. solo per le peculiarità anatomiche che esprime, ma anche in quanto essa è in genere direttamente proporzionale al grado di collaborazione offerto all’operatore durante le manovre.
A differenza dell’età, il sesso del paziente
non sembra giocare un ruolo importante nella sua predisposizione e reazione al trauma dell’iniezione, come riportato da Ram e Peretz6,7, Allin et al.8, Nakai et al.1 e Naser et al.9, i cui studi dimostrano l’assenza di una differenza sesso-specifica statisticamente significativa.
Livelli di ansia
Il comportamento del bambino e la sua attitudine a sottoporsi alle cure odontoiatriche sono classificati in base alla Scala di Frankl10 in 4 categorie:
• decisamente negativo (rifiuto del trattamento, pianto forzato, paura o altre chiare manifestazioni di estrema negatività);
• negativo (riluttanza ad accettare il trattamento, non cooperazione, qualche manifestazione di rifiuto ma non conclamata);
• positivo (accettazione del trattamento, cooperazione a volte cauta ma desiderio di accondiscendere con l’operatore);
• decisamente positivo (buon rapporto con il dentista, riso e contentezza, interesse
verso le procedure terapeutiche).
Per poter valutare tale livello di ansia è consigliabile attuare in prima seduta, o comunque sino a quando non sia consolidata la cooperazione del paziente, soltanto procedure non traumatiche, come ad esempio l’applicazione topica di fluoro o l’esecuzione di sigillature.
Tipo di patologia in atto e sua sintomaticità
Per quanto riguarda il tipo di terapia
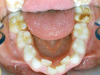
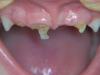
richiesta dalla lesione in esame, vari studi concordano nel considerare meno efficace il controllo del dolore in caso di cure endodontiche o exodontiche rispetto alle cure conservative1 (figure 4-6). La presenza di sintomatologia dolorosa rende in genere più difficile l’approccio dell’odontoiatra in quanto innesca nel bambino un istinto di autodifesa a tutela della regione interessata , e ogni tentativo di approccio da parte del medico può essere spesso respinto con decisione. Ciò può richiedere un intenso sforzo di convincimento circa la funzione benefica del proprio intervento, e a maggior ragione l’A.L. deve perseguire la minore traumaticità possibile. Sintomaticità e ansia sono due variabili molto spesso strettamente associate1. La presenza di flogosi acuta, e in particolare di formazioni ascessuali di origine endodontica o parodontale, rende inoltre meno efficace il controllo del dolore per un fenomeno chimico: l’ambiente fortemente acido del tessuto infiammato tampona infatti l’effetto dell’anestetico locale poiché queste molecole sono basi deboli.
Sede specifica da trattare
A seconda della localizzazione della lesione da trattare, l’A.L. nel bambino viene effettuata in una o più delle seguenti regioni:
a) mascellare sup.:
• infiltrazione plessica al n. alveolare superiore posteriore,
• infiltrazione plessica al n. alveolare superiore medio,
• infiltrazione plessica al n. alveolare superiore anteriore,
• blocco del n. palatino maggiore,
• blocco del n. naso-palatino dello Scarpa;
b) mandibola:
• infiltrazione plessica zona antero-laterale,
• infiltrazione plessica zona posteriore,
• blocco del n. buccinatorio o buccale,
• blocco del n. alveolare inferiore.
Utilizzando la scala SEM (Sound-Eye-Movement), che valuta la reazione del paziente pediatrico all’iniezione sulla base di questi 3 parametri, uno studio del 2009 di Aminabadi et al.9 ha suddiviso le sedi di iniezione in:
• sedi a basso punteggioSEM (e quindi meno dolorose): infiltrazione del n. alveolare superiore posteriore e blocco del n. alveolare inferiore;
• sedi a moderato punteggio SEM (mediamente dolorose): infiltrazione del n. alveolare superiore medio e infiltrazione vestibolare antero-laterale e posteriore della mandibola o blocco del n. buccinatorio;
• sedi ad alto punteggio SEM (molto dolorose): infiltrazione del n. alveolare superiore anteriore e blocco del n. palatino maggiore;
• sede a massimo punteggio SEM (la più dolorosa): blocco del n. naso-palatino.
Uso di anestesia topica
L’anestesia topica trova una forte indicazione in odontoiatria infantile, sia di per sé per effettuare semplici manovre su tessuti molli o estrazione di denti decidui con radici molto riassorbite sia come atto preparatorio in tutti i casi ci si appresti a effettuare un’anestesia locale. Il principio attivo viene somministrato sottoforma di gel, pomata, soluzione o soluzione spray, cerotti o gel parodontale; la molecola impiegata viene scelta in base alla sua capacità di attraversare la mucosa – non tutti gli anestetici locali iniettabili sono buoni anestetici topici; essi generalmente permettono di anestetizzare il tessuto molle fino a una profondità di 2 mm. Il principio attivo viene fornito in concentrazioni molto più elevate rispetto a quello contenuto negli anestetici iniettabili. Le principali formulazioni presenti in commercio contengono:
• benzocaina (crema, gel, cerotto, gomma, liquido, pasticca, pomata, pasta, spray, tampone) ; durata d’azione 10-20 min;
• benzocaina, butambina e tetracaina idrocloride (gel, soluzione, spray);
• diclonina idrocloride (pasticca, soluzione, spray); durata d’azione 20-40 min;
• lidocaina (pomata, cerotto, soluzione); durata d’azione 10-20 min;
• lidocaina idrocloride (gel, soluzione);
• lidocaina e prilocaina (gel parodontale); durata d’azione circa 20 min;
• tetracaina idrocloride (soluzione); durata d’azione 20-60 min.
Nessuna formulazione in commercio contiene vasocostrittori; allo scopo di ridurre il trauma da iniezione nel paziente pediatrico risultano particolarmente indicate le pomate anestetiche: esse vengono applicate mediante un pellet di cotone o un cotton fioc sulla mucosa asciutta della sede di iniezione e lasciate agire per circa 2 minuti prima di procedere all’A.L. per infiltrazione. Molto rari gli effetti collaterali da sovradosaggio per le quantità di anestetico normalmente applicate anche se il principio può raggiungere una qualche concentrazione nel torrente ematico. Se il piccolo paziente lamenta uno spiacevole gusto amaro si può proficuamente fare sciacquare la bocca, atto che aiuta il bambino a distrarsi. Anche l’anestesia superficiale per perfrigerazione, seppur meno pratica, può essere efficacemente applicata in qualche situazione come estrazione di denti vacillanti o incisione di ascessi. Essa è ottenuta spruzzando sulla mucosa uno spray di cloruro di etile o altri composti, che evaporando sottraggono calore al tessuto e lo raffreddano bloccando la conduzione degli impulsi nocicettivi. Entro pochi secondi bisogna quindi procedere con le manovre indicate. Bisogna avvertire il bambino che sentirà freddo, chiedergli di espirare o trattenere il respiro per evitare l’inalazione di cloruro di etile e far chiudere i suoi occhi perché lo spray potrebbe provocare lesioni corneali (figura 7).
Terapia sedativa o ansiolitica di supporto
Al fine di ridurre lo stress da iniezione e in generale legato alla seduta odontoiatrica, l’operatore può anche favorevolmente avvalersi di sedazione inalatoria o terapia ansiolitica per via enterale. La prima viene effettuata con una miscela di ossigeno e protossido d’azoto al 50% e determina anche una lieve analgesia non tuttavia sostitutiva dell’A.L.; la seconda non produce alcuna analgesia e viene ottenuta mediante somministrazione in gocce o supposte di cloralio idrato e idrossizina, combinazioni di meperidina e prometazina o idrossizina, diazepam, sola idrossizina o altre benzodiazepine come triazolam o midazolam11.
Scelta di siringa, ago e farmaco impiegato
La scelta della siringa impiegata può essere importante12,13: si preferisce una siringa poco ingombrante per le problematiche di accesso e di impressione generata nel bambino, rigida per evitare la rottura della tubofiala in seguito a eventuali improvvisi bruschi movimenti, con una buona fenestrazione laterale per ben controllare l’avanzamento del pistoncino e il liquido aspirato, che permetta l’aspirazione o auto-aspirante per scongiurare il rischio di iniezione intravasale. In commercio sono disponibili anche siringhe in plastica monouso trasparenti che permettono di migliorare la visibilità. Di qualche utilità possono talvolta risultare siringhe particolari quali, ad esempio:
• Citoject, con impugnatura a penna, riduce l’impressione generata dalla siringa tradizionale (figure 8 e 9);
• Sirijet, senza ago ma piuttosto rumorosa, ben accettata dai pazienti pediatrici e adulti sebbene possa esitare in piccoli ematomi e generalmente insufficiente per manovre quali pulpotomia o estrazioni dentali;
• Sistema Wand, un sistema di iniezione computerizzato che permette di modulare durata e pressione di iniezione e compiere ripetute prove di aspirazione.
L’ago impiegato deve avere un diametro sottile perché più traumatico, ma una rigidità che gli consenta di raggiungere il bersaglio desiderato senza piegarsi (specie nell’anestesia tronculare): il diametro consigliato comprende 25, 27 o 30 Gauge. La lunghezza varia da 8 mm (ago extra-corto) a 16 mm (ago corto), 31mm (ago lungo) o anche 38 mm (ago extra-lungo); aghi corti generano minor paura se osservati dal bambino ma sono più rischiosi in caso di frattura accidentale. Secondo alcuni Autori e secondo la nostra esperienza, il paziente non è in grado di avvertire differenza tra aghi di due diametri successivi a parità di tecnica di iniezione. Importante è anche la buona affilatura della punta, che si mantiene tale per massimo 3 diverse iniezioni (figura 10). Gli anestetici locali utilizzabili in odontoiatria infantile sono16:
• mepivacaina (4,5 mg/kg);
• articaina (6 mg/kg);
• prilocaina (6 mg/kg);
• bupivacaina (1 mg/kg).
Il contenuto per ml, e quindi per tubofiala da 1,8 ml, di ciascun anestetico può essere calcolato ricordando il seguente schema:
• concentrazione 1% = 10 mg/ml;
• concentrazione 2% = 20 mg/ml;
• concentrazione 3% = 30 mg/ml;
• concentrazione 4% = 40 mg/ml.
La prilocaina può indurre, in particolari condizioni, formazione di metaemoglobina, con rischio di sviluppare un quadro di metaemoglobinemia caratterizzato da cianosi delle mucose, della cute e del letto ungueale e insufficienza cardiorespiratoria. Gli A.L. usati in odontoiatria possono essere addizionati con vasocostrittori,generalmente epinefrina in diverse concentrazioni:
• concentrazione 1:100000, 1 ml = 10 mcg di epinefrina;
• concentrazione 1:200000, 1 ml = 5 mcg di epinefrina.
Di queste concentrazioni si dovrà tener conto nella somministrazione dell’A.L., considerando che la dose massima di epinefrina somministrabile, in odontoiatria, a bambini di classe ASA I e ASA II è di circa 2,5 mcg/kg17. Poiché alcune comuni preparazioni contenenti epinefrina sono addizionate con metabisolfito (antiossidante per l’epinefrina) nei pazienti allergici ai solfiti si dovrà ricorrere ad anestetici senza vasocostrittori oppure ad anestetici con vasocostrittori ma senza conservanti. La moderna tendenza del mercato è volta, infatti, a introdurre anestetici, quali l’articaina, privi di conservanti per l’epinefrina; se da un lato queste formulazioni mostrano il vantaggio di abbattere drasticamente il rischio di reazioni allergiche, comportano lo svantaggio di una minore durata di conservazione e di questo bisogna tener conto nella gestione delle forniture. Prima di procedere all’esecuzione dell’A.L. occorrerà aver effettuato un’accurata anamnesi del bambino presso i genitori o gli accompagnatori onde escludere l’esistenza di controindicazioni all’uso di anestetici locali. Tra queste, le principali comprendono:
• età inferiore ai 4 anni;
• trattamento con inibitori delle monoaminossidasi (IMAO) e beta-bloccanti;
• gravi disturbi cardiovascolari (disturbi del ritmo o della conduzione, insufficienza cardiaca acuta non compensata, ipertensione o recente infarto miocardico);
• emicrania essenziale;
• ipersensibilità nota verso gli anestetici locali di tipo estere o amidico.
Nel caso si impieghi un anestetico contenente epinefrina occorrerà tener presenti queste ulteriori controindicazioni:
• soggetti asmatici che presentano ipersensibilità ai solfiti;
• diabete mellito;
• glaucoma ad angolo chiuso;
• tachicardia parossistica o aritmia assoluta a elevata frequenza;
• gravi arteriopatie;
• manifestazioni ischemiche di qualsiasi tipo;
• ipertiroidismo.
Dal momento che il farmaco viene eliminato per via epatica e renale, precauzioni particolari dovranno essere prese in caso di insufficienza epatica o renale. Tra gli effetti indesiderati degli anestetici locali occorre includere reazioni tossiche e allergiche sia all’anestetico che al vasocostrittore (che possono comparire sia immediatamente per iniezione intravenosa accidentale, sia più tardivamente per sovradosaggio assoluto), oltre che complicanze di tipo neurologico locale o autolesioni dovute a morsicatura delle mucose per persistenza dell’anestesia dopo la fine della seduta. La tossicità dell’anestetico può esprimersi:
• sul sistema nervoso centrale: eccitazione, tremori, disorientamento, vertigini, midriasi, aumento del metabolismo e della temperatura corporea. Per dosi molto elevate anche trisma e convulsioni; se è interessato il midollo allungato si ha compartecipazione dei centri cardiovascolare, respiratorio ed emetico con sudorazione, aritmie, ipertensione, tachipnea, broncodilatazione, nausea e vomito;
• a livello periferico: può essere coinvolto l’apparato cardiovascolare con bradicardia e vasodilatazione.
Le reazioni di tipo allergico si manifestano più spesso in soggetti ipersensibili ma sono riferiti molti casi con assenza di ipersensibilità individuale all’anamnesi.
Queste sono rare e comprendono:
• manifestazioni locali: eruzioni cutanee di vario tipo, orticaria, prurito;
• manifestazioni generali: broncospasmo, edema laringeo e nei casi più gravi collasso cardiorespiratorio da shock anafilattico.
Il vasocostrittore, influenzando il circolo, può determinare effetti abnormi di vario tipo specialmente nei soggetti con preesistenti patologie cardiocircolatorie: ansia, sudorazione, dispnea, aritmie cardiache, ipertensione (particolarmente grave nei soggetti già ipertesi e negli ipertiroidei), cefalea acuta, fotofobia, dolore retrosternale e faringeo, vomito (e in questo caso sospendere immediatamente la somministrazione!). Dopo l’iniezione di A.L. è necessario osservare assiduamente il bambino dal momento che eventuali sintomi da tossicità o reazione allergica tendono in genere a manifestarsi entro i primi 5-10 minuti. Al primo segno di allarme occorre interrompere la somministrazione, porre il piccolo paziente in posizione orizzontale e assicurargli la pervietà delle vie aeree, somministrando ossigeno in caso di dispnea grave o effettuando la ventilazione artificiale con un pallone di Ambu. A questo punto è possibile ricorrere anche a opportune terapie farmacologiche di supporto14,15. Prima di ricorrere a tali terapie bisogna però sempre effettuare un’efficace diagnosi differenziale con la ben più comune reazione emotiva da sindrome vaso-vagale: i suoi sintomi comprendono pallore, sudorazione con ipotermia cutanea, ipotensione e tachicardia, nausea e irrequietezza fino alla sincope nel 15-20% dei casi. In queste situazioni è sufficiente porre il bambino in posizione orizzontale o di Trendelembourg, fargli aria e allontanare gli elementi ingombranti e fastidiosi, cercando contemporaneamente di distrarlo con argomenti lieti e divaganti. Per quanto riguarda le complicanze neurologiche locali si riportano, dopo A.L. odontoiatrica, rari casi di parestesia o di disestesia-anestesia: seppur fastidiosi per il piccolo paziente, si risolvono in genere nel periodo di 3 mesi. Molto più frequenti sono le complicanze da morsicatura del labbro, della lingua o delle altre mucose autoinflitte dal paziente a causa del persistere dell’anestesia, la cui incidenza è maggiore nei bambini e nei disabili17-20. Per contrastare questo rischio sarà necessario motivare i genitori a un assiduo controllo nelle due ore successive all’intervento e utilizzare, per quanto possibile, anestetici a più breve durata d’azione. Il formato delle tubofiale standard del commercio da 1,8 ml è la forma più pratica e igienica e la dose fornita è quella minima utile per produrre un’efficace anestesia tronculare nel bambino e nel paziente adulto. Per ottenere altri tipi di anestesia sono sufficienti dosi minori, ad esempio:
• infiltrazione sovra periostea a livello mascellare: 0,5 ml;
• blocco del n. mentoniero: 0,5-1 ml.
Vari studi dimostrano che riscaldare aghi e soluzione anestetica con fornetti termostatati a 40 ºC può ridurre il dolore da iniezione senza sostanzialmente alterare il pH della soluzione21,22.
Approccio al paziente
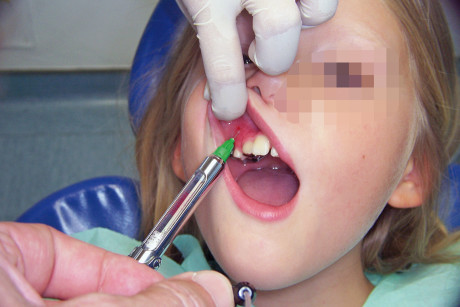
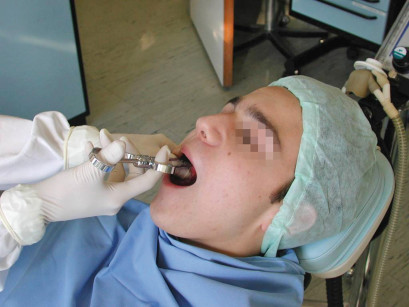
La statura del bambino rappresenta talvolta un ulteriore ostacolo per il pedodontista dal momento che la sua testa non arriva al poggiatesta dei normali riuniti per adulti compromettendo l’ergonomia e l’accessibilità. La realizzazione di speciali riuniti per bambini non ha mai trovato una reale diffusione sul mercato causa la difficoltà di commercializzazione. Si può in parte ovviare al problema staturale ponendo sulla seduta cuscini più o meno alti o lasciando il bambino in braccio a un genitore. Lo schienale della poltrona sarà inclinato a 45º o più, così che il paziente, per alzarsi, sia costretto a vincere il peso del proprio corpo e i suoi movimenti siano pertanto più lenti: questo riduce il rischio di provocare lesioni con l’ago in caso di risposte motorie improvvise. La testa del bambino dovrà essere reclinata indietro a 45º: così facendo, il suo campo visivo è spostato verso l’alto e gli strumenti ne rimangono al di fuori (figura 11). La mano o il braccio dell’operatore non impegnati nell’anestesia devono bloccare la testa o il viso del bambino per prevenire movimenti di fuga o rotazioni improvvise, con fermezza e decisione ma senza trasmettere un senso di costrizione. L’assistente porge quindi la siringa già pronta senza possibilmente farsi notare dal piccolo paziente; l’operatore la afferra saldamente e l’assistente rimuove il cappuccio (figura 12).
Approccio psicologico e tecniche di distrazione
L’approccio psicologico al paziente pediatrico è importante quanto una corretta tecnica esecutiva, poiché la collaborazione del bambino deve essere conquistata sin dal primo incontro e mai data per scontata ma anzi continuamente riconfermata. Ricerche di numerosi autori e la pratica quotidiana indicano che l’A.L. è la manovra più temuta di tutta la seduta pedodontica. Il fallimento di questa prova pregiudica tutte le fasi successive del nostro intervento terapeutico. Il tono di voce dell’operatore deve essere calmo, suadente e confortante; egli può avvalersi proficuamente di un lessico e immagini ludiche e giocose ricorrendo spesso a perifrasi e senza mai proferire i termini “puntura”, “ago”, “iniezione” ecc., senza necessariamente mentire, ma accennando piuttosto alla necessità di “addormentare il dentino per poterlo curare” o a immagini come “un piccolo pizzicotto” o “una punturina di zanzara”. In nessun caso si dovrà ingannare il bambino, pena la perdita della sua fiducia e collaborazione23. Può rivelarsi utile l’applicazione di tecniche di distrazione per distogliere l’attenzione del paziente nel momento esatto dell’iniezione, come ad esempio fargli sollevare alternativamente la gamba destra e sinistra9.
Procedura di iniezione
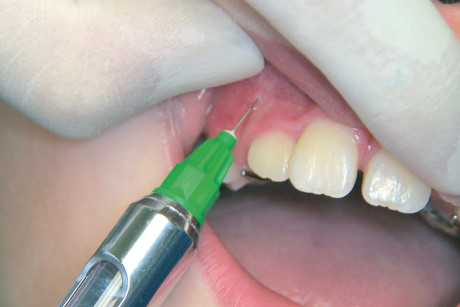
Prima dell’infiltrazione occorre necessariamente attendere 2-3 minuti dopo la somministrazione dell’anestesia topica sulla mucosa asciutta (figure 13 e 14). Ottenuto l’effetto anestetico superficiale, si disperdono le prime gocce di anestetico facendo avanzare il pistoncino della tubofiala onde vincere l’iniziale resistenza di questo; si porta la siringa in bocca tenendola fuori dal campo visivo del paziente e si penetra lentamente la mucosa. Prima di iniziare l’eiezione si effettua la prova di aspirazione, che è bene ripetere dopo aver ruotato di 90º l’ago onde evitare che la punta, impegnandosi contro la parete interna di un vaso, determini un falso negativo. Il rilascio della soluzione deve essere lento, della durata di circa 2 minuti per tubofiala per non provocare eccessiva distensione dolorosa dei tessuti (figura 15). Al fine di ottenere un’analgesia da disturbo di contorno si è rivelata molto efficace anche la stimolazione della mucosa adiacente la sede dell’iniezione (o counterstimulation)24: essa si produce stirando la mucosa alveolare oppure comprimendo la mucosa aderente a seconda della regione infiltrata, oppure ancora effettuando pressioni vibratorie con un polpastrello con frequenza di 2-3 cicli/sec (figura 16). In alcune regioni come il palato è sufficiente depositare 0,2-0,3 ml di soluzione. Per regioni più ampie si può procedere con iniezioni multiple ma ravvicinate, al fine di estendere in modo atraumatico l’anestesia. Per quanto riguarda l’anestesia tronculare del n. alveolare inferiore si consiglia la tecnica diretta poiché aghi molto sottili (25-27-30 G) sono anche poco precisi (figura 17). Nel bambino i tempi di attesa perché abbia effetto l’A.L. sono più brevi rispetto all’adulto: si consiglia di attendere 1-3 minuti per anestesia plessica e 3-10 minuti per l’anestesia tronculare.
Conclusioni
Tenere ben presenti tutti gli aspetti descritti fino a tradurli in routine quotidiana può far sì che l’anestesia locale nel paziente pediatrico perda quell’aura di terrore che la circonda agli occhi sia del bambino sia del dentista. Infatti, riuscire a ridurre lo stress della seduta in occasione dei primi contatti del bambino con il setting odontoiatrico è un obiettivo fondamentale che determinerà l’imprinting del paziente nel collaborare a tutte le future cure odontoiatriche domiciliari e professionali per molti anni della sua vita. Inoltre, il professionista deve obbligatoriamente imparare a gestire tutti gli aspetti dell’anestesia locale, con particolare attenzione alla diagnosi e al trattamento delle reazioni acute tossiche o allergiche che possono talvolta manifestarsi e mettere a serio rischio la vita dei piccoli pazienti.
Corrispondenza
Dottor Luigi Paglia
Dipartimento di Odontoiatria Infantile
Isitituto Stomatologico Italiano
Via Pace, 21 – 20122 Milano
bibliografia
1. Nakai Y, Milgrom P, Mancl L, Coldwell SE, Domoto PK, Ramsay DS. Effectiveness of local anesthesia in pediatric dental practice. J Am Dent Assoc 2000;131;1699-1705.
2. Berggren U, Meynert G. Dental fear and avoidance: causes, symptoms, and consequences. JADA 1984;109:247-51.
3. Milgrom P, Vigneshsa H, Weinstein P. Adolescent dental fear and control: prevalence and theoretical implications. Behav Res Ther 1992;30:367-73.
4. Malamed SF, Trieger N. Intraoral maxillary nerve block: an anatomical and clinical study. Anesth Prog 1983 Mar-Apr;30(2):44-8.
5. Zerosi C. On some morphological aspects of the fibrous matrix of the pulp of deciduous teeth during resorption. SSO Schweiz Monatsschr Zahnheilkd 1965 Jan 1;75:123-6.
6. Ram D, Peretz B. The assessment of pain sensation during local anesthesia using a computerized local anesthesia (Wand) and a conventional syringe. J Dent Child 2003;70:130-133.
7. Ram D, Peretz B. Reaction of children to maxillary infiltration and mandibular block injections. Pediatr Dent 2001;23:343-346.
8. Allin KD, Kotil D, Larzelere RE, Hutfless S, Beiraghi S. Comparison of a computerized anesthesia device with a traditional syringe in preschool children. Pediatr Dent 2002;24:315-320.
9. Aminabadi NA, Farahani RM, Oskouei SG. Site-specificity of pain sensitivity to intraoral anesthetic injections in children. J Oral Sci 2009;51(2):239-43.
10. Wright GZ. Nonpharmacologic management of children’s behaviors. In: Dentistry for the child and adolescent (2004). McDonald RE, Avery DR, Dean JA eds, 8th ed, St Louis, Mosby, 38-39.
11. G.Damia, L.Paglia, F.Ghielmi. Tecniche ambulatoriali di sedazione cosciente in odontoiatria. Il Dentista Moderno 2010;12:58-63.
12. Munshi AK, Hegde A, Bashir N. Clinical evaluation of the efficacy of anesthesia and patient preference using the needle-less jet syringe in pediatric dental practice. J Clin Pediatr Dent 2001 Winter;25(2):131-6.
13. Kraus DM, Stohlmeyer LA, Hannon PR, Freels SA. Effectiveness and infant acceptance of the Rx medibottle versus the oral syringe. Pharmacotherapy 2001 Apr;21(4):416-23.
14. Adewumi A, Hall M, Guelmann M, Riley J. The incidence of adverse reactions following 4% septocaine (articaine) in children. Pediatr Dent 2008 Sep-Oct;30(5):424-8.
15. Malamed SF. Local anesthesia reversal. Dent Today 2010 Mar; 29(3):65-6,68,71-2passim;quiz 74.
16. Ahmed MM, Martinez HR. Short communication: Graph for calculating maximum local analgesic dose in millilitres for the paediatric population. Eur Arch Paediatr Dent 2009 Nov;10 Suppl 1:40-2.
17. http://www.ainos.info/portal/?q=node/37 , Raccomandazioni sulla sedazione cosciente e sull’anestesia loco-regionale in odontoiatria pediatrica (2006). A cura dell’Associazione Italiana di Narco Odontostomatologia.
18. Chi D, Kanellis M, Himadi E, Asselin ME. Lip biting in a pediatric dental patient after dental local anesthesia: a case report. J Pediatr Nurs 2008 Dec;23(6):490-3. Epub 2008 Sep 10.
19. Townsend JA, Ganzberg S, Thikkurissy S. The effect of local anesthetic on quality of recovery characteristics following dental rehabilitation under general anesthesia in children. Anesth Prog 2009 Winter;56(4):115-22.
20. Ngeow WC. Look out for the bite marks. A letter to editor on article “Lip biting in a pediatric dental patient after dental local anesthesia: a case report”. J Pediatr Nurs 2009 Dec;24(6):447.
21. Colaric KB, Overton DT, Moore K. Pain reduction in lidocaine administration through buffering and warming. Am J Emerg Med 1998;16:353-356.
22. Courtney DJ, Agrawal S, Revington PJ. Local anaesthesia: to warm or alter the pH? A survey of current practice. J R Coll Surg Edinb 1999;44:167-171.
23. Nutter DP. Good clinical pain practice for pediatric procedure pain: target considerations. J Calif Dent Assoc 2009 Oct;37(10):719-22.
24. Aminabadi NA, Farahani RMZ, Balayi Gajan E. The efficacy of distraction and counterstimulation in the reducing of pain reaction to intraoral injection by pediadric patients. J Contemp Dent Pract 2008;9:33-40.