Obiettivi. L’obiettivo di questo lavoro è di presentare un protocollo operativo dedicato all’approccio odontoiatrico al paziente non collaborante, in regime di anestesia generale, mediante singola seduta di trattamento.
Materiali e metodi. Viene presentato un protocollo operativo che integra una revisione della letteratura con l’esperienza maturata dagli autori in numerosi anni di applicazione dell’anestesia generale nel trattamento odontoiatrico completo del paziente non collaborante. Mediante la presentazione di un caso clinico, verranno descritte la conclusione del processo diagnostico e la formulazione del piano di trattamento definitivo contestuale alla stessa seduta di anestesia generale. Verranno, inoltre, analizzati vantaggi, difficoltà e limiti correlati all’esecuzione di un trattamento odontoiatrico completo in una singola seduta terapeutica.
Risultati e conclusioni. Nonostante la variabilità clinica impedisca di definire delle linee guida dettagliate applicabili a ogni caso, l’insieme delle indicazioni fornite consente di attuare un valido inquadramento del caso clinico e del piano di trattamento da un punto di vista endodontico, conservativo, parodontale, protesico e chirurgico.
Applications of general anesthesia in dentistry. Operative protocols for the treatment of non compliant patients in a single surgical session.
Purpose. The aim of this paper is to present a clinical protocol designed to provide complete dental treatment to non compliant patients via a single session under general anesthesia.
Materials and methods. We present a practical protocol based on a literature review and on the experience acquired by the authors after several years of implementing general anesthesia to treat non compliant dental patients in a single surgical session. Through a case presentation, a detailed analysis of the main advantages, limits, and disadvantages of complete dental treatments in a single surgical session is provided. The need to complete the diagnostic process and treatment plan during the anesthesia session is also evaluated.
Results and conclusions. Despite clinical variability does not allow to define a specific guideline applicable to all clinical cases, the indication we provided allows to efficiently define a valid treatment plan, with respect to the endodontic, conservative, periodontal, prosthetic and surgical approaches.
Il trattamento odontoiatrico del paziente non collaborante comporta notevoli difficoltà in merito all’inquadramento diagnostico completo del caso clinico, alla scelta delle procedure terapeutiche idonee e al monitoraggio nel tempo delle terapie effettuate.
La letteratura indica che le principali cause di mancata complicance sono rappresentate da gravi forme di odontofobia e da inabilità fisica e/o mentale1-5.
Per il trattamento odontoiatrico completo, in singola seduta di questi pazienti, l’anestesia generale spesso è l’unica opzione terapeutica efficace e sicura1,6.
L’obiettivo di questo lavoro è quello di presentare un protocollo operativo dedicato alla progettazione e all’esecuzione di trattamenti odontoiatrici completi in anestesia generale.
Mediante una revisione della letteratura su queste tematiche e la descrizione di un caso esemplificativo, verranno analizzati vantaggi, difficoltà e limiti di tale approccio terapeutico.
Indicazioni all’anestesia generale in campo odontoiatrico
Le principali condizioni per cui sia indicato un trattamento odontoiatrico in regime di anestesia generale sono rappresentate da:
a) incapacità di collaborazione secondaria ad autismo, ritardo mentale idiopatico o associato a quadri patologici/sidromici, paralisi cerebrali e disturbi psichiatrici;
b) mancata efficacia/possibilità di utilizzo degli anestetici locali, secondaria a infezione acuta, varianti anatomiche o allergie;
c) esigenza immediata di terapie invasive, di carattere chirurgico o polispecialistico;
d) presenza di condizioni sistemiche ad alto rischio, per cui sia indicato un controllo intraoperatorio dei parametri vitali sotto anestesia generale1,7-9.
Molteplici autori hanno evidenziato come la maggior parte dei pazienti in cui tale approccio trova maggiore indicazione presenta un’età inferiore a 20 anni, in particolare rientra nella fascia dei 2-9 anni1,3.
La richiesta di procedure odontoiatriche in regime di anestesia generale è tuttavia in crescita anche negli adulti, soprattutto a causa di odontofobia associata o meno a patologie psichiatriche farmaco-controllate10-13.
Un lavoro di Abdulwahab et al. riporta come il 60% della popolazione adulta del Kuwait preferirebbe ricevere i propri trattamenti odontoiatrici attraverso una metodica di controllo dell’ansia. In particolare, il 14% è affetto da franca odontofobia, il 30% riferisce di avere cancellato i propri appuntamenti dentali una o più volte in seguito ad ansia e il 40% preferirebbe ricevere trattamenti odontoiatrici in regime di anestesia generale14.
Ad oggi, l’utilizzo dell’anestesia generale in campo odontoiatrico è ampiamente diffuso: Balogh et al. evidenziano come il 40% di tutte le sedute di anestesia generale eseguite in pazienti affetti da disabilità mentali siano infatti richieste per un trattamento odontoiatrico2,15.
La programmazione di un intervento odontoiatrico in anestesia generale viene sempre delineata in collaborazione con un anestesista, in modo che venga eseguita un’attenta analisi di tutte le condizioni sistemiche che possano rappresentare una controindicazione1,16.
Secondo i dati riportati da Ohtawa et al. sul trattamento odontoiatrico di 163 pazienti in regime di anestesia generale, le procedure maggiormente eseguite sono i restauri conservativi (60%), seguite dalle estrazioni dentarie (18,3%) e dai trattamenti endodontici (12,4%), di cui il più frequente in ambito pediatrico è la pulpotomia dell’elemento vitale1.
La quasi totalità dei trattamenti è correlata a presenza di carie e secondariamente a malattia parodontale, in relazione alla scarsa capacità dei pazienti affetti da ritardo mentale nel mantenere un’adeguata igiene orale domiciliare1-3,7.
Diversi autori concordano nel definire il numero medio di elementi trattati per paziente fra 7 e 131,2,17-19.
O’Sullivan et al. hanno, inoltre, stimato che in tali pazienti il trattamento odontoiatrico in anestesia locale, ove possibile, richiederebbe più di sei appuntamenti, evidenziando l’indubbio vantaggio offerto da una singola seduta di anestesia generale3,20.
Morbilità e mortalità
La frequenza di eventi avversi nel corso di interventi odontoiatrici/oro-maxillo-facciali in regime di anestesia generale è stata stimata da diversi autori6,21-25.
Fra i dati più recenti, D’Eramo et al. riportano un tasso di mortalità di 1:1.733.055, e una frequenza di eventi avversi di 1:26.698, in pazienti sottoposti ad anestesia generale per interventi di chirurgia oro-maxillo-facciale6.
L’evento avverso più frequentemente riscontrato è il laringospasmo, presente in 1 su 833 pazienti (0,15%).
Vengono inoltre riportati, con frequenza inferiore: broncospasmo, aritmie cardiache, ipertensione, ipotensione, insufficienza cardiaca congestizia, angina pectoris, infarto miocardico, lesioni nervose e/o cervicali associate a cambiamenti nel posizionamento del paziente in corso di anestesia, flebiti, shock insulinico e chetoacidosi diabetica6.
Dal confronto con pubblicazioni precedenti, emerge come l’introduzione dei moderni principi anestetici - quali il midazolam, il fentanyl e il propofol - abbia ridotto significativamente la frequenza di laringospasmo, broncospasmo, nausea, emesi e flebiti. Tali complicanze erano infatti maggiormente frequenti con l’utilizzo di agenti quali metoexitale, diazepam e meperidina6,26.
È importante specificare come l’evento avverso più frequentemente riscontrato in ambito oro-maxillo-facciale non si verifichi durante sedute di anestesia generale, ma sia rappresentato da eventi sincopali sviluppati in regime di anestesia locale, riscontrati in 1 su 151 pazienti, principalmente rappresentati da svenimento insorto all’inizio o al termine della seduta chirurgica6.
La ridotta morbilità e mortalità da anestesia generale descritta nella letteratura di ambito oro-maxillo-facciale deve tuttavia essere correlata al fatto che le procedure chirurgiche eseguite in tale campo vengono frequentemente condotte in pazienti in buone condizioni di salute sistemica (ASA I e ASA II-American Society of Anesthesiologists’ Physical Status Classification)27 poiché generalmente elettive.
Inoltre, in presenza di eventuali problematiche correlate all’anestesia generale, l’intervento di chirurgia orale può generalmente essere interrotto senza complicanze di carattere sistemico.
Il limite della letteratura disponibile in tale ambito è rappresentato dalla mancanza di un’analisi dettagliata di come la classe ASA, l’età del paziente e la durata della seduta di anestesia generale influiscano sulla morbilità della procedura6.
Alternative all’anestesia generale
La principale alternativa all’anestesia generale per il trattamento odontoiatrico del paziente non collaborante è rappresentata dalla sedazione cosciente, indotta per via parenterale o inalatoria6,7,28,29.
Molti degli agenti utilizzati in ambito di sedazione cosciente per via parenterale sono farmaci anestetici somministrati a dosi sub-anestetiche30-33 mentre l’agente di prima scelta per la somministrazione inalatoria è il protossido di azoto34.
In entrambi i casi, la sedazione cosciente si distingue dall’anestesia generale per il mantenimento dello stato di coscienza, della capacità di comunicazione e dei riflessi protettivi faringei e tracheali28.
Tale metodica rappresenta una valida alternativa a bassa invasività, indicata per l’esecuzione di procedure avanzate in pazienti altamente collaboranti, o di procedure poco invasive in pazienti con ridotta compliance29,35-39.
Tuttavia, il suo utilizzo richiede un buono stato di salute generale (ASA I o II)36,39, un’età superiore a 12-16 anni29,37,38 e un minimo grado di collaborazione da parte del paziente, spesso non presente nelle forme avanzate di odontofobia, patologia psichiatrica o ritardo mentale35.
In presenza di trattamenti chirurgici invasivi, di compromissioni significative della salute sistemica e di gravi forme di disturbo/ritardo mentale, l’anestesia generale rimane quindi una scelta obbligata28.
Fra gli eventi avversi più frequentemente associati all’utilizzo della sedazione cosciente sono stati descritti possibili fenomeni allucinatori, legati all’utilizzo di benzodiazepine, propofol e ossido nitrico28,40,41.
L’esposizione occupazionale al protossido di azoto pone inoltre rischi potenziali di natura ematologica, immunologica e a carico del sistema riproduttivo femminile, in seguito a una reattività con la cobalamina (forma ridotta della vitamina B12), da cui derivano alterazioni a carico delle reazioni di metilazione e di sintesi degli acidi nucleici30,34,42,43.
Case report
Un paziente di 42 anni, in buono stato di salute generale (ASA I - Sakland, 1941), non fumatore, gravemente odontofobico e non sottopostosi a trattamenti odontoiatrici negli ultimi 10 anni, si presenta alla nostra attenzione per cure odontoiatriche complete. Il paziente riferisce una bassa esigenza estetica e il timore di lussare i propri denti durante lo spazzolamento; pertanto, ha sospeso da tempo indefinito le normali manovre di igiene orale.
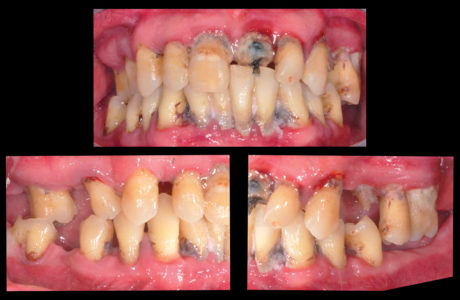
L’esame obiettivo evidenzia in primo luogo un basso grado di igiene orale, con indice di sanguinamento (Full Mouth Bleeding Score - FMBS) e indice di placca (Full Mouth Plaque Score - FMPS) del 100%, associato ad assenza degli elementi 1.7, 1.5, 2.7, 3.7, 3.6, 4.6, persi in seguito a parodontopatia e/o carie (Figura 1).
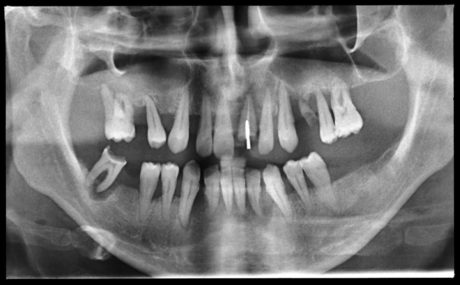

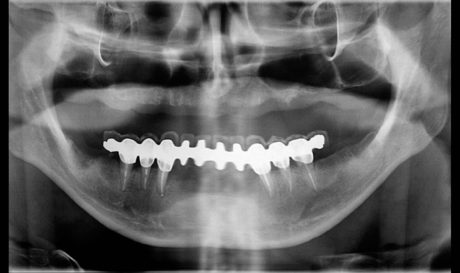
Previo esame obiettivo, esecuzione di un esame ortopantomografico (Figura 2) ed esecuzione di una valutazione anestesiologica basata su esami strumentali convenzionali (Figura 3), viene proposto un trattamento completo in anestesia generale, in singola seduta, comprensivo di igiene orale professionale, trattamento endodontico/restaurativo/parodontale/protesico degli elementi residui salvabili in arcata inferiore, trattamento estrattivo degli elementi residui non salvabili e confezionamento di una protesi mobile totale in arcata superiore.
Nello specifico, il piano di cura è stato impostato come segue:
a) in una seduta preliminare, con l’ausilio di una sedazione cosciente endovenosa, sono state rilevate impronte in alginato di sodio, al fine di confezionare modelli studio e master, previa igiene orale professionale sopragengivale, attuata mediante strumentario ultrasonico;
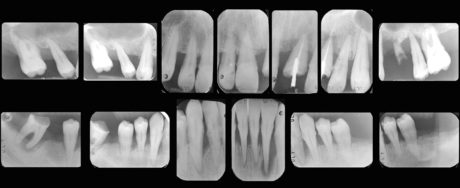
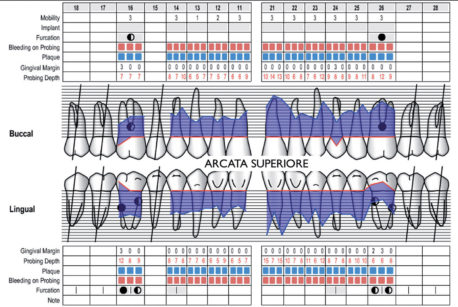
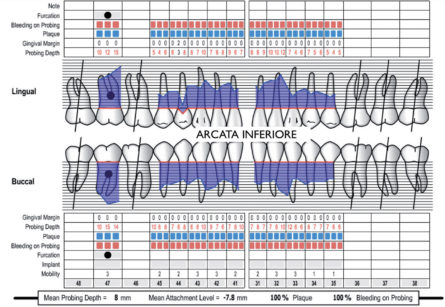
b) nella seduta di trattamento in regime di anestesia generale, si è proceduto in primo luogo al completamento del processo diagnostico e alla definizione del piano di trattamento definitivo mediante uno status radiografico endorale e una cartella parodontale (Figure 4-6). Tali procedure non erano attuabili a paziente sveglio per mancanza di compliance;
c) trattamento endodontico degli elementi 4.5, 4.4, 4.3, 3.3, 3.4, 3.5 in vista di una successiva preparazione protesica. L’elemento 43 era, inoltre, affetto da carie a estensione endodontica. La strumentazione canalare è stata eseguita con strumentario rotante in lega nickel-titanio (Mtwo Files - Sweden & Martina S.p.A., Padova, Italia) e l’otturazione dello spazio endodontico è stata eseguita mediante tecnica di condensazione verticale a caldo con coni di guttaperca;
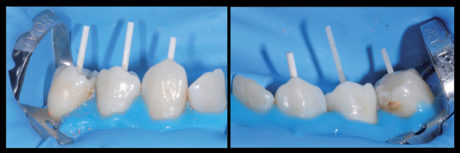
d) restauro degli elementi trattati endodonticamente, mediante posizionamento di una ritenzione endocanalare a perno in fibra di vetro (EnaPost - Micerium S.p.A., Genova, Italia) e confezionamento di un build-up diretto in materiale composito (Enamel Plus HRi - Micerium S.p.A., Genova, Italia) (Figura 7);
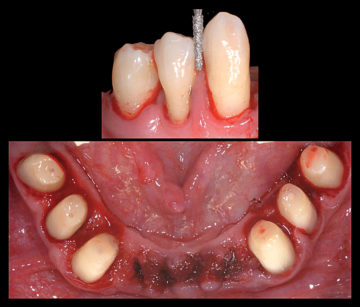
e) estrazione degli elementi affetti da malattia parodontale considerati non recuperabili: 1.6, 1.4, 2.1, 2.2, 2.3, 2.4, 2.6, 3.2, 3.1, 4.1, 4.2, 4.6. Sono stati inoltre estratti gli elementi 1.3, 1.2, 1.1 al fine di consentire una riabilitazione protesica mobile totale in arcata superiore (Figura 8);

f) preparazione protesica degli elementi residui 3.3, 3.4, 3.5, 4.3, 4.4, 4.5 con margine di preparazione a finire (Figura 9);
g) ribasatura di un restauro protesico provvisorio confezionato in pre-limatura, esteso da 3.5 a 4.5 con elementi intermedi 3.2, 3.1, 4.2, 4.1. Il margine di finitura è stato appositamente collocato in sede sopra-gengivale al fine di facilitare le manovre di igiene orale domiciliare durante la fase di mantenimento delle terapie parodontali eseguite a carico degli elementi pilastro 3.3, 3.4, 3.5, 4.3, 4.4, 4.5 e in modo tale da rispettare lo spazio biologico44;
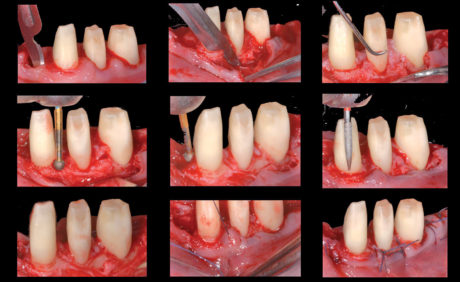
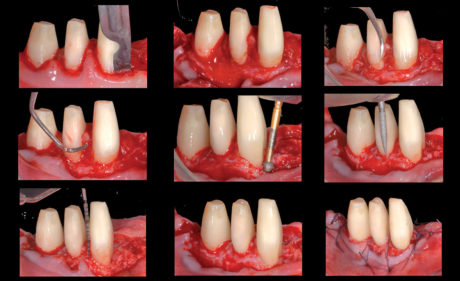
h) chirurgia parodontale resettiva degli elementi 3.3, 3.4, 3.5, 4.3, 4.4, 4.5 atta al ripristino della fisiologica architettura positiva del tessuto osseo a supporto di tali elementi. Previa rimozione del restauro protesico ribasato è stata eseguita l’escissione del tessuto infiammatorio delle tasche gengivali mediante incisione a bisello interno, posta 0,5 mm apicalmente al margine gengivale libero degli elementi trattati. Successivamente, in entrambi i siti è stato elevato un lembo a riposizionamento apicale, mediante scollamento a spessore totale nei versanti linguali e nel terzo coronale dei versanti vestibolari, e dissezione a spessore parziale nei due terzi apicali dei versanti vestibolari. Sono stati quindi eseguiti scaling e root planing degli elementi dentari mediante strumentario manuale e ultrasonico, seguiti da rimodellamento osseo con strumentario rotante e dalla finalizzazione a cielo aperto del margine protesico degli elementi pilastro. L’accesso è stato chiuso mediante punti a materassaio verticale esterno in Vycril 5/0 (Perma Sharp® Suture, Hu-Friedy Mfg. Co., LLC) e suture periostali, che hanno consentito il riposizionamento apicale del margine gengivale (Figure 10, 11);
i) cementazione provvisoria del restauro protesico ribasato nell’arcata inferiore (Figura 12);
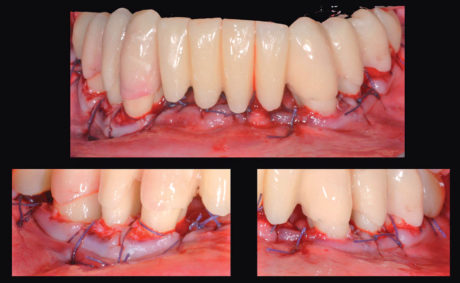
j) ribasatura (Viscogel®, Dentsply International INC., York, PA, USA) e posizionamento di una protesi mobile totale immediata in arcata superiore, pre-confezionata (Figura 13).
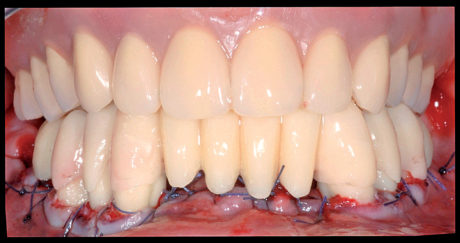
La seduta di anestesia generale si è conclusa nell’arco di circa 5 ore senza alcuna complicanza di sorta. La dimissione del paziente è stata effettuata dopo 8 ore dal termine dell’intervento con le seguenti istruzioni post-operatorie:
a) applicazione di impacchi di ghiaccio sulla zona operata per le prime 6-8 ore dopo l’intervento;
b) terapia antibiotica mediante 2 grammi di amoxicillina+acido clavulanico per 6 giorni dopo l’intervento;
c) terapia analgesico/antinfiammatoria con FANS per 2-3 giorni;
d) sciacqui con clorexidina fino alla rimozione dei punti di sutura;
e) dieta fredda e liquida per 24 ore dopo l’intervento e dieta morbida fino a rimozione dei punti.
Il decorso post-operatorio è stato privo di complicanze, eccetto un modesto edema risoltosi entro pochi giorni dall’intervento. A distanza di 7 giorni è stata eseguita la rimozione dei punti di sutura (Figura 14).
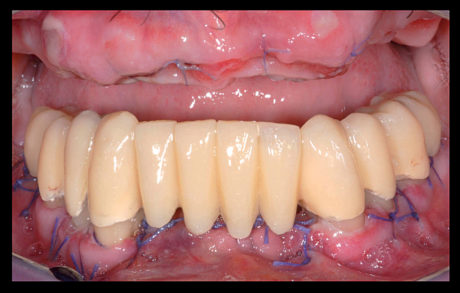
In seguito al rapido miglioramento delle proprie condizioni orali, il paziente è risultato nettamente più collaborante nelle sedute di richiamo, consentendoci, a distanza di 12 settimane, di riscontrare un netto miglioramento dell’igiene orale domiciliare, di eseguire il sondaggio parodontale degli elementi pilastro residui, di ribasare la protesi totale in arcata superiore e di rilevare un’impronta di precisione in arcata inferiore.
Successivamente, è stato pertanto posizionato nell’arcata inferiore un ponte protesico in resina con armatura metallica, utilizzato come restauro provvisorio a lungo termine in seguito alla scarsa disponibilità economica del paziente (Figure 15-17).
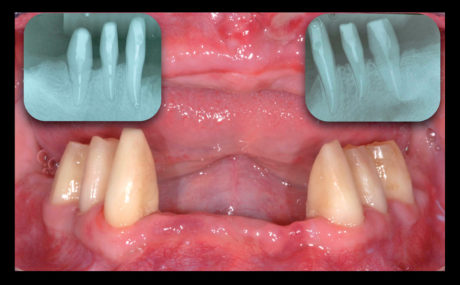
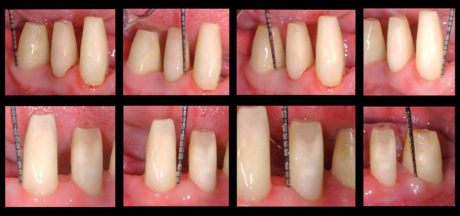
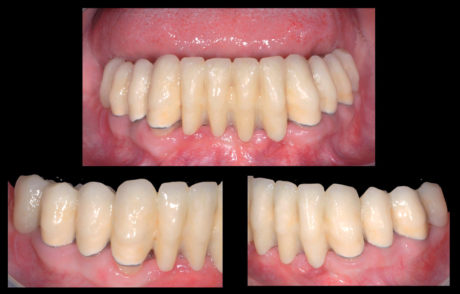
Il follow-up del paziente è stato condotto per 36 mesi, attraverso regolari sedute motivazionali volte a migliorare il mantenimento dell’igiene orale domiciliare. All’ultimo richiamo non è stata evidenziata alcuna complicanza (Figura 18).
Discussione
L’anestesia generale rappresenta un’opzione largamente supportata nel trattamento odontoiatrico completo in singola seduta del paziente non collaborante1-3,6. Tuttavia, tale approccio comporta molteplici problematiche nell’impostazione di un piano di trattamento multidisciplinare, primariamente legate alla mancata possibilità di:
a) suddividere le procedure terapeutiche in più appuntamenti;
b) attuare un processo diagnostico accurato durante le valutazioni pre-operatorie;
c) sfruttare a pieno il contributo del paziente nel mantenimento dell’igiene orale domiciliare.
Tali limitazioni influiscono in modo differente nei diversi ambiti delle procedure odontoiatriche, richiedendo talvolta di modificare approcci terapeutici convenzionali in funzione del caso clinico, e in particolare:
a) delle motivazioni per cui viene eseguito un trattamento in regime di anestesia generale;
b) delle condizioni di salute orale del paziente;
c) della sua capacità di contribuire al mantenimento a lungo termine dei risultati terapeutici.
Proponiamo il seguente protocollo operativo quale riferimento per l’impostazione di un piano di trattamento completo in tale contesto.
Valutazione pre-operatoria
In relazione al grado di collaborazione del paziente, il processo diagnostico e la formulazione del piano di trattamento in prima seduta possono essere limitati in vario grado. Al fine di pianificare un trattamento completo in regime di anestesia generale, si ritiene quantomeno indispensabile l’esecuzione di un’indagine ortopantomografica e di una valutazione clinica preliminare e, quando possibile, la rilevazione di impronte studio.
Indagini maggiormente invasive, quali il sondaggio parodontale e l’esecuzione di uno status radiografico endorale, non risultano talvolta realizzabili e vengono rimandate, qualora necessarie, alla seduta di anestesia generale.
In collaborazione con il medico anestesista, viene eseguita un’attenta valutazione dello stato di salute generale del paziente e del suo rischio di sviluppare complicanze in corso di anestesia generale1,16. Nello specifico, vengono valutati la possibilità di intubazione naso-faringea e i convenzionali esami strumentali pre-operatori indicati in caso di narcosi (Figura 3). È inoltre fondamentale sondare possibili alternative al trattamento in anestesia generale, quali la sedazione cosciente, coinvolgendo attivamente il paziente nella scelta della tecnica di controllo dell’ansia.
Qualora la seduta di anestesia generale sia pianificata al di fuori di un contesto ospedaliero, è inoltre fondamentale valutare attentamente che la struttura di cui si dispone sia adeguatamente attrezzata per la gestione delle complicanze riconducibili allo stato di salute sistemico del paziente o alle procedure odontoiatriche/oro-maxillo-facciali pianificate13.
Ordine delle procedure
In primo luogo, vengono eseguiti tutti gli approfondimenti di tipo radiografico o clinico necessari al completamento del processo diagnostico e alla formulazione di un piano di trattamento definitivo, che non siano tollerati dal paziente nel contesto pre-operatorio13. Seguono in ordine: procedure endodontiche e conservative, procedure protesiche, trattamenti parodontali e trattamenti chirurgici.
Tale sequenza operativa presenta infatti molteplici vantaggi: l’esecuzione delle procedure endodontico-conservative in prima istanza consente il pieno consolidamento dei restauri pre-protesici prima della preparazione degli elementi per cui sia prevista la ricopertura; il confezionamento di restauri protesici prima di eventuali terapie parodontali e chirurgiche evita il contatto dei materiale da impronta con il sito post-chirurgico, con eventuale traumatismo delle suture alla rimozione dell’impronta; l’esecuzione delle procedure chirurgiche al termine della seduta terapeutica consente di ridurre il sanguinamento del campo operatorio durante le fasi endodontico-conservative, protesiche e parodontali.
Tuttavia, qualora la presenza di elementi non salvabili interferisca con il trattamento degli elementi adiacenti, la chirurgica estrattiva viene generalmente anticipata.
Procedure endontiche-conservative
L’approccio in singola seduta richiede forzatamente di riunire strumentazione e otturazione canalare allo stesso tempo chirurgico, nonostante alcuni autori abbiano riportato come la suddivisione delle due procedure in appuntamenti separati si associ a una ridotta percezione di dolore e minore assunzione di farmaci antidolorifici nei giorni successivi all’otturazione canalare45. Inoltre, l’orientamento terapeutico è influenzato dalle motivazioni alla base della pianificazione del caso in anestesia generale: Savanheimo et al. riportano come pazienti odontofobici estremamente non cooperanti ricevano più frequentemente terapie conservative, endodontiche e preventive, mentre pazienti trattati in anestesia generale in seguito a condizioni di salute orale particolarmente gravi sono soggetti più frequentemente a estrazioni e terapie parodontali7.
Secondo l’esperienza riportata dagli autori, nel trattamento di pazienti non collaboranti con limitata possibilità di rivalutazione e mantenimento di adeguata igiene orale è generalmente preferibile attuare il trattamento endodontico degli elementi candidati alla protesizzazione, come eseguito per gli elementi 4.5, 4.4, 3.3, 3.4, 3.5 del caso descritto.
Per quanto concerne il restauro dei denti trattati endodonticamente, è inoltre possibile avvalersi di metodiche CAD-CAM chairside al fine di confezionare in modo immediato restauri post-endodontici di tipo indiretto, quali onlay, overlay ed endo-crown46,47.
Procedure protesiche
Il piano di trattamento protesico viene impostato al fine di massimizzare la capacità del paziente di mantenere un adeguato livello di igiene orale, prediligendo soluzioni di facile manutenzione quali protesi mobili parziali/totali e restauri a ponte su pilastri naturali.
Qualora venga eseguito un restauro protesico fisso, l’approccio in singola seduta limita fortemente le potenzialità delle fasi di provvisorizzazione, impedendo di ottenere un ideale condizionamento dei tessuti molli peri-protesici nelle aree estetiche, attraverso le convenzionali ribasature periodiche dei margini del restauro. Nel contesto dell’anestesia generale, alcuni autori riportano inoltre una maggiore difficoltà nella preparazione protesica dei pilastri posteriori13.
In aggiunta, la rilevazione di impronte di precisione a distanza dalla seduta di anestesia generale può risultare problematica qualora il paziente non sia sufficientemente collaborante. In tale caso, l’utilizzo della sedazione cosciente rappresenta un valido supporto per l’esecuzione di procedure secondarie al trattamento eseguito in anestesia generale, quali la rilevazione di impronte di precisione, l’esecuzione di radiografie endorali e la compilazione della cartella parodontale.
Procedure parodontali
Il principale limite di un approccio in singola seduta a forme attive di malattia parodontale consiste nell’impossibilità di sfruttare appieno il potenziale di guarigione del paziente attraverso la convenzionale suddivisione della terapia parodontale nelle sue fasi sistemica, causale, di rivalutazione, chirurgica (qualora necessaria) e di mantenimento.
Un trattamento corretto della malattia parodontale si fonda in primo luogo su una terapia causale non chirurgica, di tipo sistemico (eliminazione/controllo di fattori di rischio quali abitudine al fumo e controllo glicemico nel paziente diabetico) e locale (sedute di levigatura radicolare - Scaling and Root Planing - SRP)48,49.
La terapia causale non chirurgica mira alla risoluzione dell’infezione parodontale in fase attiva attraverso la rimozione dei depositi di tessuto infiammatorio e dei fattori di ritenzione batterica presenti nella tasca parodontale48,50. L’eventuale indicazione a una seconda fase terapeutica, di tipo chirurgico, viene normalmente valutata a distanza di 45-80 giorni durante un’apposita seduta di rivalutazione48,49. Il trattamento chirurgico costituisce pertanto uno stadio opzionale della terapia parodontale, volto alla correzione di eventuali esiti anatomici che persistono nonostante la terapia causale abbia sfruttato appieno il potenziale di guarigione del paziente48.
In presenza di tasche parodontali inferiori a 6 mm, nella maggior parte dei casi la sola terapia causale è sufficiente a ripristinare una profondità del solco gengivale compatibile con il mantenimento a livello domiciliare dell’igiene orale sub-gengivale, rendendo la terapia chirurgica non necessaria. Tomasi et al. riportano infatti un successo del 94 e 84% rispettivamente nella terapia causale di tasche di 5 e 6 mm in elementi mono-radicolati50.
Nel trattamento in singola seduta del paziente non collaborante, in cui viene meno la possibilità di impostare un trattamento di lunga durata comprensivo di sedute di terapia causale, terapia motivazionale e rivalutazione, risulta indispensabile attuare un approccio più radicale, strettamente finalizzato al ripristino di condizioni anatomiche compatibili con il mantenimento dell’igiene orale domiciliare a livello sub-gengivale.
Secondo l’esperienza riportata dagli autori, in presenza di sondaggio superiore a
6 mm (Tomasi et al. riportano un successo nella terapia causale di elementi monoradicolati del 63% con sondaggio 7 mm, 36% con 8 mm e 15% con 9 mm)50 e/o evidenza radiografica di un’anatomia ossea ad architettura negativa e/o riscontro di fattori prognostici negativi quali l’interessamento delle forcazioni radicolari51, quadri di malattia parodontale normalmente approcciati con terapia causale e motivazionale, abbinate a rivalutazioni seriate, trovano un’indicazione immediata a una terapia chirurgica, comprensiva di SRP a cielo aperto e chirurgia ossea.
Parimenti, elementi con prognosi significativamente compromessa, normalmente approcciati con un trattamento parodontale convenzionale a ridotta predicibilità, vengono generalmente estratti. L’impossibilità di seguire regolarmente il paziente con sedute di richiamo ravvicinate, e di pianificare un trattamento a lungo termine suddiviso in molteplici incontri, limita significativamente l’efficacia della terapia parodontale nei casi complessi.
Gli autori ritengono pertanto che tale approccio rappresenti un valido compromesso fra efficacia e invasività, volto a ripristinare rapidamente la capacità del paziente di mantenere un’adeguata igiene orale domiciliare a livello sub-gengivale.
Procedure chirurgiche, rigenerative e implantari
Il trattamento in singola seduta in anestesia generale consente un’agevole esecuzione delle procedure di chirurgia orale, primariamente di tipo estrattivo, pre-protesico e bioptico. La possibilità di eseguire procedure chirurgiche avanzate di tipo implantare e/o rigenerativo è strettamente limitata in quanto, al pari della terapia parodontale, queste risentono dell’impossibilità di suddividere il trattamento in più incontri e di rivalutare regolarmente il paziente attraverso sedute di richiamo e di motivazione all’igiene orale52-54. Perciò, la riabilitazione implanto-protesica deve essere limitata a quei casi ove è possibile ottenere una buona collaborazione del paziente per le manovre di igiene orale e, in particolare, a quelle situazioni in cui non esiste alternativa di pari efficacia alla sostituzione di denti mancanti.
Conclusioni
Il trattamento odontoiatrico del paziente non collaborante attraverso una singola seduta terapeutica in regime di anestesia generale costituisce una soluzione efficace ed efficiente nel ripristino di un buono stato di salute orale. Tuttavia, tale approccio richiede molteplici compromessi nelle fasi di progettazione e conduzione del piano di trattamento, in particolare sotto l’aspetto parodontale e protesico, in seguito alla difficoltà di ottenere un’adeguata collaborazione del paziente in merito alle manovre di igiene orale domiciliare e alla possibilità di eseguire controlli clinici frequenti. Gli autori sono concordi nell’affermare che nonostante le difficoltà sopracitate sia possibile curare la dentatura residua di questi pazienti anche in presenza di malattia parodontale, limitando il più possibile l’estrazione degli elementi dentali compromessi.
Corrispondenza
Matteo Chiapasco
Unità Clinica di Chirurgia Orale - Clinica odontostomatologica Dipartimento di scienze della salute Università degli studi di Milano
Via Beldiletto 1 - 20142 Milano
matteo.chiapasco@unimi.it
Unità clinica di chirurgia orale (direttore: prof. Matteo Chiapasco) Clinica odontostomatologica - Dipartimento di scienze della salute - Università degli studi di Milano
1. Ohtawa Y, Tsujino K, Kubo S, Ikeda M. Dental treatment for patients with physical or mental disability under general anesthesia at Tokyo Dental College Suidobashi Hospital. Bull Tokyo Dent Coll 2012;53(4):181-7.
2. Loyola-Rodriguez JP, Zavala-Alonso V, Patiño-Marin N, Friedman C. A new classification system for dental treatment under general anesthesia. Spec Care Dentist 2006 Jan-Feb;26(1):25-9.
3. Jamjoom MM, al-Malik MI, Holt RD, el-Nassry A. Dental treatment under general anaesthesia at a hospital in Jeddah, Saudi Arabia. Int J Paediatr Dent 2001 Mar;11(2):110-6.
4. Dionne RA, Gordon SM, McCullagh LM, Phero JC. Assessing the need for anesthesia and sedation in the general population. J Am Dent Assoc 1998 Feb;129(2):167-73.
5. Slovin M, Falagario-Wasserman J. Special needs of anxious and phobic dental patients. Dent Clin North Am 2009 Apr;53(2):207-19,viii.
6. D’Eramo EM. Morbidity and mortality with outpatient anesthesia: the Massachusetts experience. J Oral Maxillofac Surg 1992 Jul;50(7):700-4.
7. Savanheimo N, Sundberg SA, Virtanen JI, Vehkalahti MM. Dental care and treatments provided under general anaesthesia in the Helsinki Public Dental Service. BMC Oral Health 2012 Oct 27;12:45.
8. Sun L. Early childhood general anaesthesia exposure and neurocognitive development. Br J Anaesth 2010;105(Suppl 1):i61-i68.
9. Stratmann G. Review article: neurotoxicity of anesthetic drugs in the developing brain. Anesth Analg 2011;113:1170-9.
10. Wong A. Treatment planning considerations for adult oral rehabilitation cases in the operating room. Dent Clin North Am 2009 Apr;53(2):255-67,ix.
11. Berggren U. Long-term effects of two different treatments for dental fear and avoidance. J Dent Res 1986 Jun;65(6):874-6.
12. Hakeberg M, Berggren U, Carlsson SG, Gröndahl HG. Long-term effects on dental care behavior and dental health after treatments for dental fear. Anesth Prog 1993;40(3):72-7.
13. Wolff A, Singer A, Shlomi B. Comprehensive dental treatment under general anaesthesia. Dental Cadmos 2014;82(3):182-8.
14. Abdulwahab M, Al-Sayegh F, Boynes S, Abdulwahab H, Zovko J, Close J. Assessing the need for anesthesia and sedation services in Kuwaiti Dental Practice. Anesth Prog 2010;57:91-5.
15. Balogh RS, Ouellette-Kuntz H, Hunter DJ. Regional variation in dental procedures among people with an intellectual disability, Ontario, 1995-2001. J Can Dent Assoc 2004;70:681.
16. Little JW, Falace DA, Miller CS, Rhodus NL. Dental management of the medically compromised patient. St. Louis: Mosby, 2002, 6th ed:1-20.
17. Ide M, Aoyagi Y, Hoshi M, Moriyasu K, Takano F, Asada Y. A survey of the actual status of the dental treatment under general anesthesia at pediatric dentistry clinic of university dental hospital. J Jpn Ped Dent 2003;41:694-9.
18. Ono S, Honma S, Kasa Y, Obata M, Kondo T, Ishida Y, Tokura S, Kawada I. Clinical observation of the dental treatment for the handicapped under general anesthesia in our hospital during the past 9 years. J Jpn Soc Disability Oral Health 2003;24:186-192.
19. Yasuda J, Iwata K, Ohyama Y, Tanabe S, Nishitouge K, Harada J, Iwayama Y. Clinical study of the dental treatments under general anesthesia for disabled – Statistical survey in our hospital during the past 10 years. J Jpn Soc Disability Oral Health 2001;22:1-7.
20. O’Sullivan EA, Curzon ME. The efficacy of comprehensive dental care for children under general anesthesia. British Dental Journal 1991;171:56-8.
21. Deegan AE. Anesthesia morbidity and mortality, 1988-1999: claims statistics from AAOMS National Insurance Company. Anesth Prog 2001 Summer;48(3):89-92.
22. Tomlin PJ. Death in outpatient dental anaesthetic practice. Anaesthesia 1974 Sep;29(5):551-70.
23. Lytle JJ, Stamper EP. The 1988 anesthesia survey of the Southern California Society of Oral and maxillofacial surgeons. J Oral Maxillofac Surg 1989 Aug;47(8):834-42.
24. D’Eramo EM. Morbidity and mortality with outpatient anesthesia: the Massachusetts experience. J Oral Maxillofac Surg. 1999 May;57(5):531-6.
25. D’Eramo EM, Bookless SJ, Howard JB. Adverse events with outpatient anesthesia in Massachusetts. J Oral Maxillofac Surg. 2003 Jul;61(7):793-800.
26. Gan TJ, Ginsberg B, Grant AP, Glass PS. Double-blind, randomized comparison of ondansetron and intraoperative propofol to prevent postoperative nausea and vomiting. Anesthesiology 1996 Nov;85(5):1036-42.
27. Saklad M. Grading of patients for surgical procedures. Anesthesiology 1941;2:281-4.
28. O’Halloran M. The use of anaesthetic agents to provide anxiolysis and sedation in dentistry and oral surgery. Australas Med J 2013 Dec 31;6(12):713-8.
29. Dorman ML, Wilson K, Stone K, Stassen LF. Is intravenous conscious sedation for surgical orthodontics in children a viable alternative to general anaesthesia? A case review. Br Dent J 2007 Jun 9;202(11):E30.
30. Lahoud GY, Averley PA. Comparison of sevoflurane and nitrous oxide mixture with nitrous oxide alone for inhalation conscious sedation in children having dental treatment: a randomised controlled trial. Anaesthesia 2002 May;57(5):446-50.
31. Haraguchi N, Furusawa H, Takezaki R, Oi K. Inhalation sedation with sevoflurane: a comparative study with nitrous oxide. J Oral Maxillofac Surg 1995;53:24-6.
32. Ganzberg S, Weaver J, Beck FM, McCaffrey G. Use of sevoflurane inhalation sedation for outpatient third molar surgery. Anesth Prog 1999 Winter;46(1):21-9.
33. Girdler NM, Hill CM, Wilson KE. Clinical sedation in dentistry. Oxford: Wiley-Blackwell, 2009, 1st ed.
34. Malamed SF. Sedation: A guide to patient management. 4th ed. St. Louis (Mo): Mosby; 2003. p. 26-54.
35. Prabhu NT, Nunn JH, Evans DJ, Girdler NM. Development of a screening tool to assess the suitability of people with a disability for oral care under sedation or general anesthesia. Spec Care Dentist 2008 Jul-Aug;28(4):145-58.
36. Girdler NM, Rynn D, Lyne JP, Wilson KE. A prospective randomised controlled study of patient-controlled propofol sedation in phobic dental patients. Anaesthesia 2000 Apr;55(4):327-33.
37. Robb ND, Hosey MT, Leitch JA. Intravenous conscious sedation in patients under 16 years of age. Fact or fiction? Br Dent J 2003;194:469-71.
38. Averley PA, Girdler NM, Bond S, Steen N, Steele J. A randomised control trial of paediatric conscious sedation for dental treatment using intravenous midazolam combined with inhaled nitrous oxide or nitrous oxide/sevoflurane. Anaesthesia 2004;59:844-52.
39. Matthews RW, Malkawi Z, Griffiths MJ, Scully C. Pulse oximetry during minor oral surgery with and without intravenous sedation. Oral Surg Oral Med Oral Pathol 1992 Nov;74(5):537-43.
40. Saraghi M, Badner VM, Golden LR, Hersh EV. Propofol: an overview of its risks and benefits. Compend Contin Educ Dent 2013 Apr;34(4):252-8.
41. Lambert C. Sexual phenomena hypnosis and nitrous oxide sedation. J Am Dent Assoc 1982 Dec;105(6):990-1.
42. Nunn JF, Sharer N, Royston D, Watts RW, Purkiss P, Worth HG. Serum methionine and hepatic enzyme activity in anaesthetists exposed to nitrous oxide. Br J Anaesth 1982 Jun;54(6):593-7.
43. Sweeney B, Bingham RM, Amos RJ, Petty AC, Cole PV. Toxicity of bone marrow in dentists exposed to nitrous oxide. Br Med J (Clin Res Ed) 1985 Aug 31;291(6495):567-9.
44. Gargiulo AW, Wentz FM, Orban B. Dimensions and relations of the dentogingival junction in humans. J Periodontol 1961;32:261-7.
45. Figini L, Lodi G, Gorni F, Gagliani M. Single versus multiple visits for endodontic treatment of permanent teeth. Cochrane Database Syst Rev 2007 Oct 17;(4):CD005296.
46. Fasbinder DJ. Clinical performance of chairside CAD/CAM restorations. J Am Dent Assoc 2006 Sep;137 Suppl:22S-31S.
47. Otto T. Computer-aided direct all-ceramic crowns: preliminary 1-year results of a prospective clinical study. Int J Periodontics Restorative Dent 2004 Oct;24(5):446-55.
48. Lindhe J, Lang NP, Thorkild K. Clinical periodontology and implant dentistry. Blackwell Munksgaard, 2008, 5th ed:655-74.
49.Società italiana di parodontologia. Consensus sul trattamento in parodontologia. Incontro dei soci attivi. Rimini, 13 settembre 2003.
50. Tomasi C, Leyland AH, Wennström JL. Factors influencing the outcome of non-surgical periodontal treatment: a multilevel approach. J Clin Periodontol 2007 Aug;34(8):682-90.
51. Johansson KJ, Johansson CS, Ravald N. The prevalence and alterations of furcation involvements 13 to 16 years after periodontal treatment. Swed Dent J 2013;37(2):87-95.
52. Esposito M, Grusovin MG, Felice P, Karatzopoulos G, Worthington HV, Coulthard P. Interventions for replacing missing teeth: horizontal and vertical bone augmentation techniques for dental implant treatment. Cochrane Database Syst Rev 2009 Oct 7;(4):CD003607.
53. Chen ST, Beagle J, Jensen SS, Chiapasco M, Darby I. Consensus statements and recommended clinical procedures regarding surgical techniques. Int J Oral Maxillofac Implants 2009;24 Suppl:272-8.
54. Chiapasco M, Casentini P, Zaniboni M. Bone augmentation procedures in implant dentistry. Int J Oral Maxillofac Implants 2009;24 Suppl:237-59.