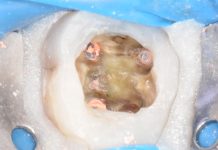
Iatrogenic root perforations. Diagnosis and therapy
Oggi grazie a nuovi materiali, strumenti e tecnologie, la prognosi delle perforazioni è notevolmente migliorata. Molti casi, che anni fa sarebbero stati trattati solo per via chirurgica oppure estratti, possono essere salvati con approccio clinico ortogrado, con altissime percentuali di successo a lungo termine.
Riassunto
L’utilizzo di moderne tecnologie endodontiche e di moderni protocolli portano ad altissime percentuali di successo delle nostre terapie. Ciononostante, talvolta a causa di difficoltà anatomiche o di danni iatrogeni come le perforazioni, il trattamento può non portare ai risultati desiderati. Si rende pertanto necessario il ritrattamento, sia per via convenzionale che, talvolta, per via chirurgica. Oggi grazie alle nuove tecnologie, ai nuovi strumenti e ai nuovi materiali, molti casi che anni fa sarebbero stati trattati solo per via chirurgica oppure estratti, possono essere salvati con approccio clinico ortogrado con altissime percentuali di successo a lungo termine. Il presente articolo ha lo scopo di illustrare gli attuali materiali, strumenti e tecniche che possono essere utilizzati nella pratica quotidiana nella terapia ortograda delle perforazioni iatrogene, allo scopo di salvare denti che altrimenti sarebbero stati trattati chirurgicamente o sarebbero stati estratti e rimpiazzati con impianti.
Summary
The use of modern endodontic techniques and treatment protocols result in high success rates for primary endodontic treatment. Neverthelesss, due to certain anatomical or biological constrains and/or after iatrogenic interference like perforations, treatment might not result in a positive outcome. This may necessitate either conventional or surgical retreatment. Today, thanks to the new technologies, new instruments and new materials, many cases that years before could have been treated only surgically or extracted, can be retreated non-surgically with a very high long tem success rate. The aim of the presentation is to describe modern materials, instruments and techniques that can be used in our every day practice when we perform nonsurgical treatment of iatrogenic perforations, in order to save teeth that otherwise should have been treated surgically or extracted and replaced with implants.

Laureato in Medicina e chirurgia a Firenze nel 1973 e specializzato in Odontoiatria e protesi dentaria nel 1977. Ha frequentato il reparto di Endodonzia del professor H. Schilder presso la Boston University e dal 1980 esercita la professione limitatamente all’endodonzia. È past president della SIE (Società Italiana di Endodonzia) e della IFEA (International Federation of Endodontic Associations). È socio attivo della AAE (American Association of Endodontists) e della ESE (European Society of Endodontology). È fondatore e presidente del “Warm Gutta-Percha Study Club”, relatore a numerosi corsi e conferenze in congressi nazionali e internazionali in Italia ed all’estero ed è autore del libro “Endodonzia”. È fondatore del Centro per l’insegnamento della Micro- Endodonzia, con sede in Firenze, dove insegna e tiene corsi teorico-pratici.
Le perforazioni sono comunicazioni iatrogene tra il sistema dei canali radicolari e l’apparato di sostegno del dente. Il clinico deve stare particolarmente attento per evitare di commettere tale danno nel corso della terapia endodontica, in quanto la perforazione richiede un trattamento addizionale non richiesto. Se è stata eseguita una perforazione, il dente non necessariamente richiede la chirurgia, o l’estrazione o il reimpianto intenzionale. Infatti, può essere trattato con successo per via ortograda e continuare così a funzionare in arcata come se la perforazione non fosse mai stata eseguita. Oggi non c’è alcun motivo per pensare che il dente possa essere perduto prematuramente a causa di questa spiacevole complicazione.
Nel parodonto circostante la sede della perforazione s’instaura una reazione infiammatoria, dovuta sia al trauma meccanico sia all’introduzione di sostanze di derivazione batterica che inevitabilmente si accompagnano alla perforazione stessa.
La perforazione crea una porta di uscita “addizionale” nel sistema dei canali radicolari che richiede di essere sigillata prima possibile, perché una compromissione parodontale insorgente dalla perforazione può col tempo diventare irreversibile e compromettere seriamente la prognosi.
La terapia della perforazione richiede spesso un approccio multidisciplinare, allo scopo di stabilire il più corretto piano di trattamento. Si deve cioè decidere se è il caso di estrarre il dente o rivolgere i nostri sforzi al ritrattamento ortogrado o chirurgico o a entrambi.
Quando si valuta un dente che ha subito una perforazione, si devono considerare quattro variabili: il livello, la sede, le dimensioni e la forma, e infine il tempo1.
- Livello. Le perforazioni possono essere state eseguite a livello del terzo coronale, medio o apicale del dente. La prognosi delle perforazioni radicolari del terzo apicale e del terzo medio è sicuramente migliore rispetto alle perforazioni del terzo coronale o del pavimento della camera pulpare di un pluriradicolato2-7.
- Sede. Le perforazioni possono essere sul lato vestibolare, linguale, mesiale o distale della superficie radicolare. Questo ha importanza nel caso si prenda in considerazione l’approccio chirurgico, mentre non ne ha nel caso del ritrattamento ortogrado.
- Forma e dimensioni. La realizzazione di un buon sigillo dipende innanzitutto dalle dimensioni e dalla forma della perforazione. Più grande è la fresa che esegue la perforazione, maggiore sarà l’area da sigillare. Inoltre, le perforazioni laterali non sono mai rotonde, ma hanno una forma ellittica, in quanto la fresa incontra la parete canalare con un angolo di 45°. La cavità della perforazione inoltre non ha conicità, e questo rende più difficile ottenere un buon sigillo senza disturbare i tessuti parodontali circostanti.
- Tempo. Le perforazioni creano una reazione infiammatoria nei tessuti circostanti e di conseguenza una perdita di attacco. Pertanto, per impedire un’ulteriore perdita di attacco e di supporto parodontale, devono essere sigillate prima possibile, possibilmente nel corso dello stesso appuntamento in cui si sono verificate.
Oltre alle perforazioni iatrogene, si possono riscontrare anche perforazioni spontanee o patologiche dovute a carie o a riassorbimenti interni o esterni. Nell’ambito di questo articolo verranno prese in considerazione le perforazioni che più frequentemente capita di osservare nella routinaria pratica clinica.
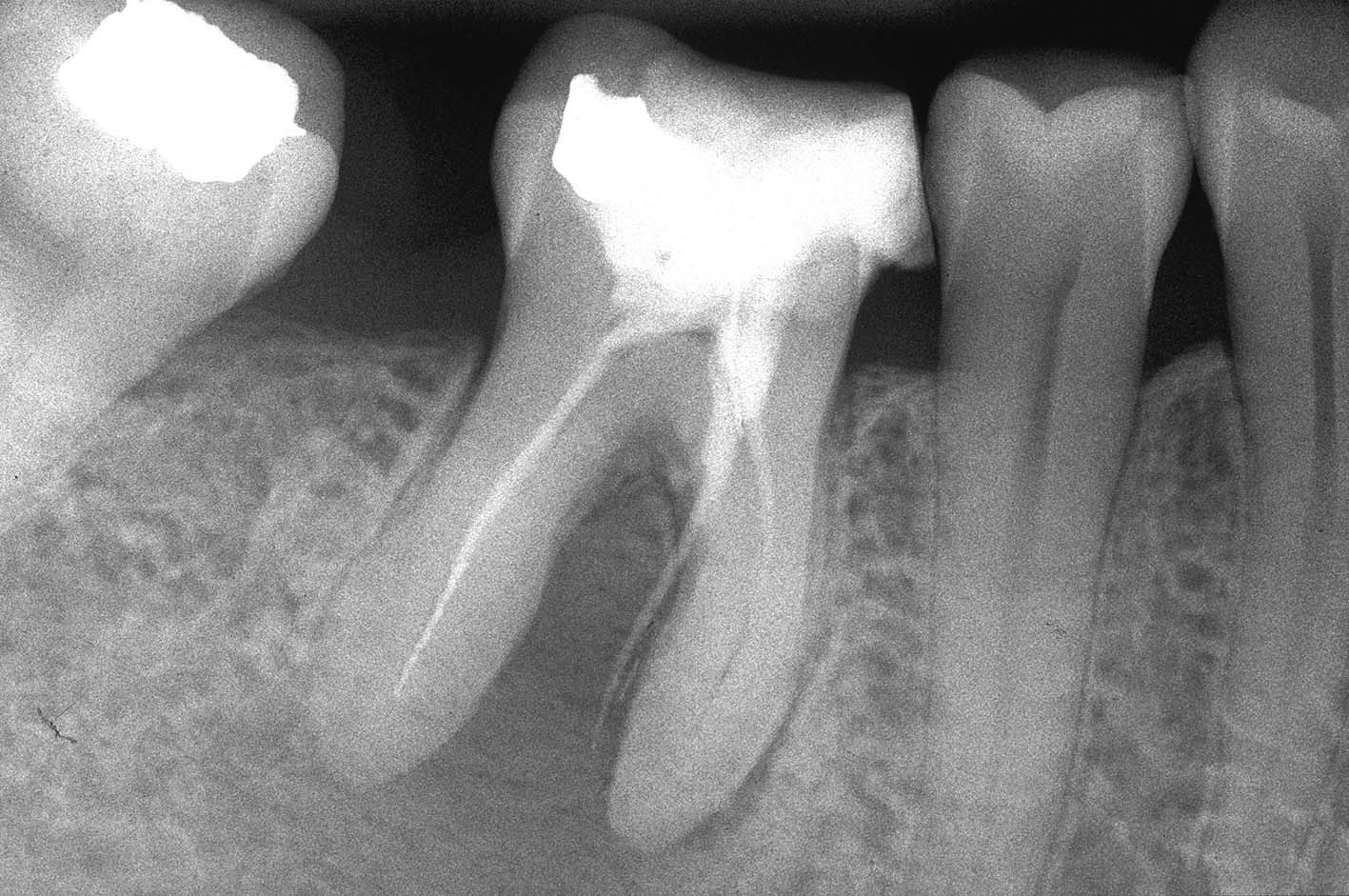
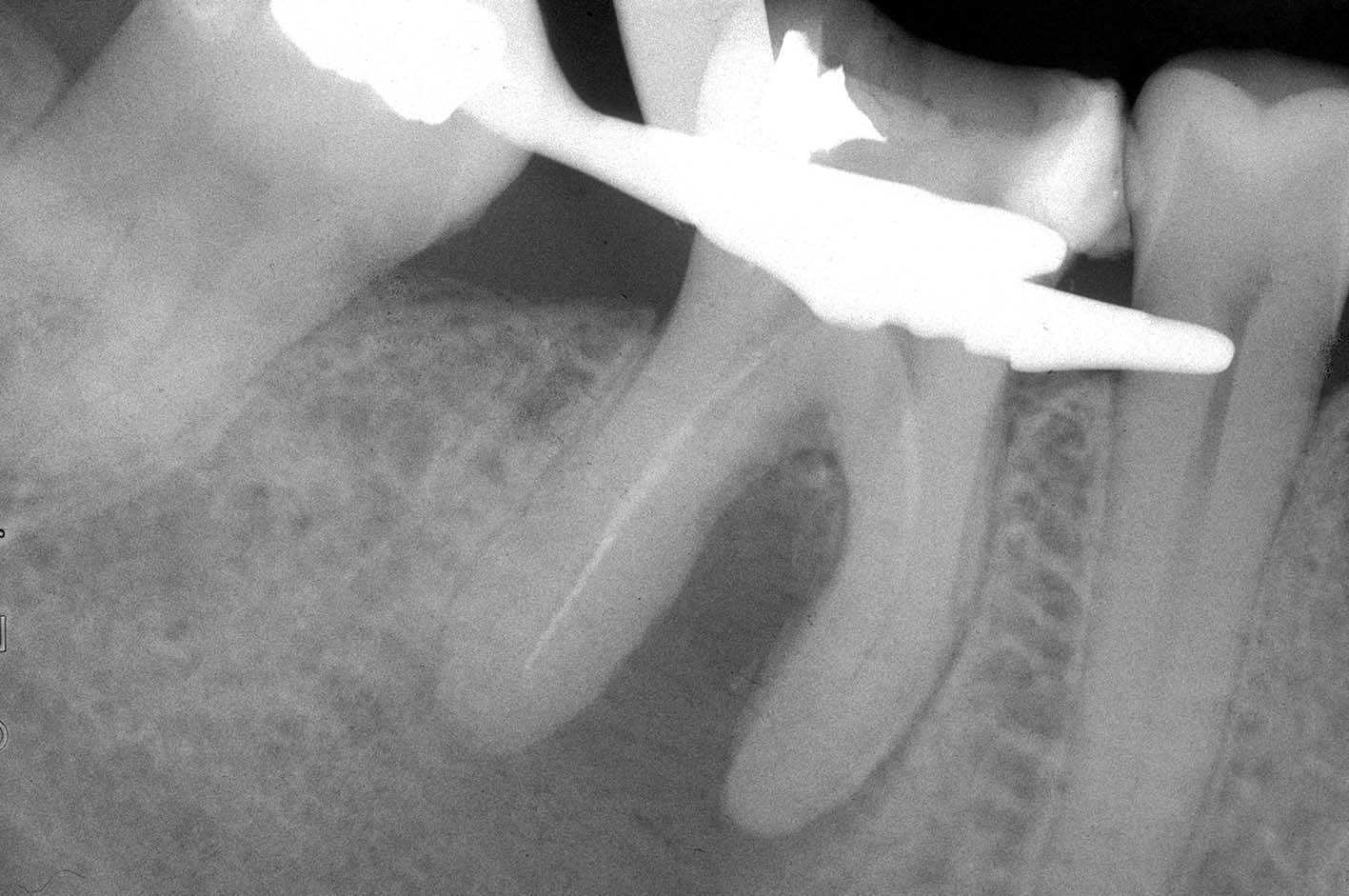
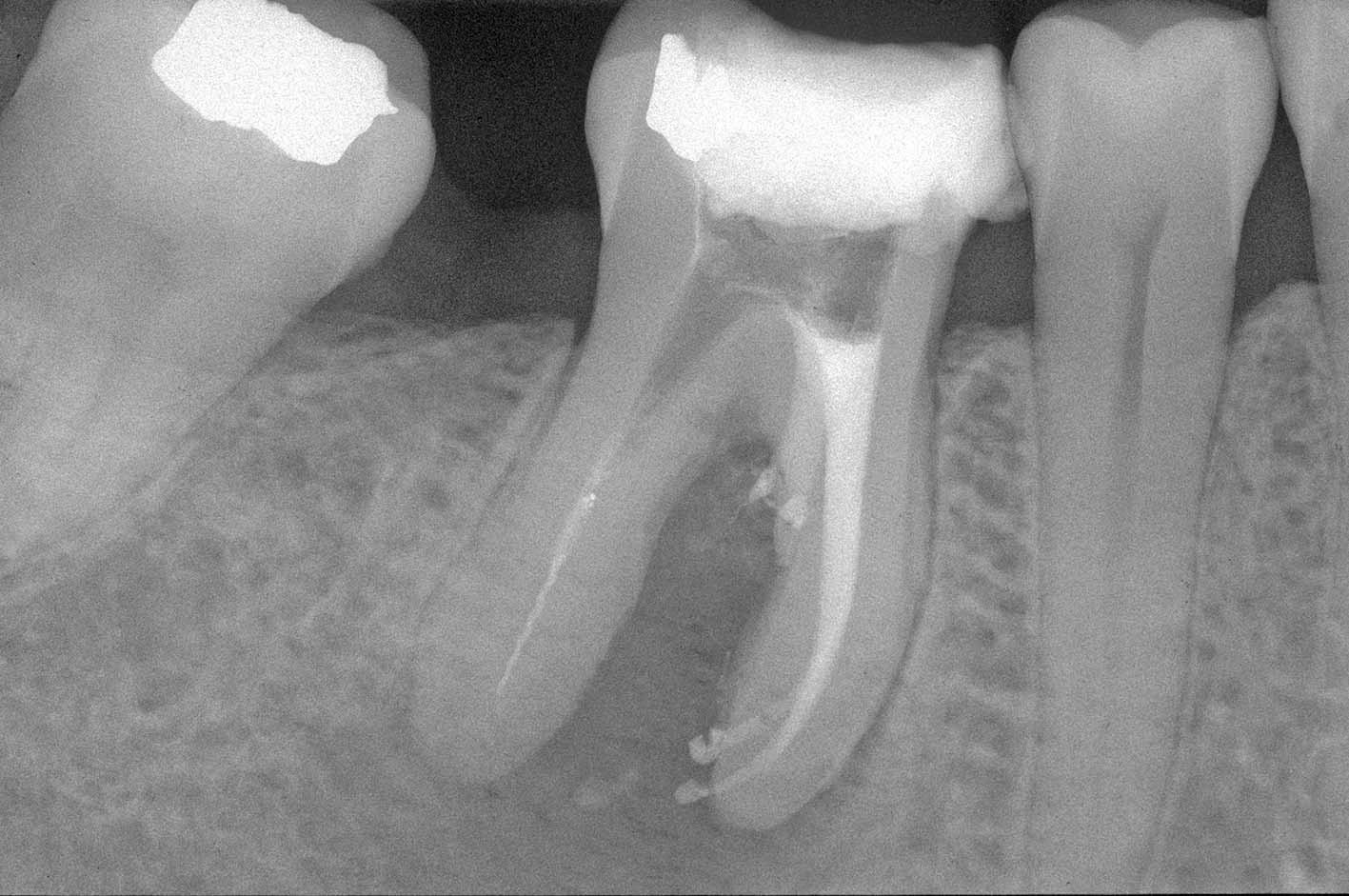
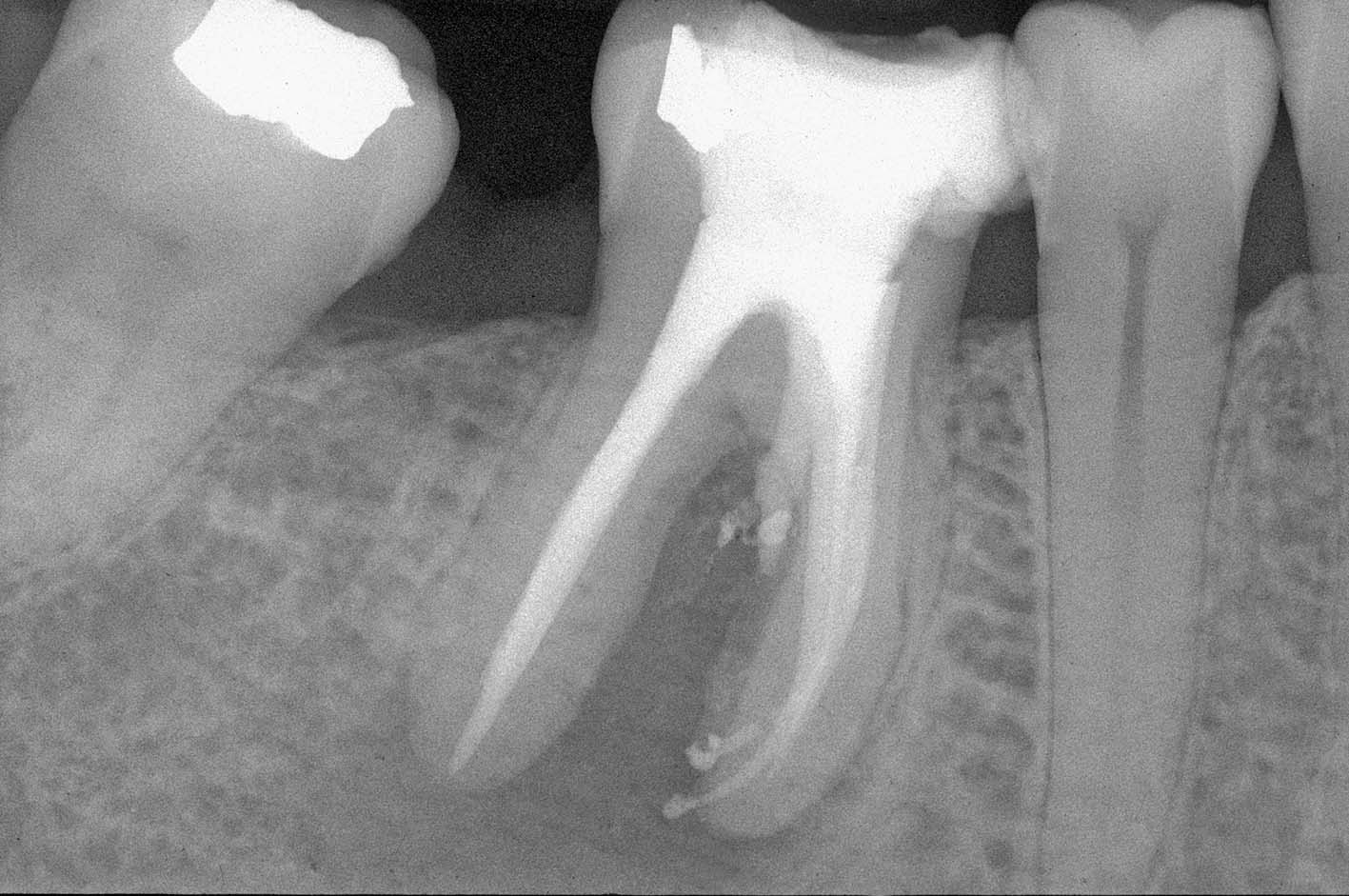
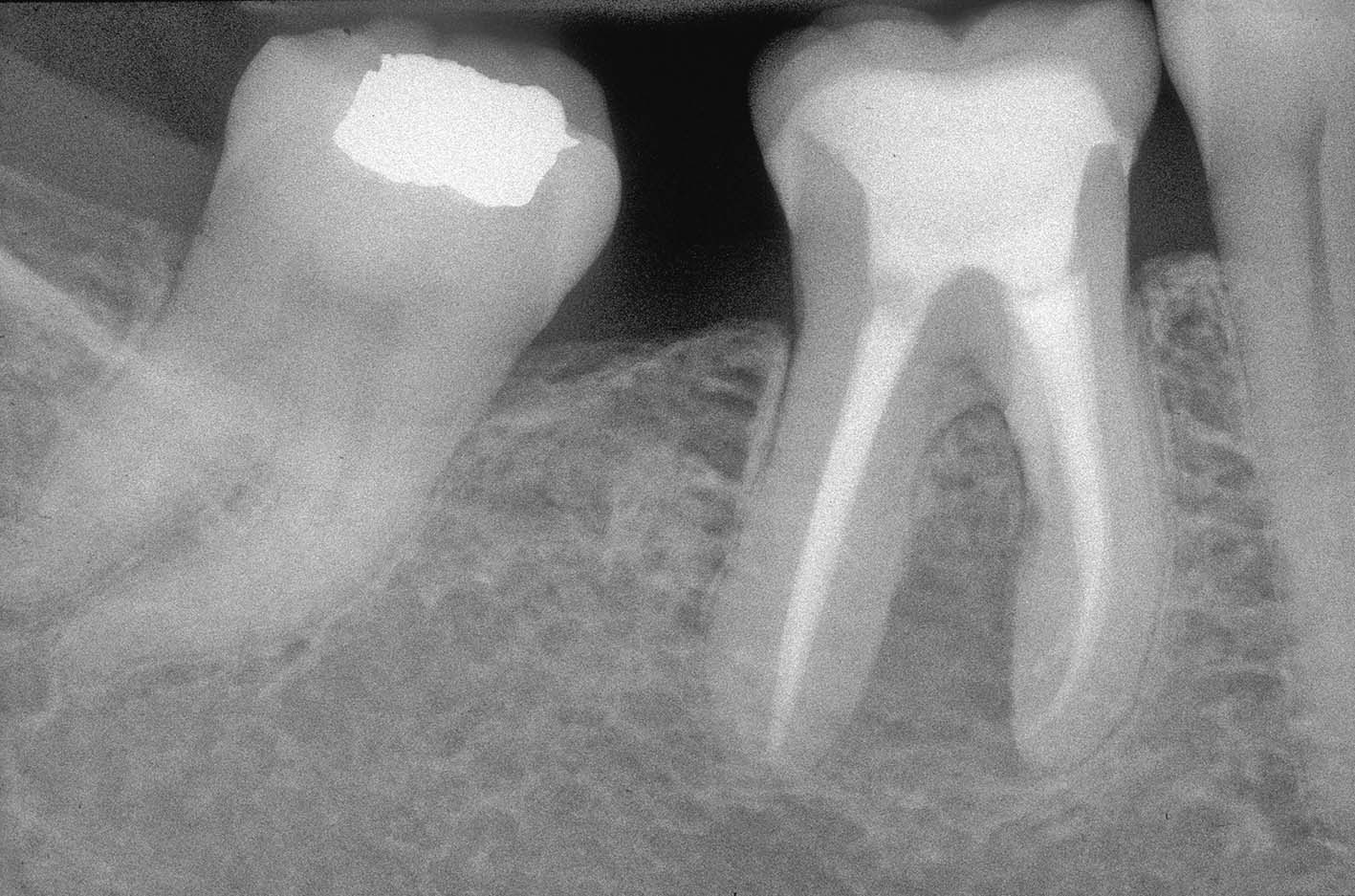
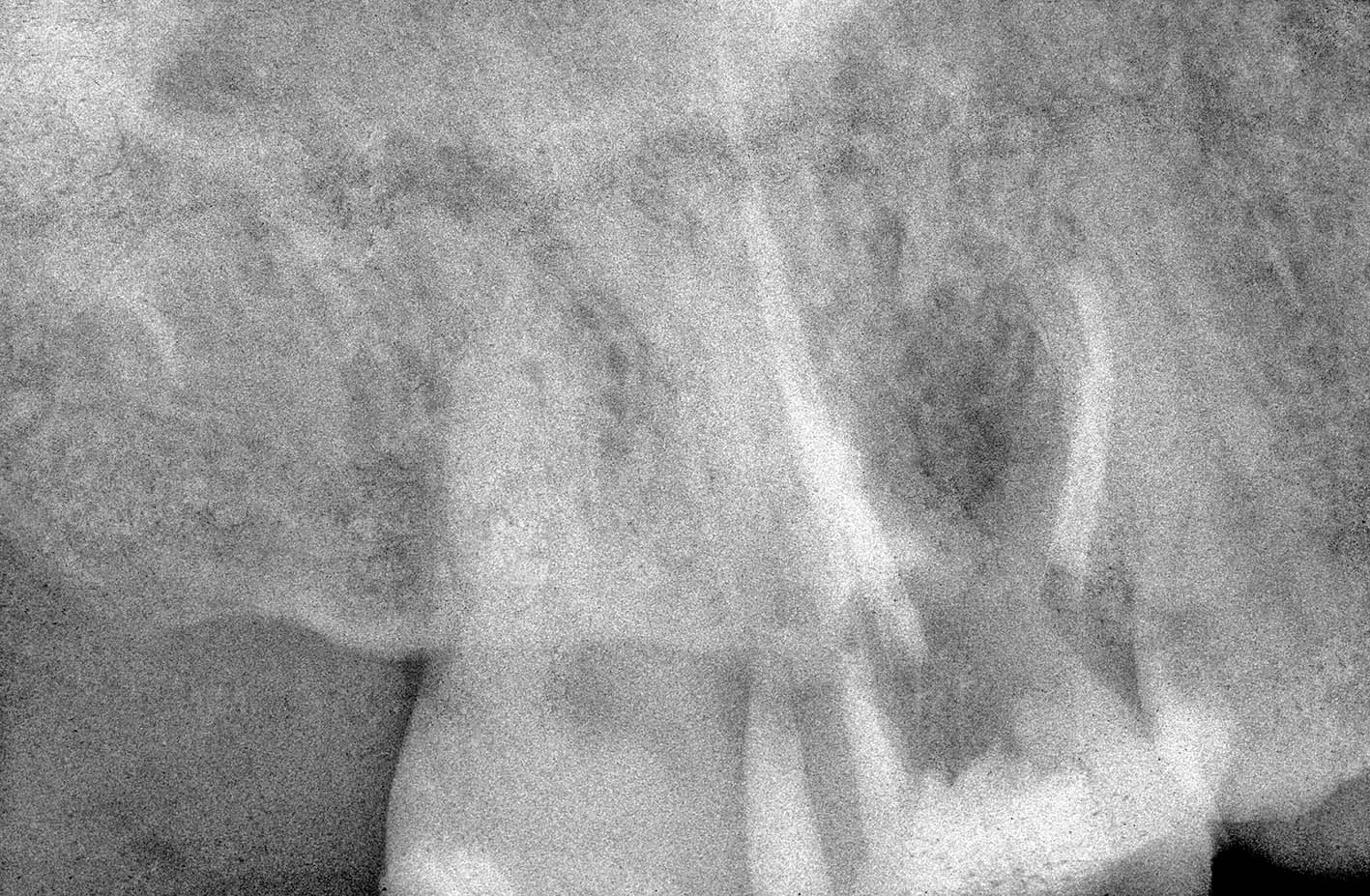
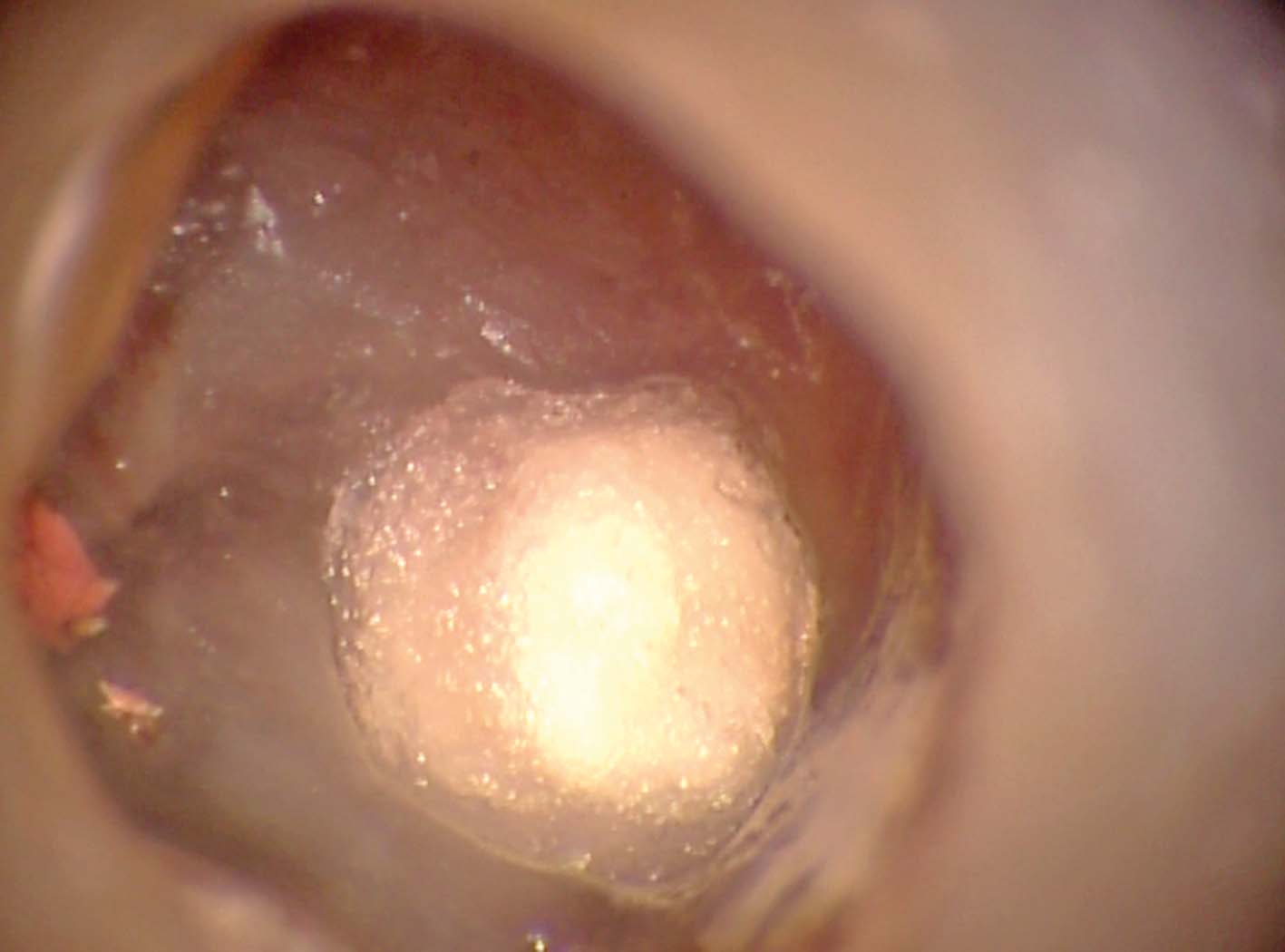
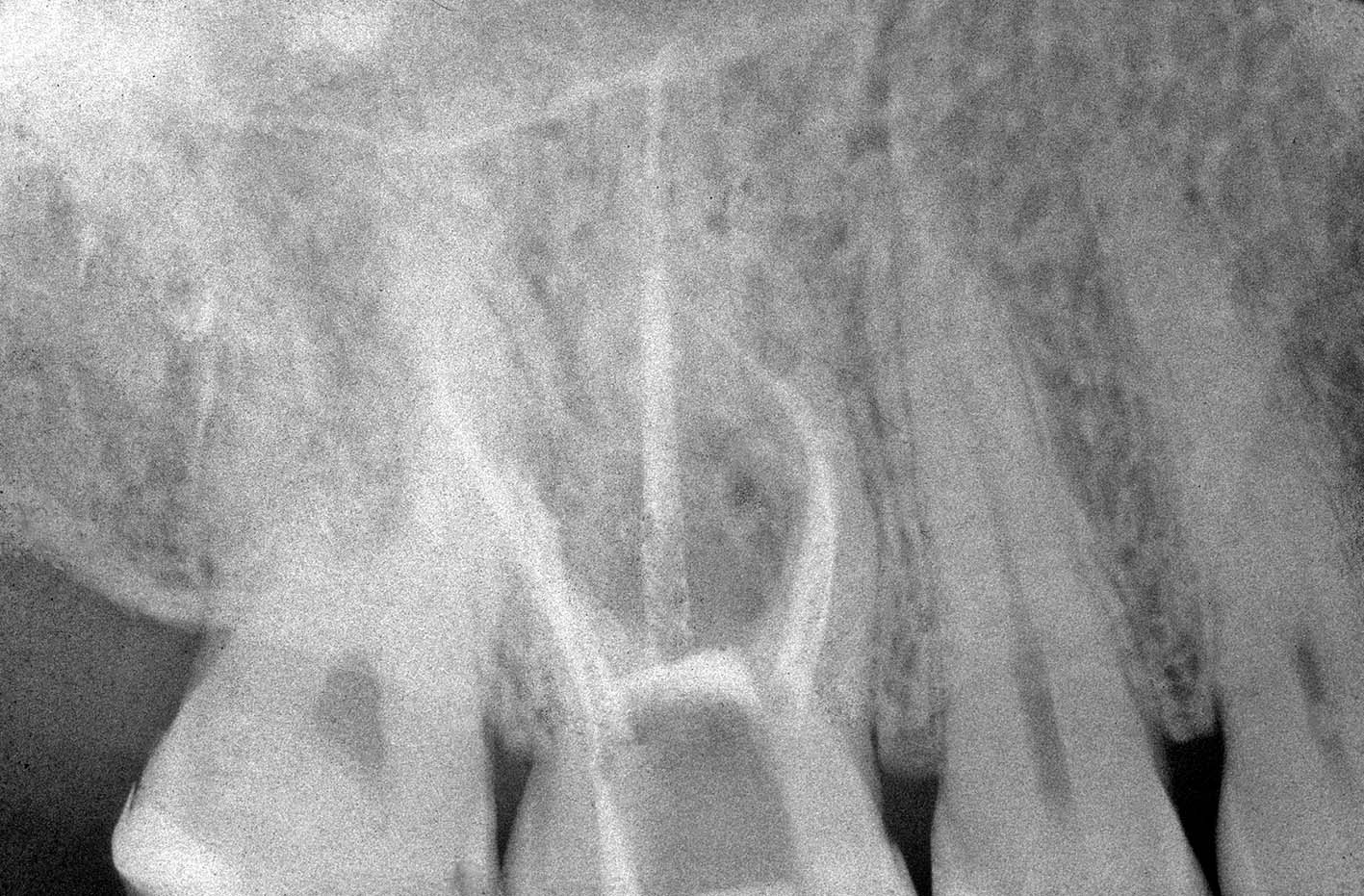
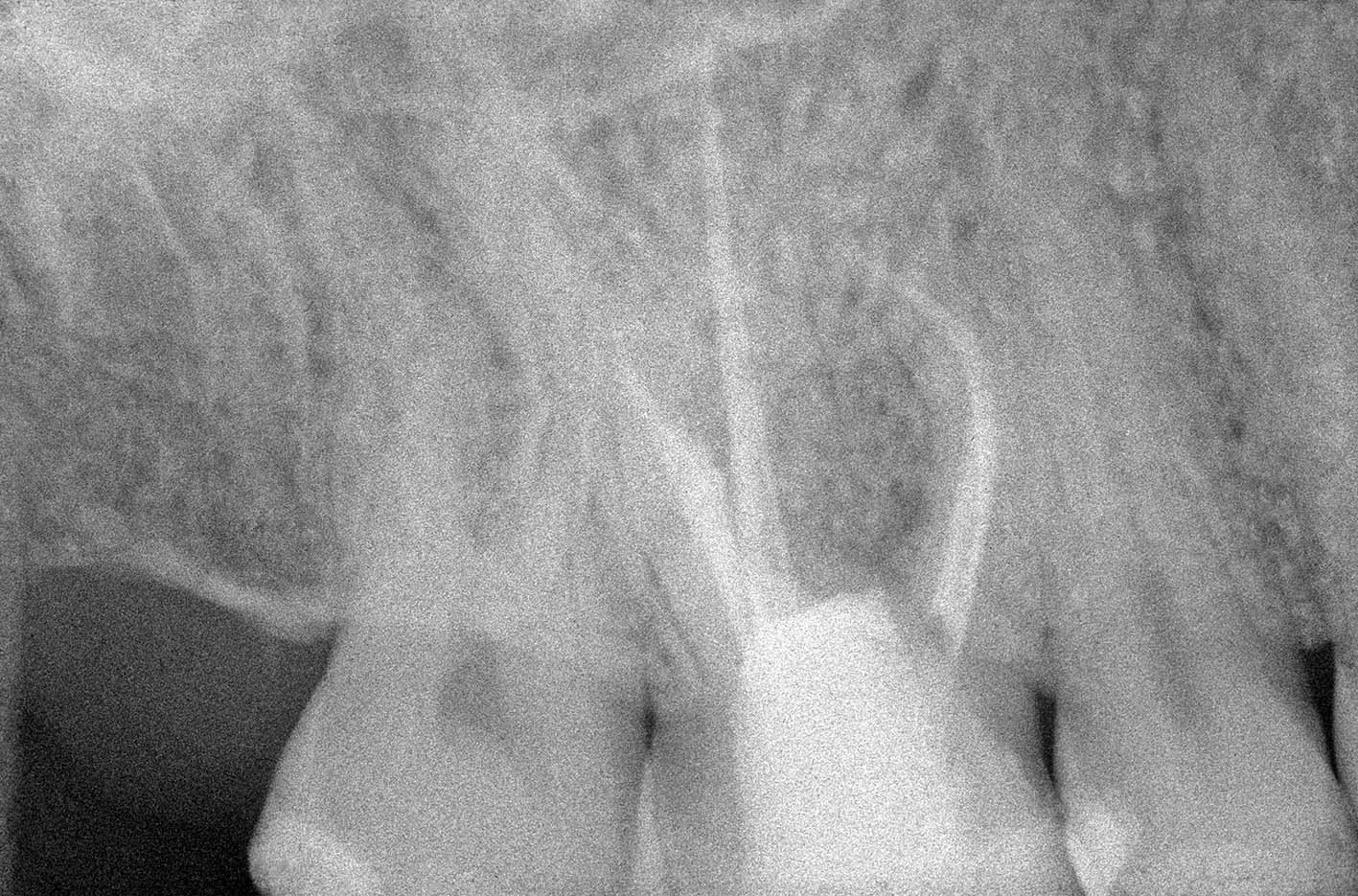
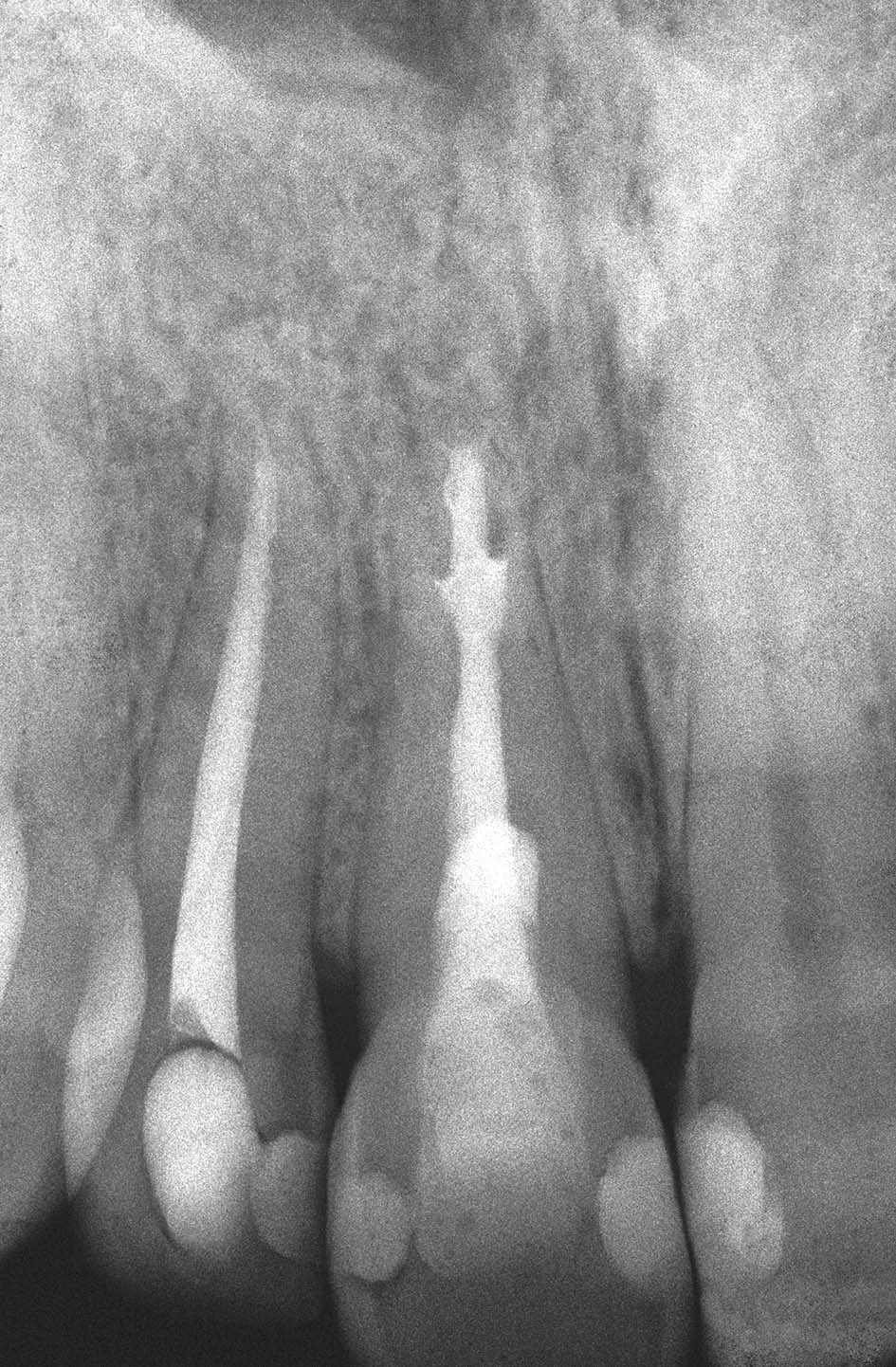
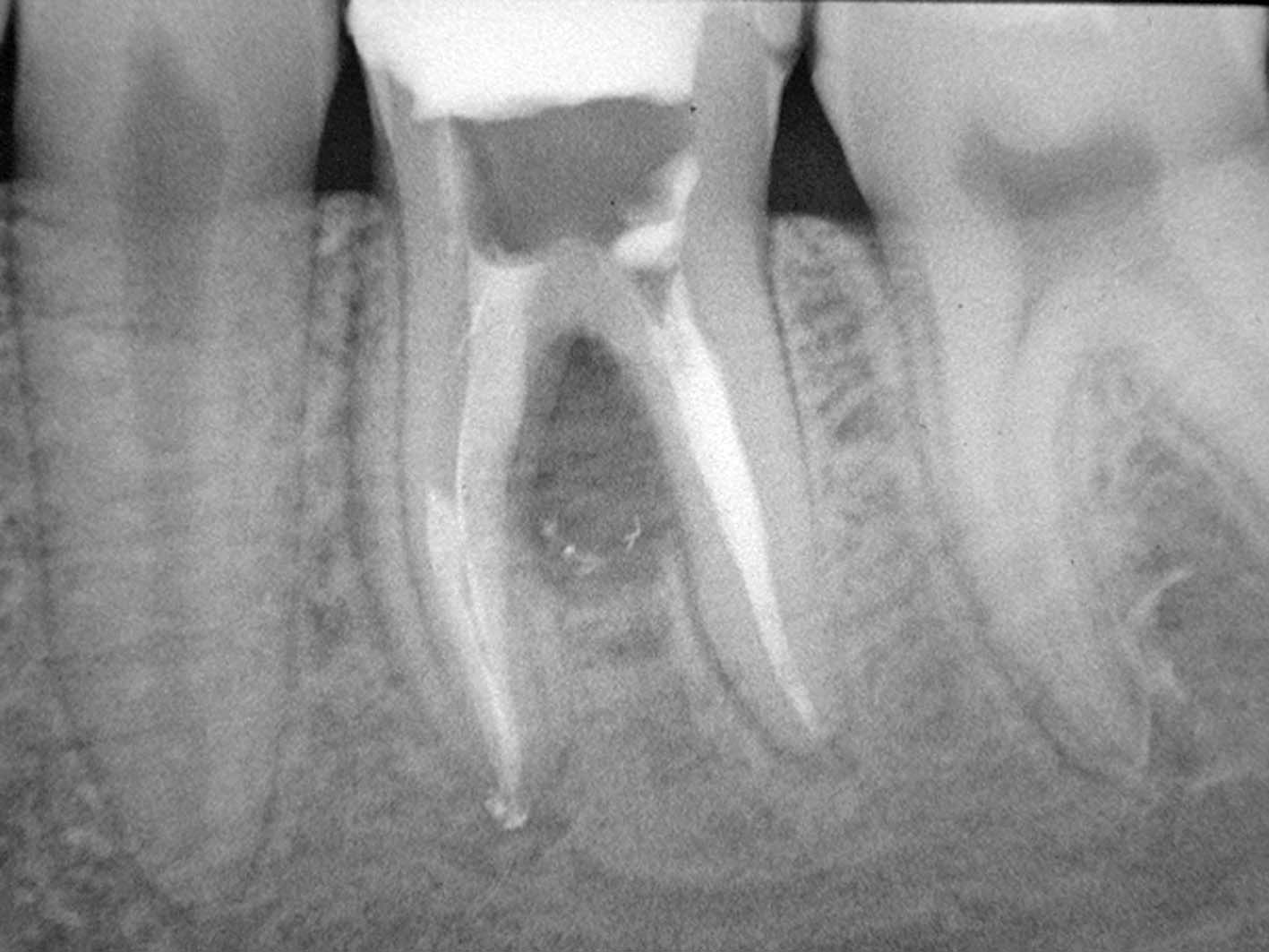
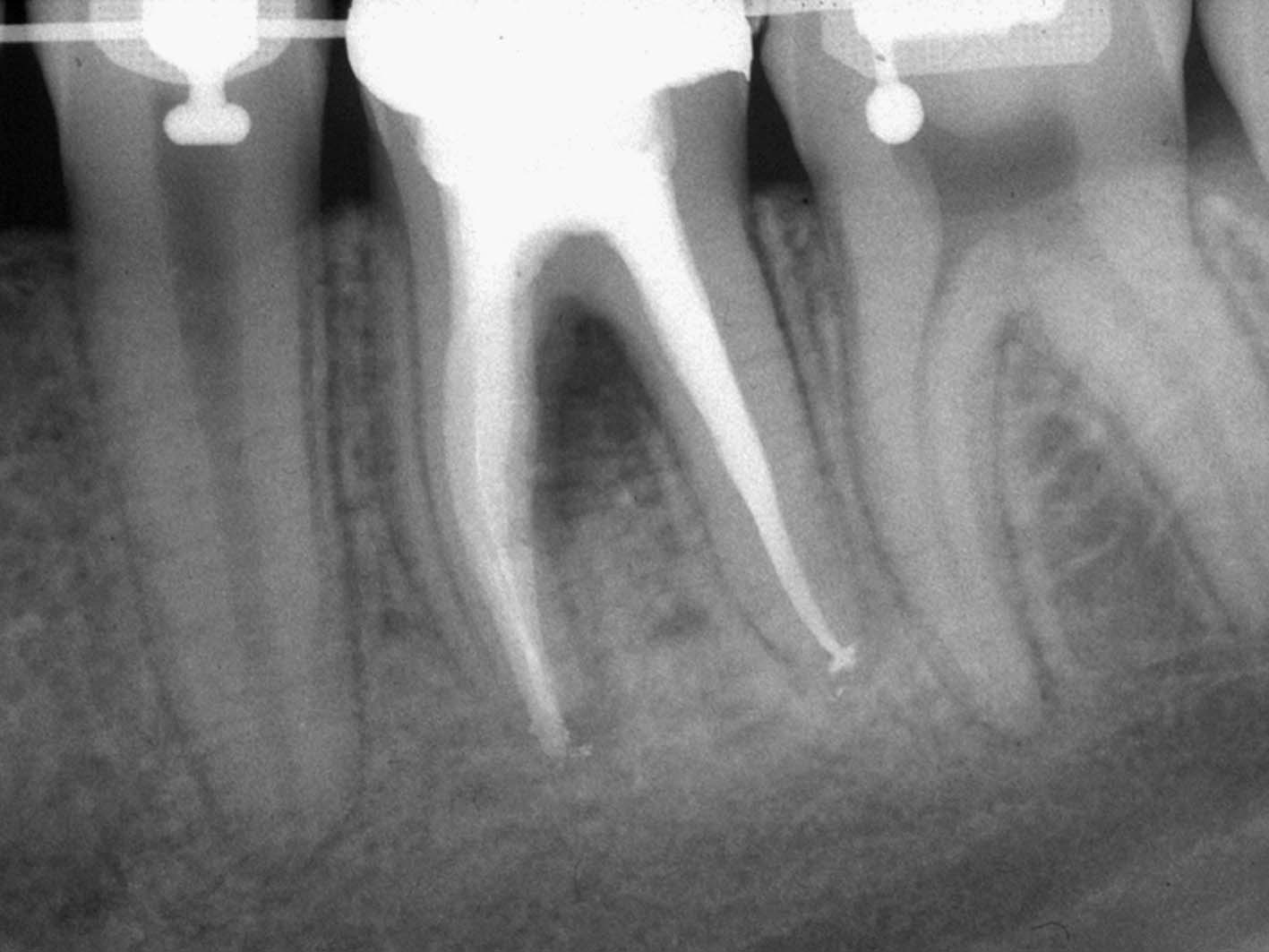
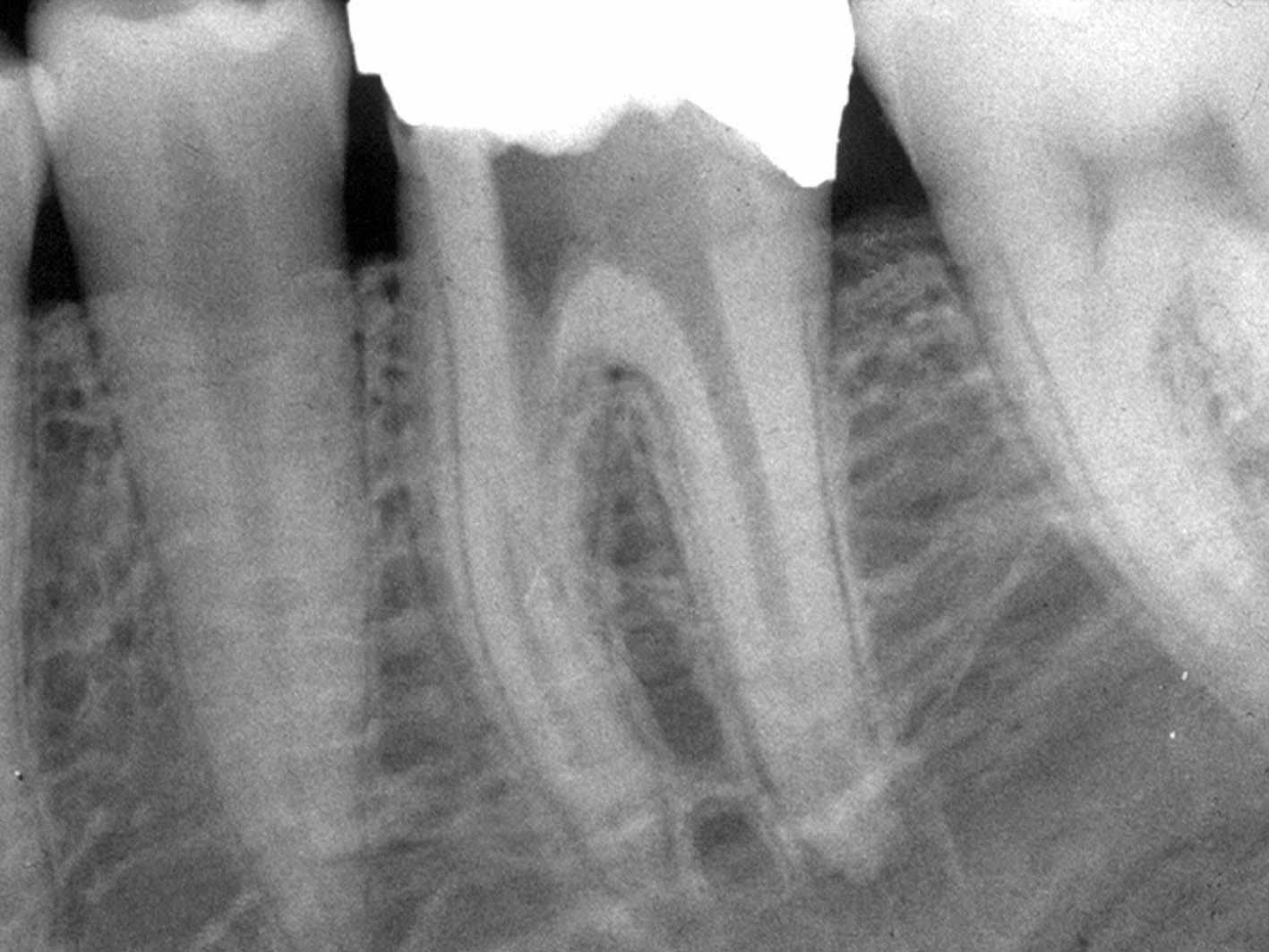
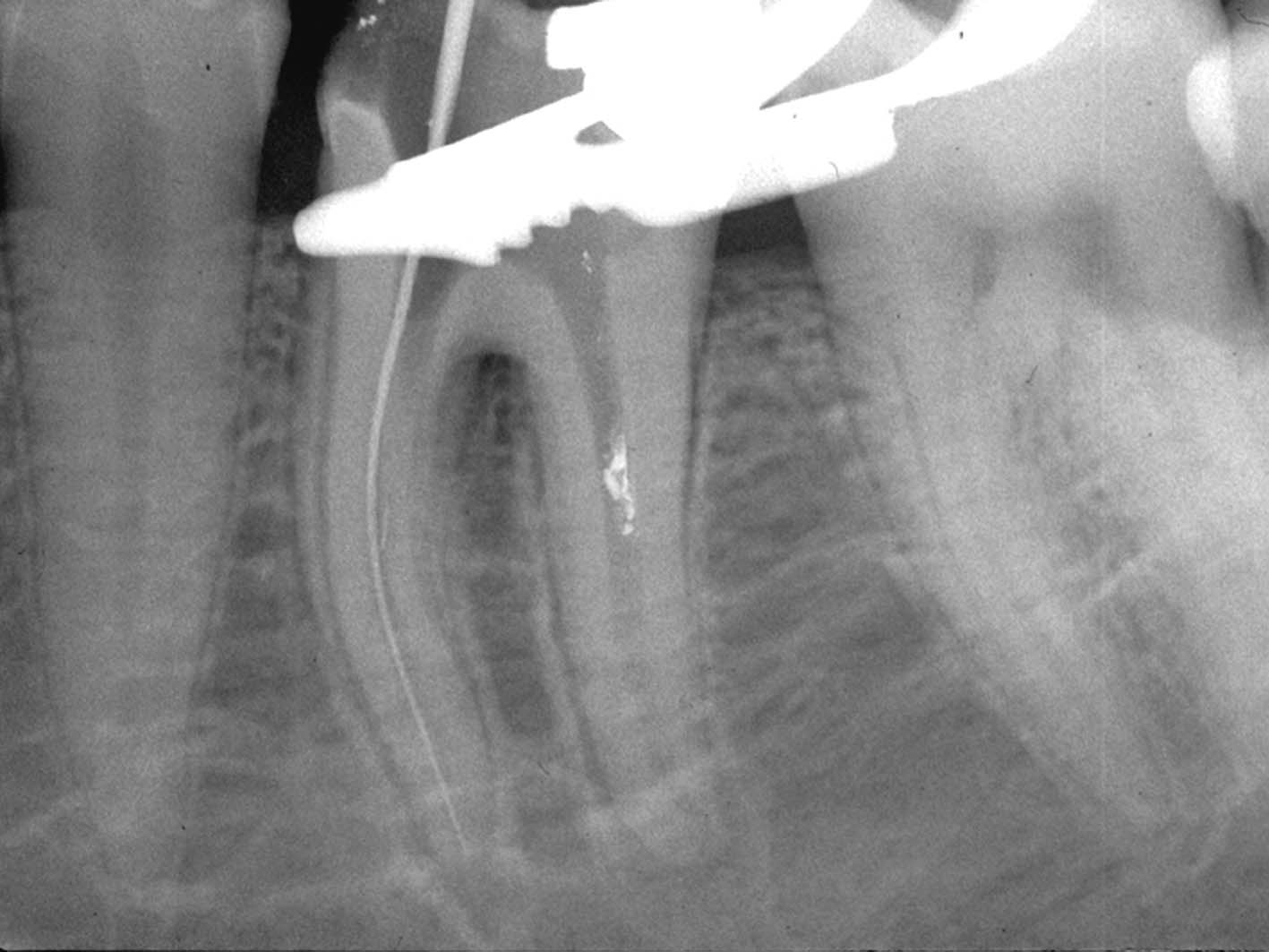
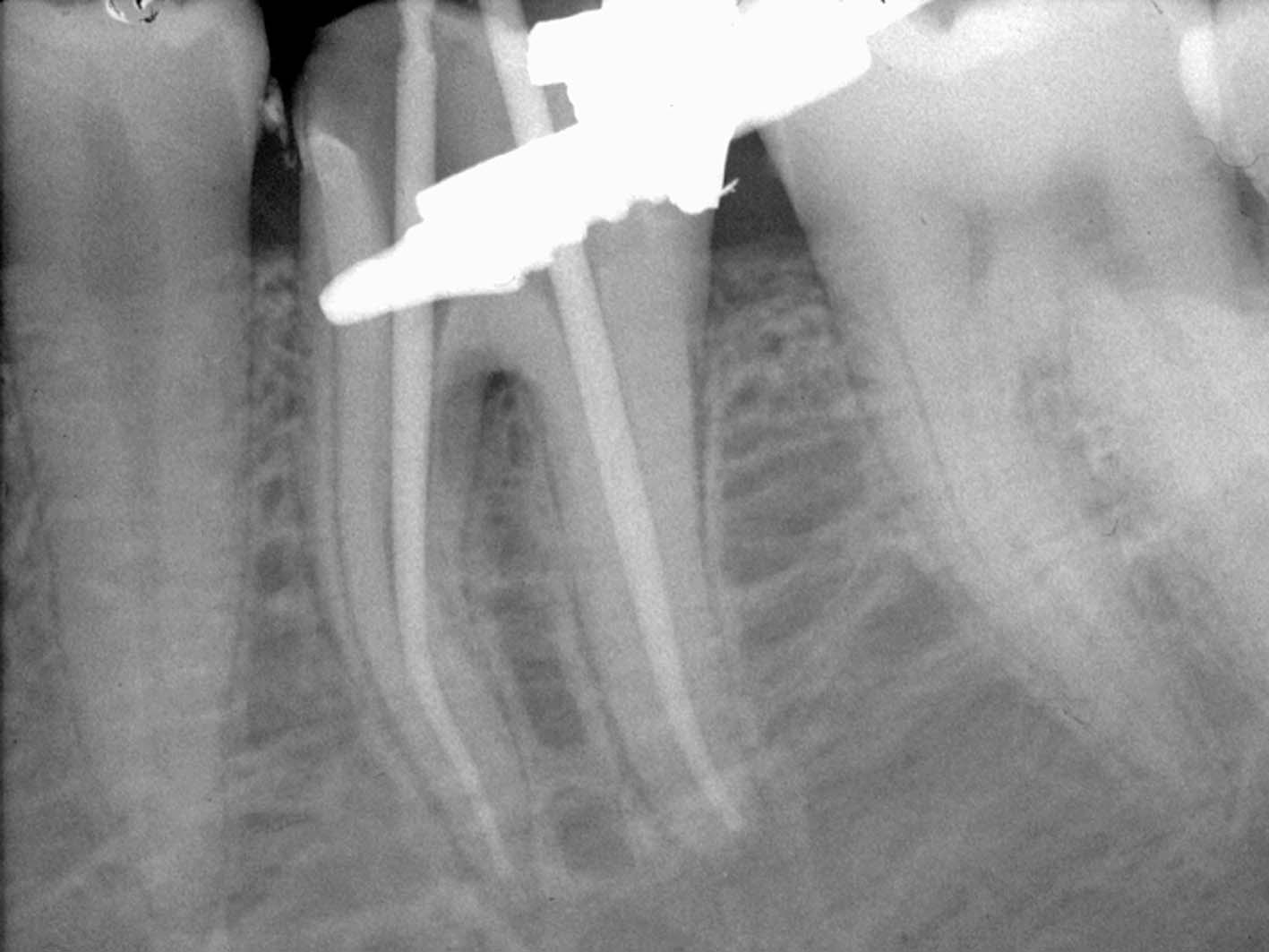
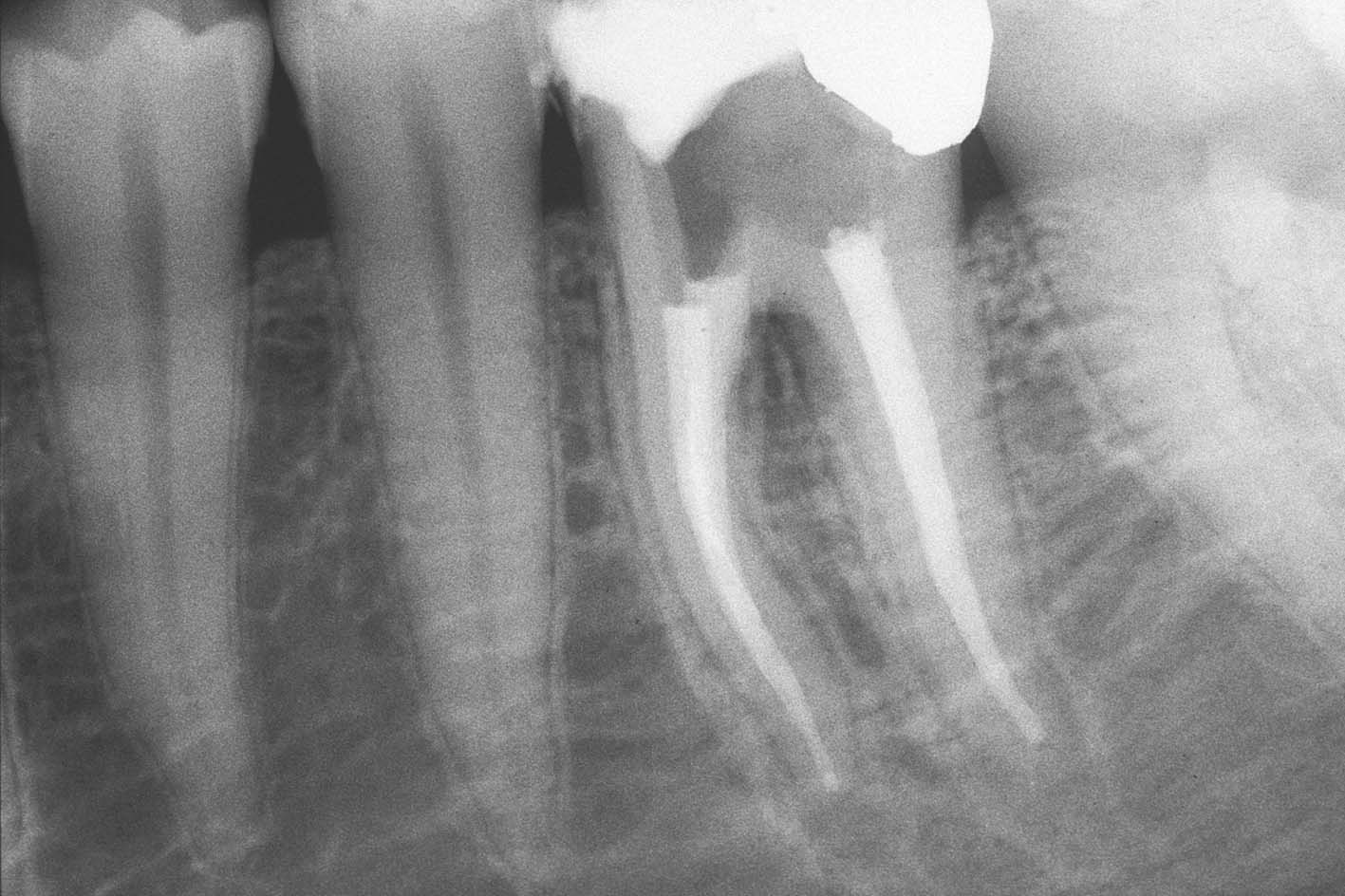
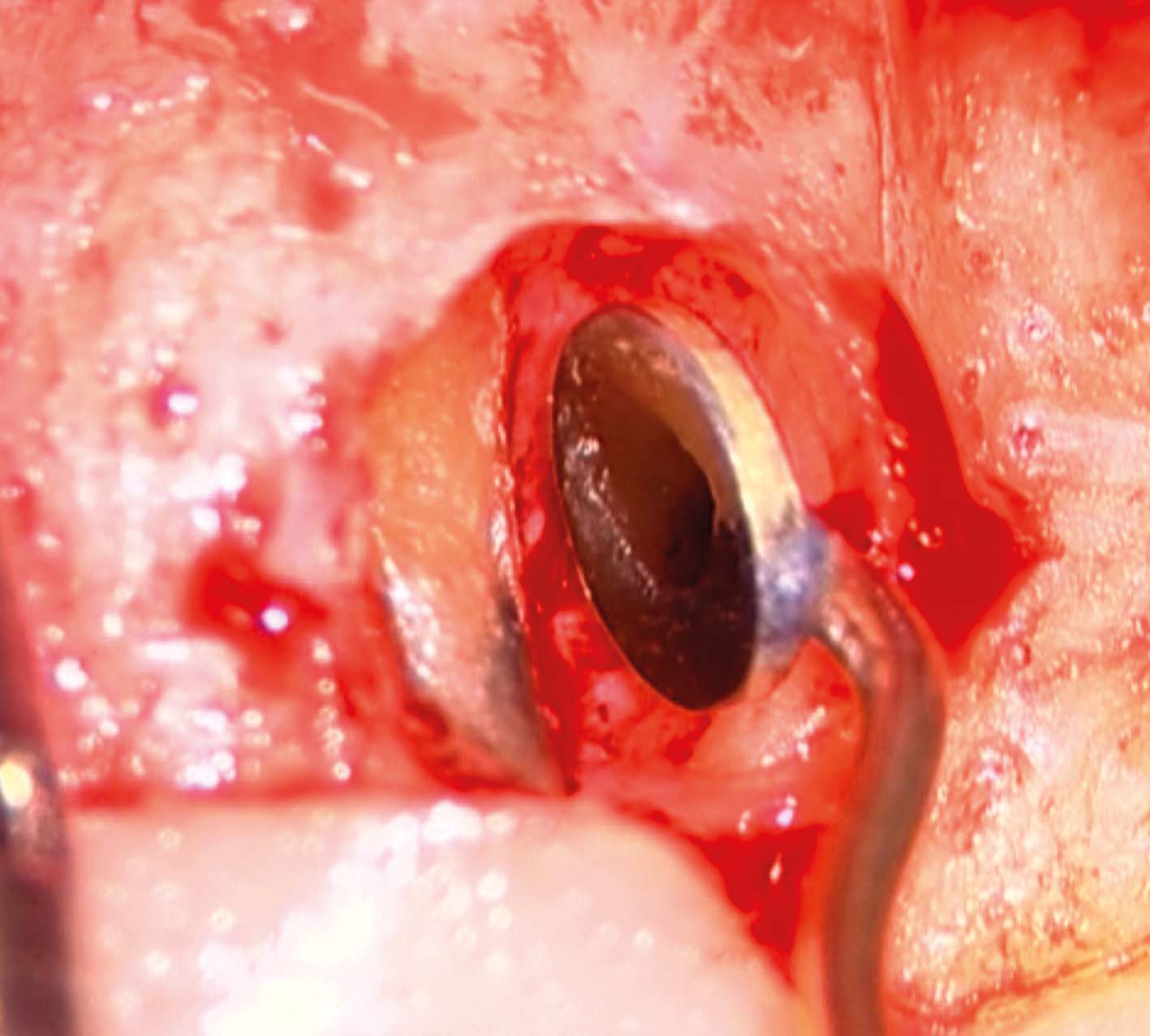
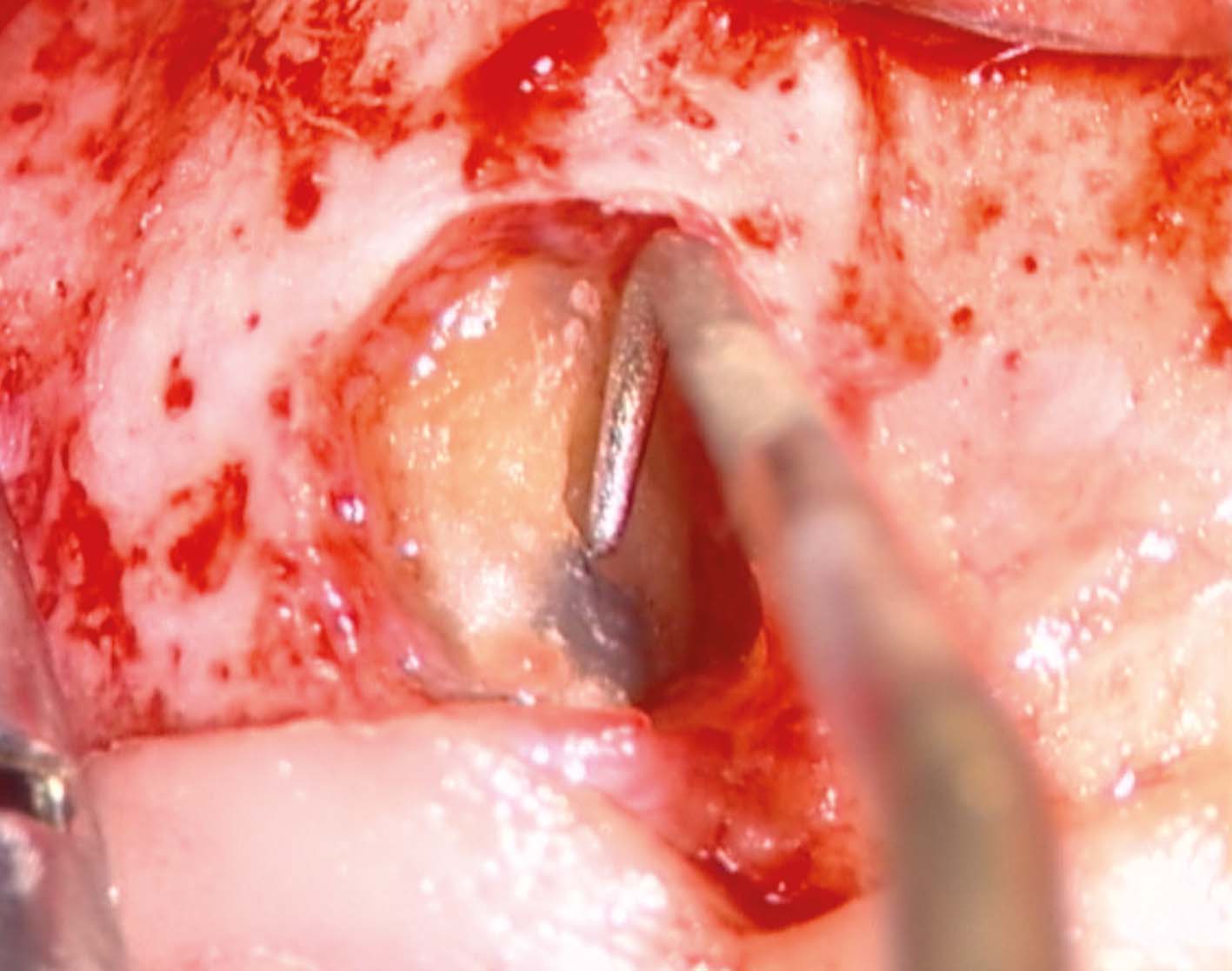
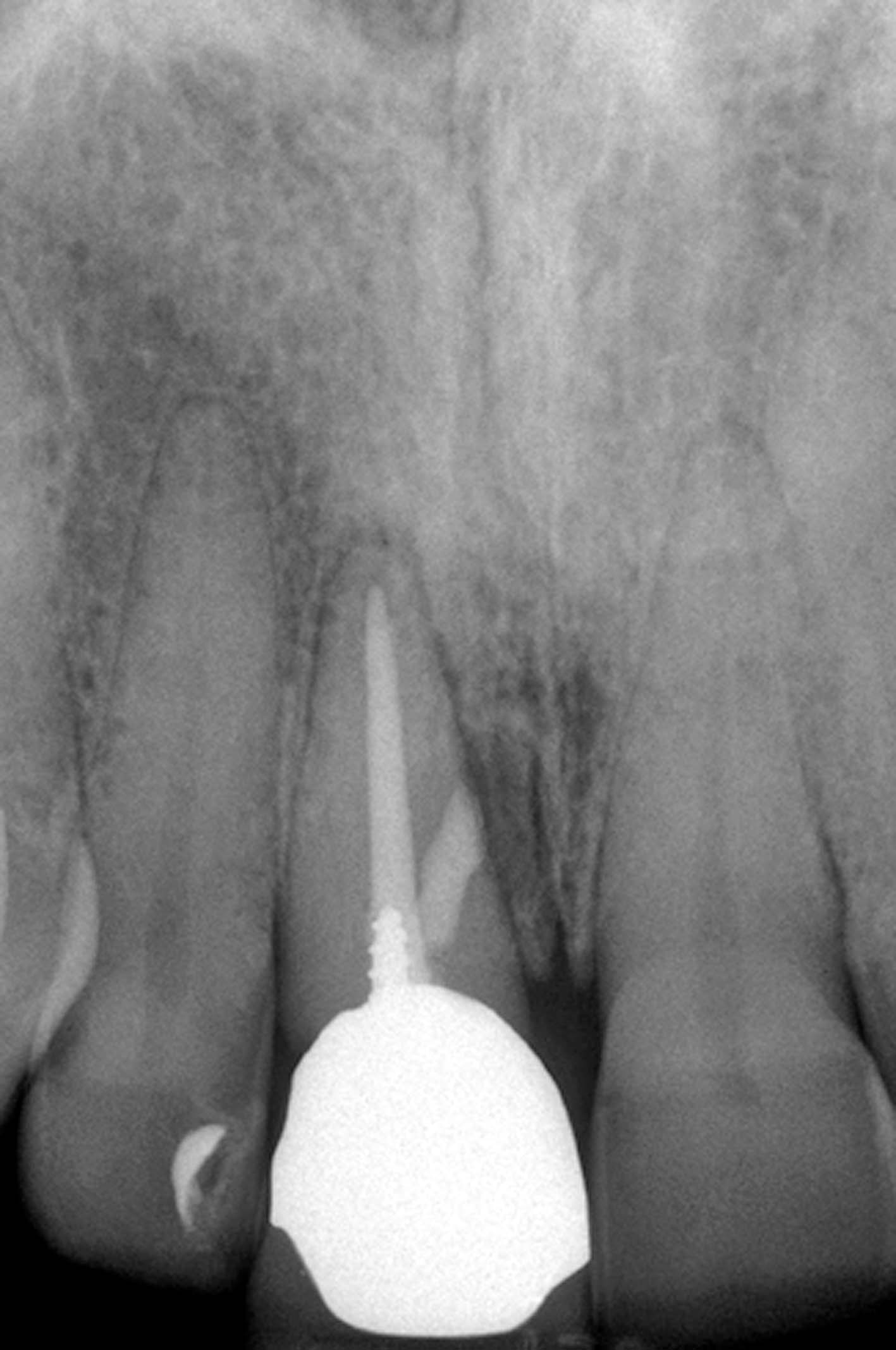
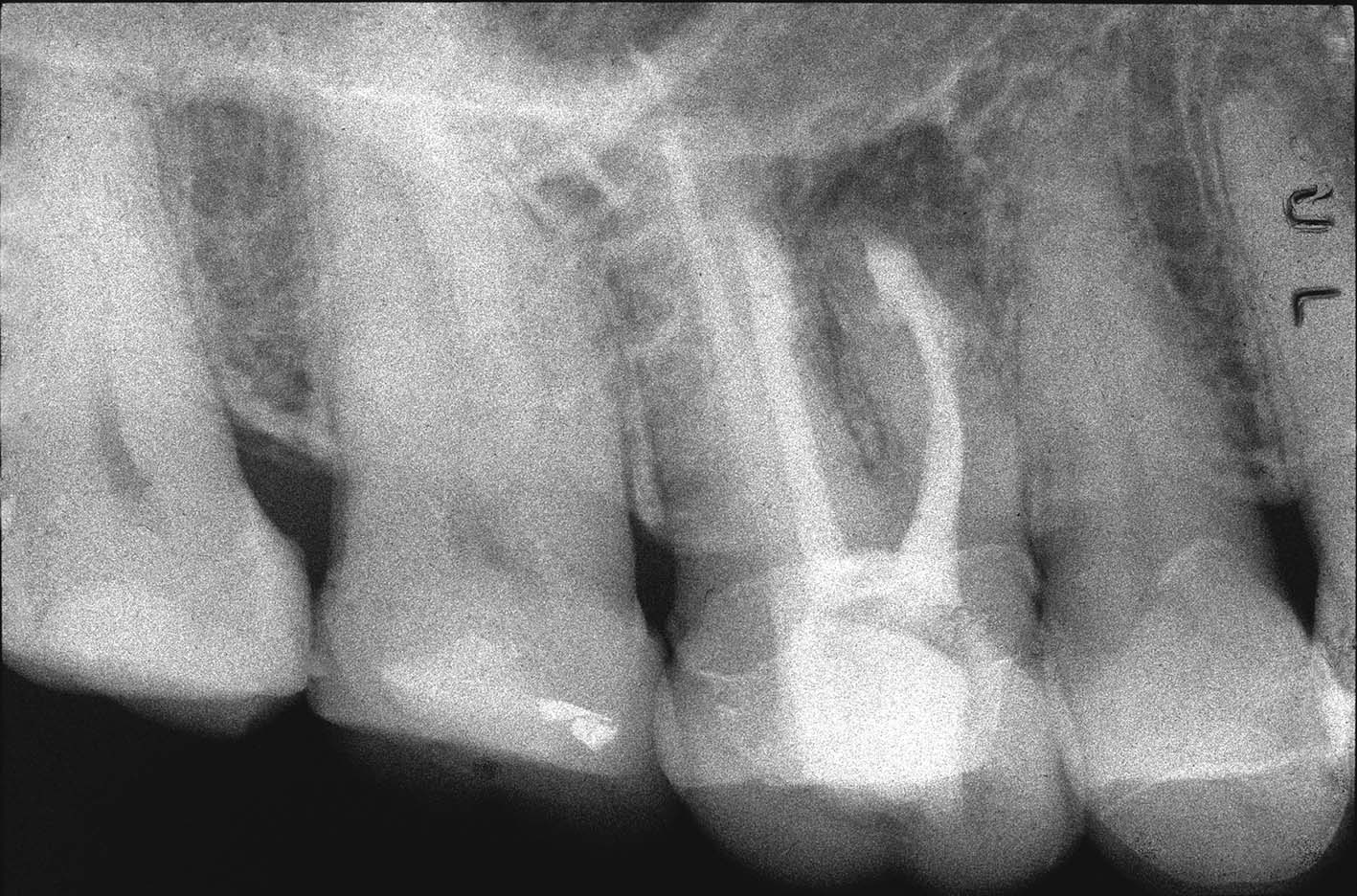
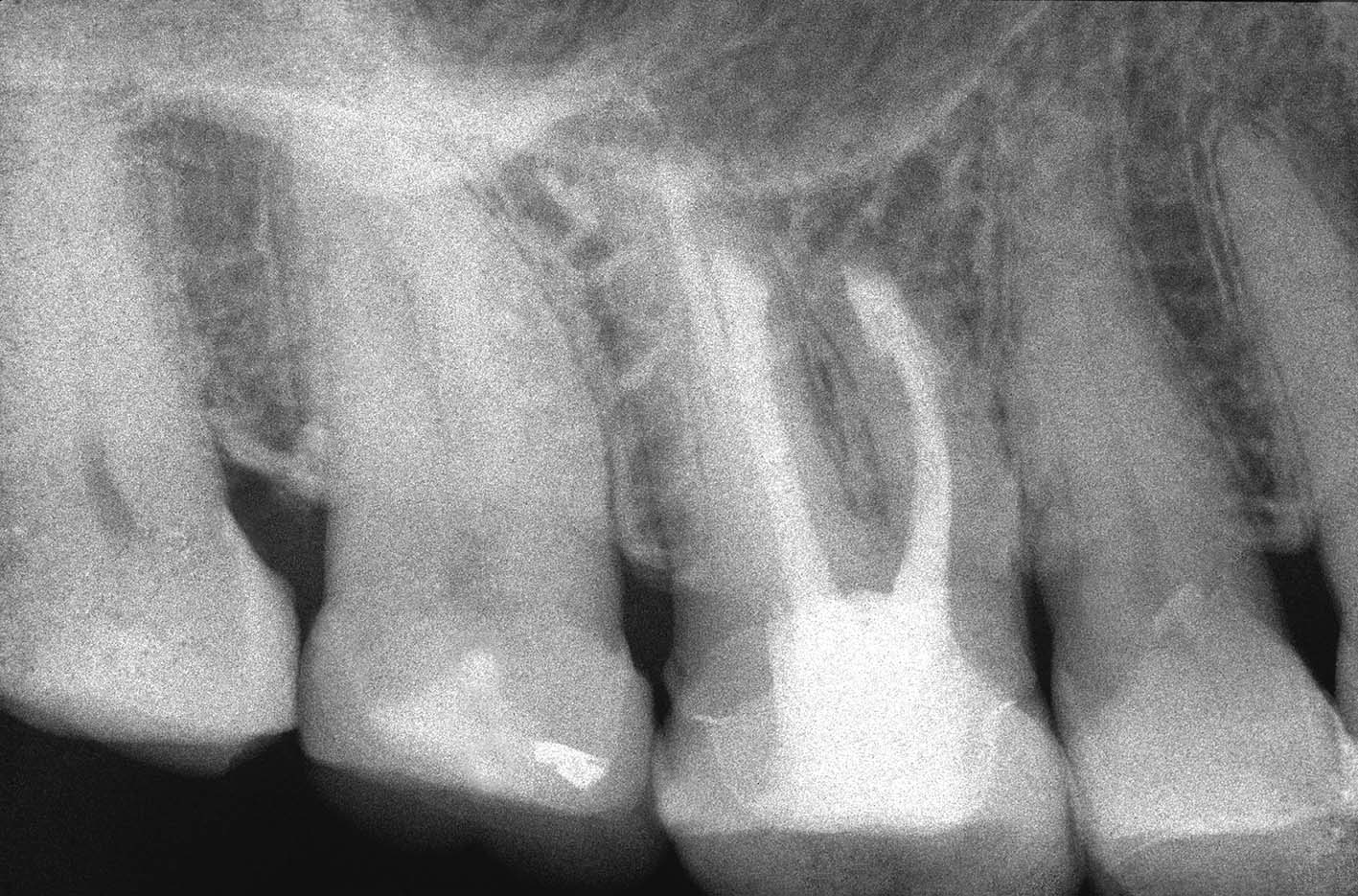
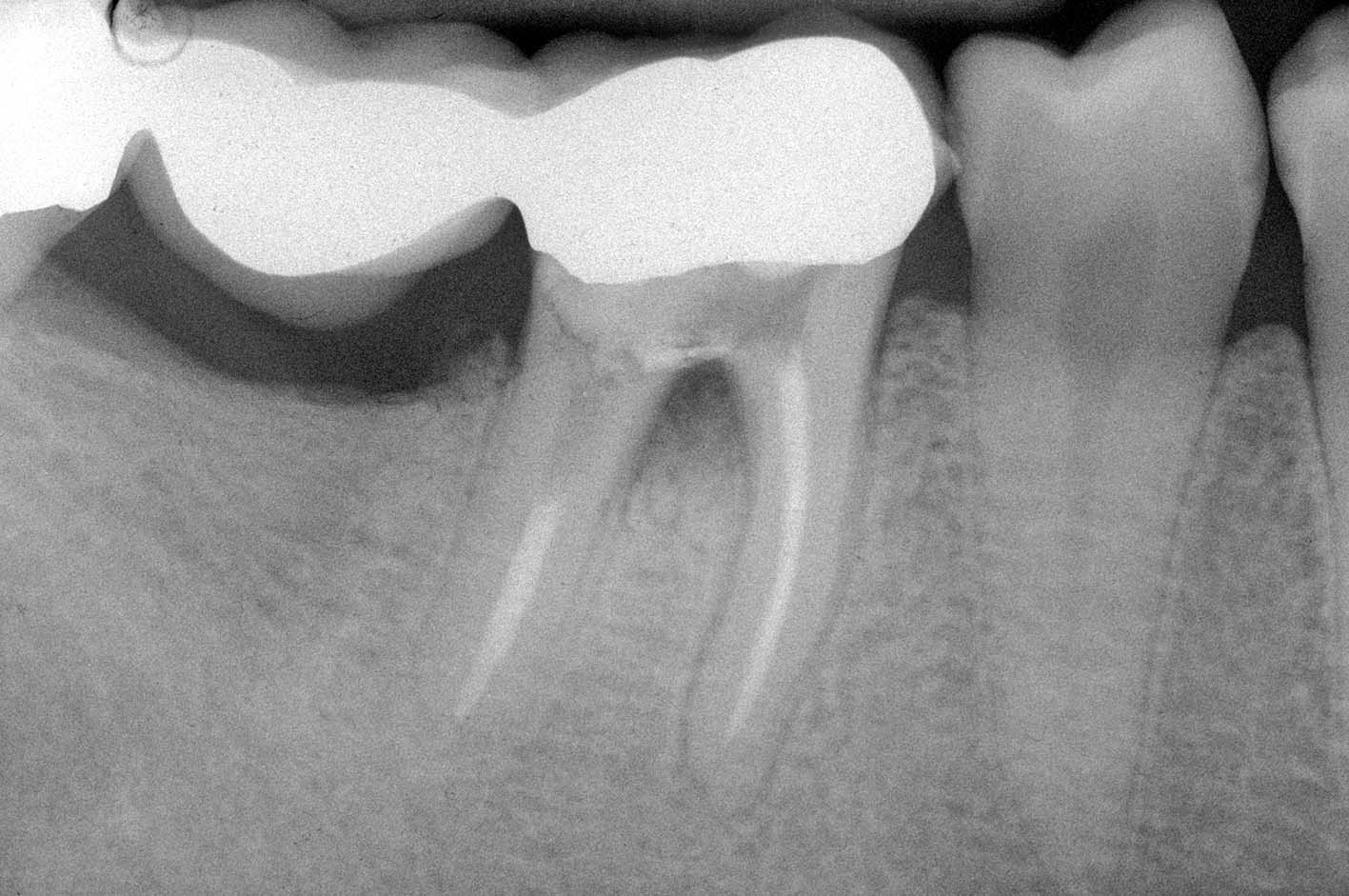
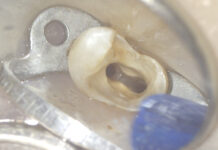
La radiografia pre-operatoria (Figura 1) mostra la presenza di uno strumento rotto nel canale della radice distale e la perforazione del pavimento camerale, con fuoriuscita di un cono di guttaperca. Dopo aver rimosso il cono di guttaperca (Figura 2) si è
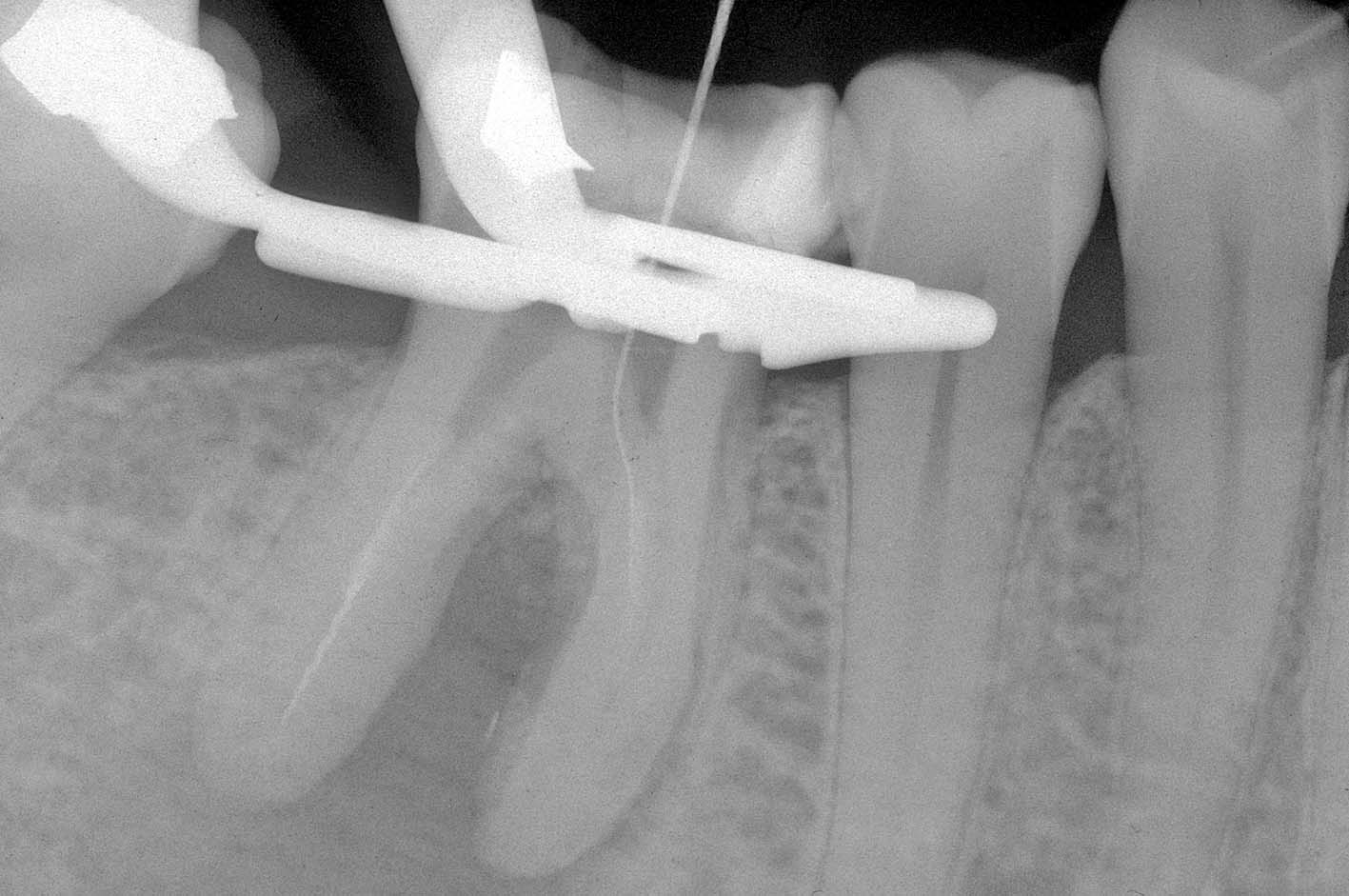
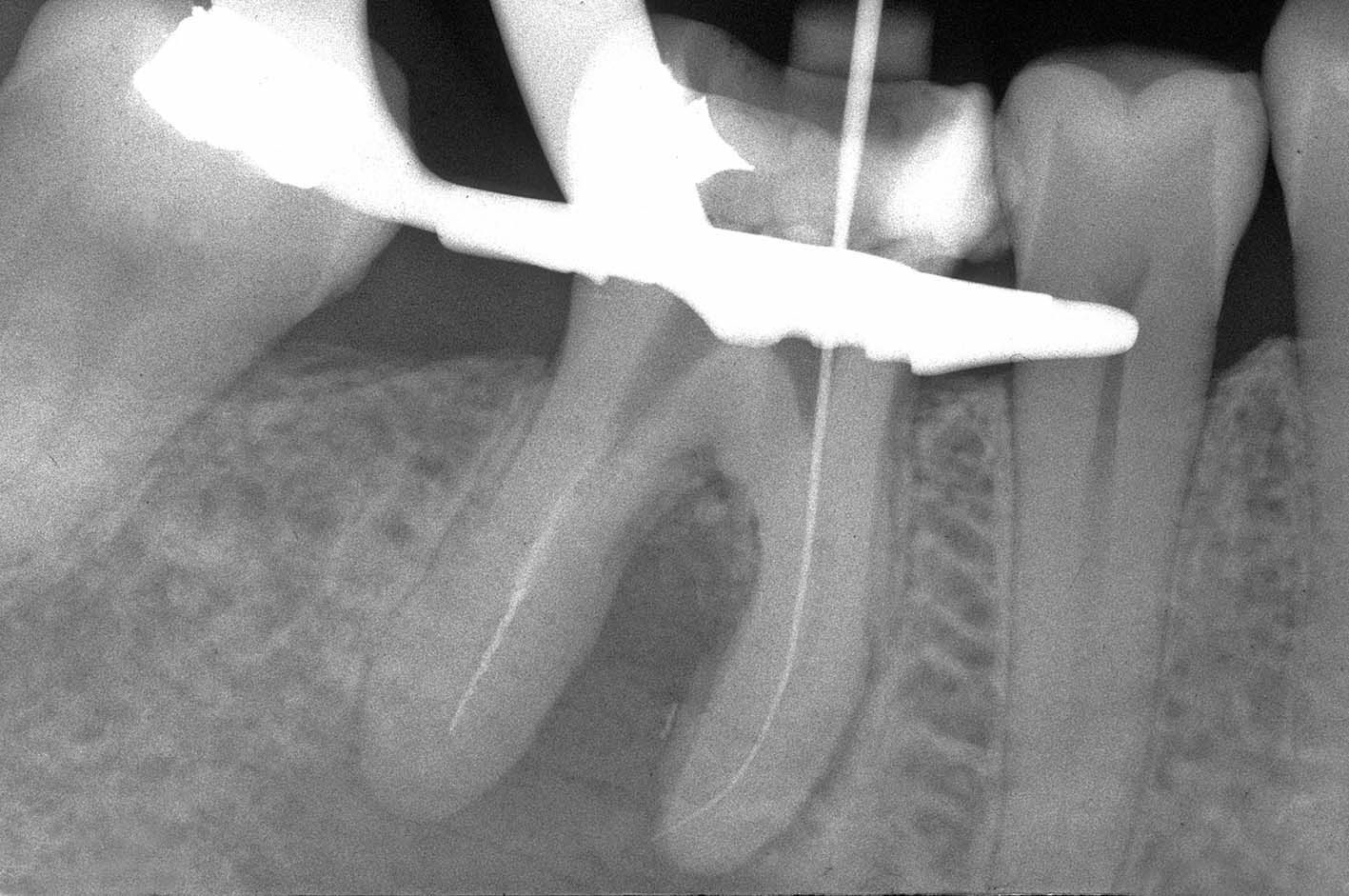
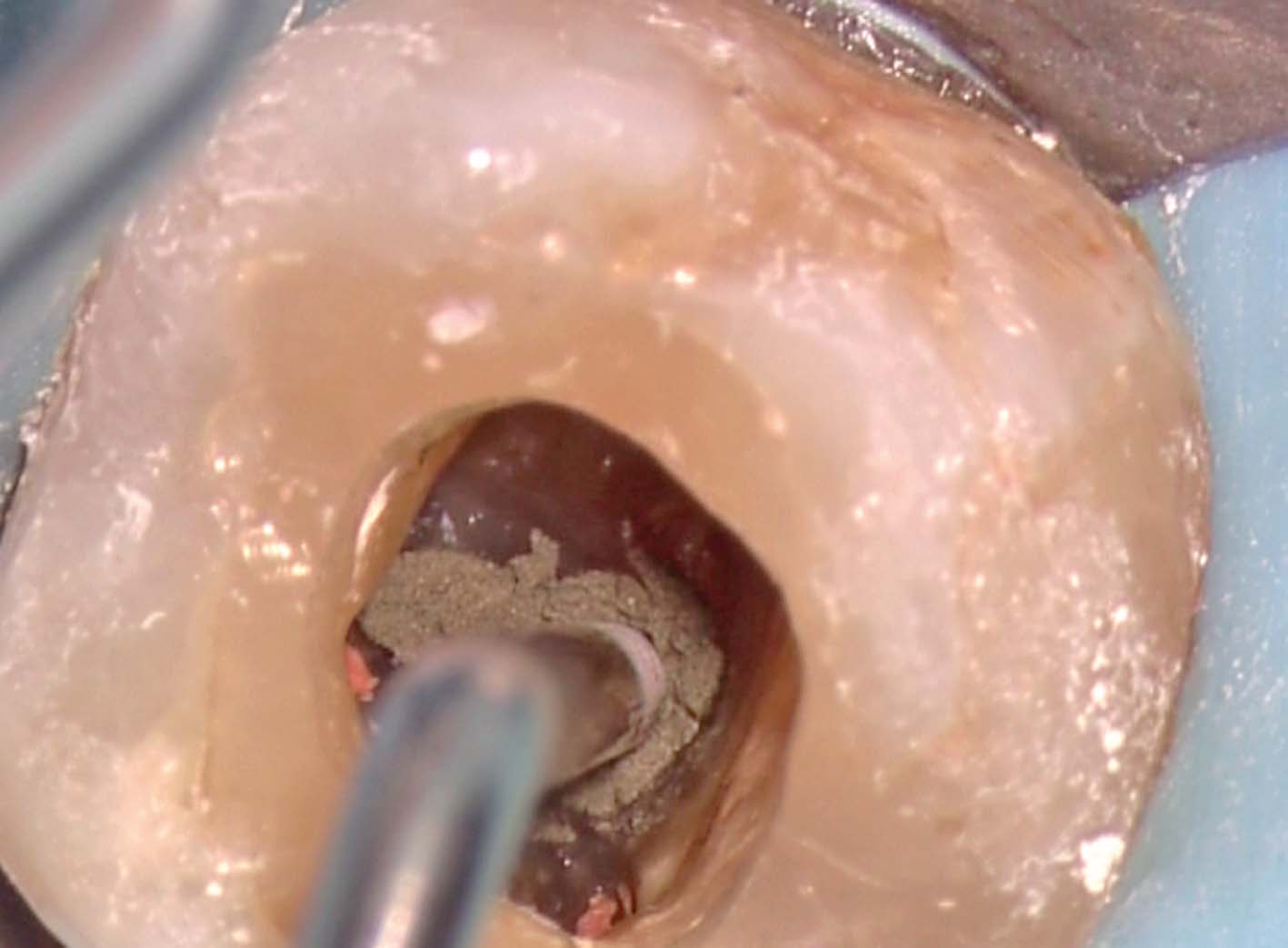
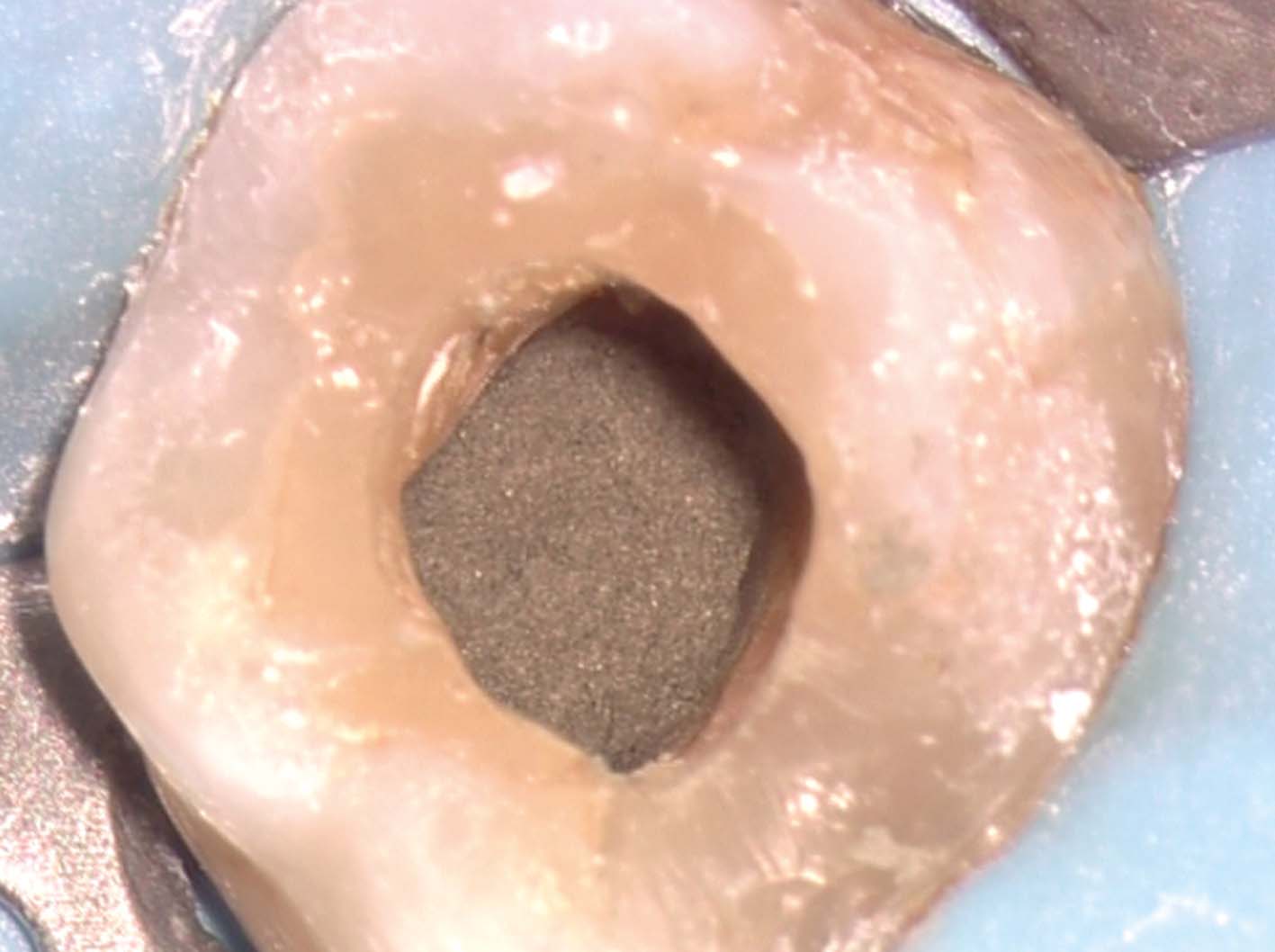
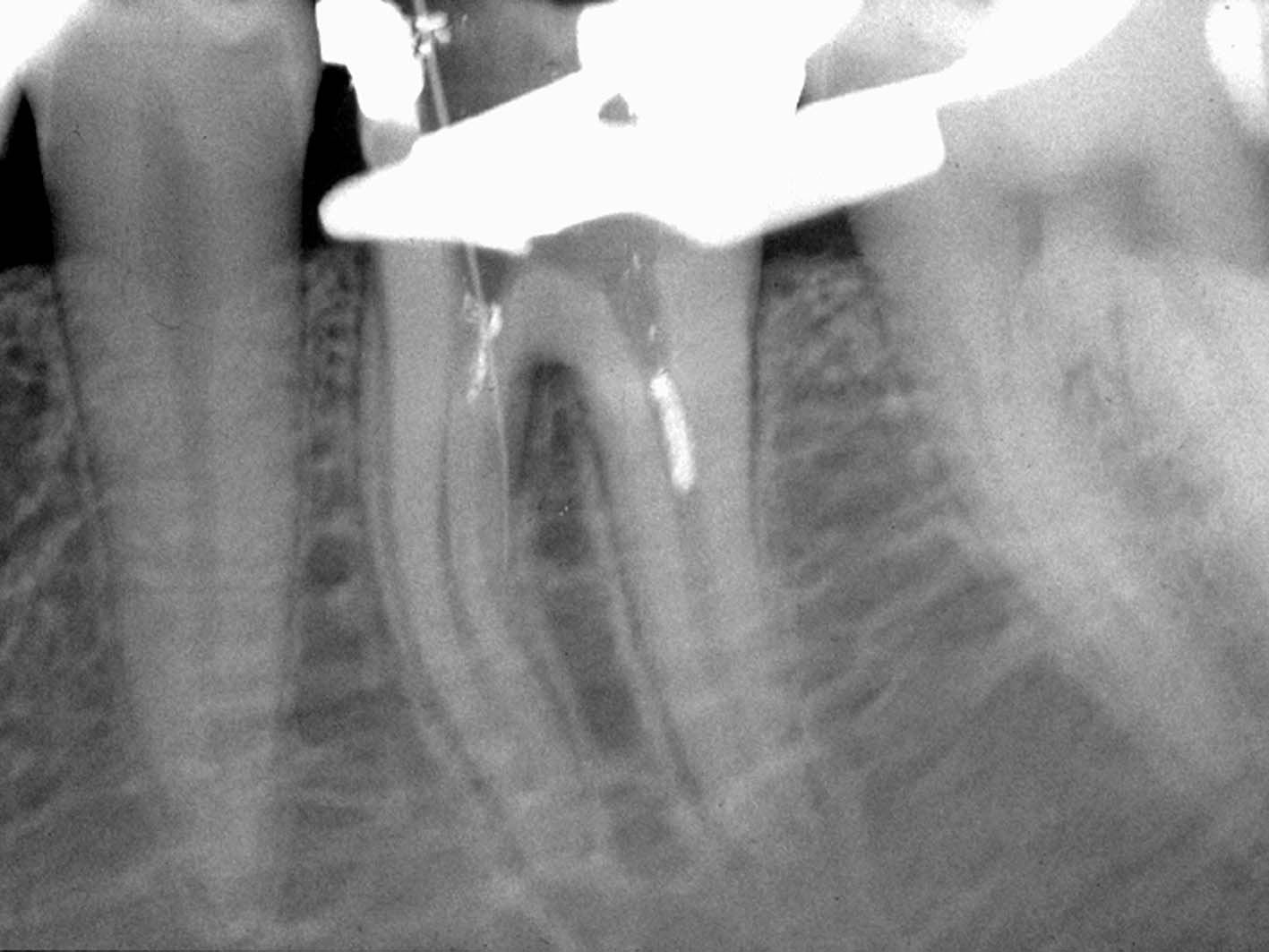
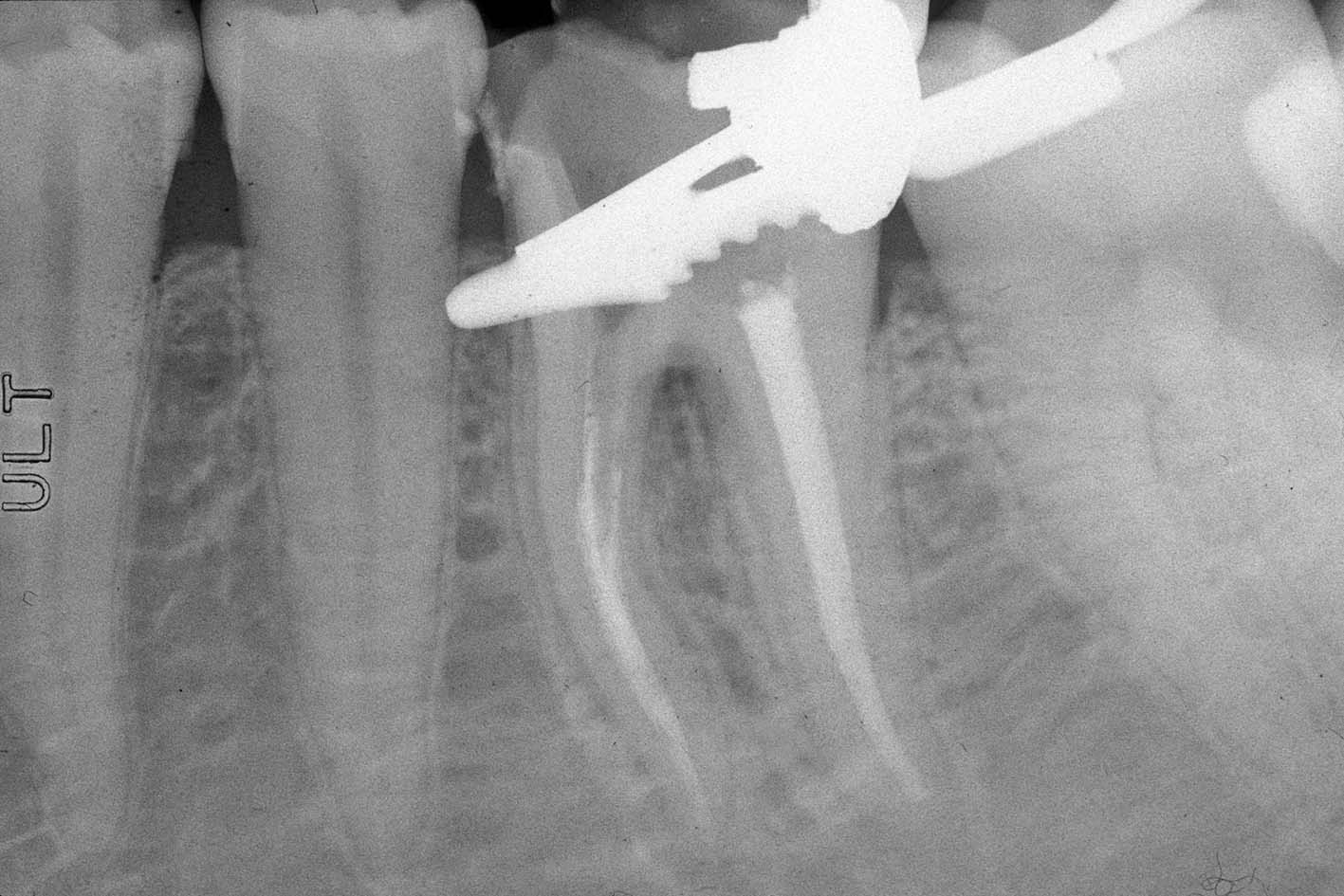
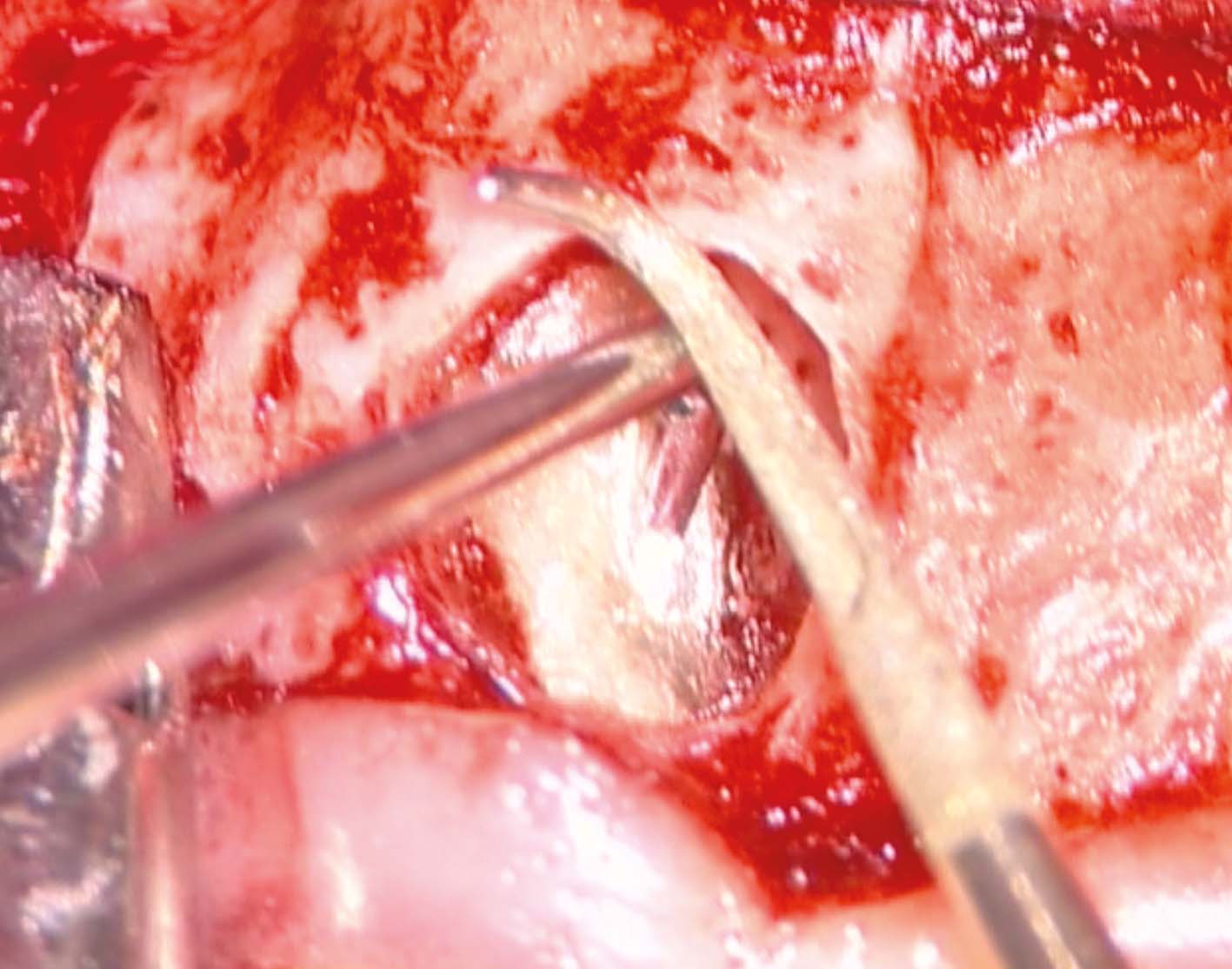
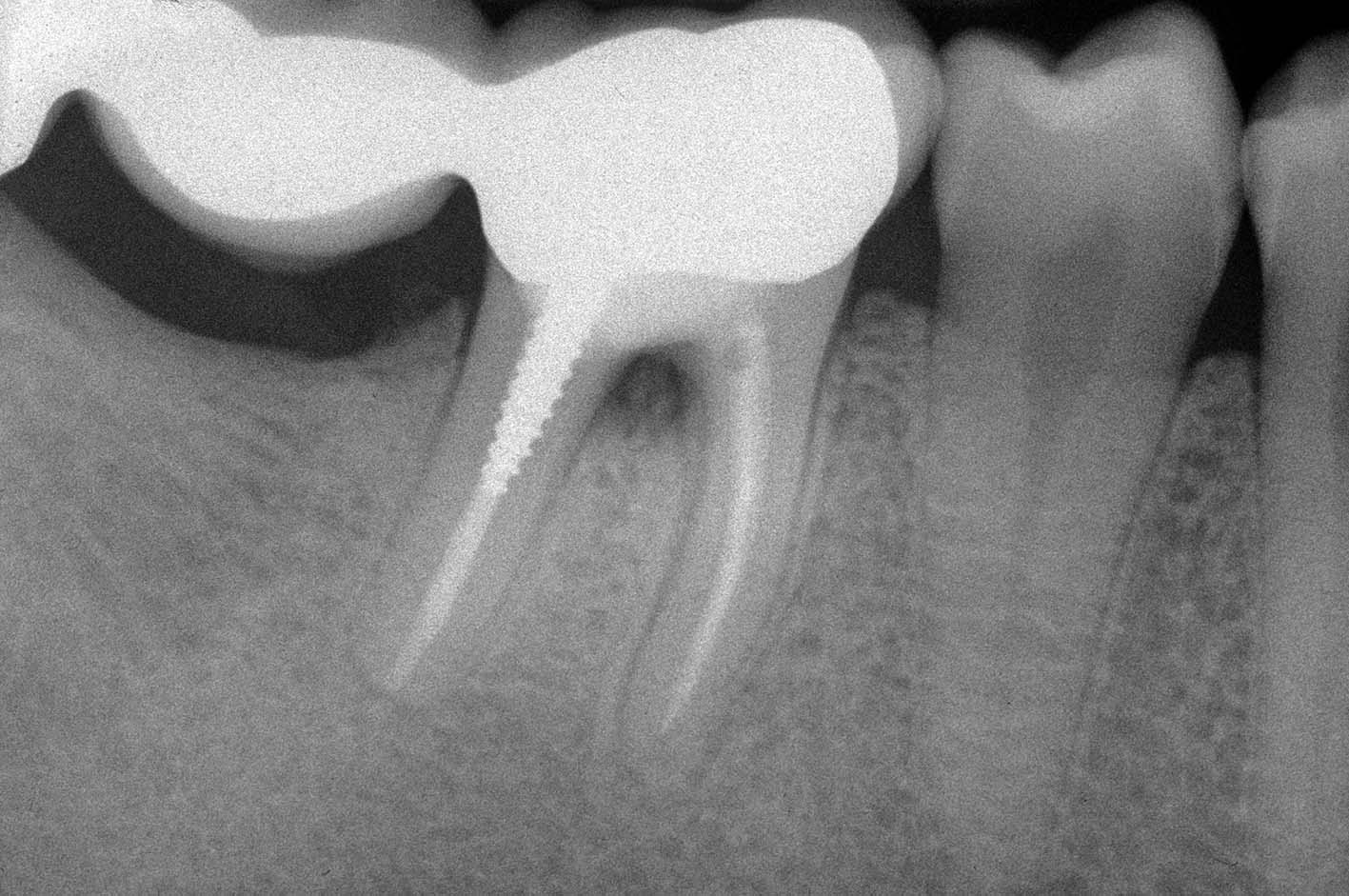
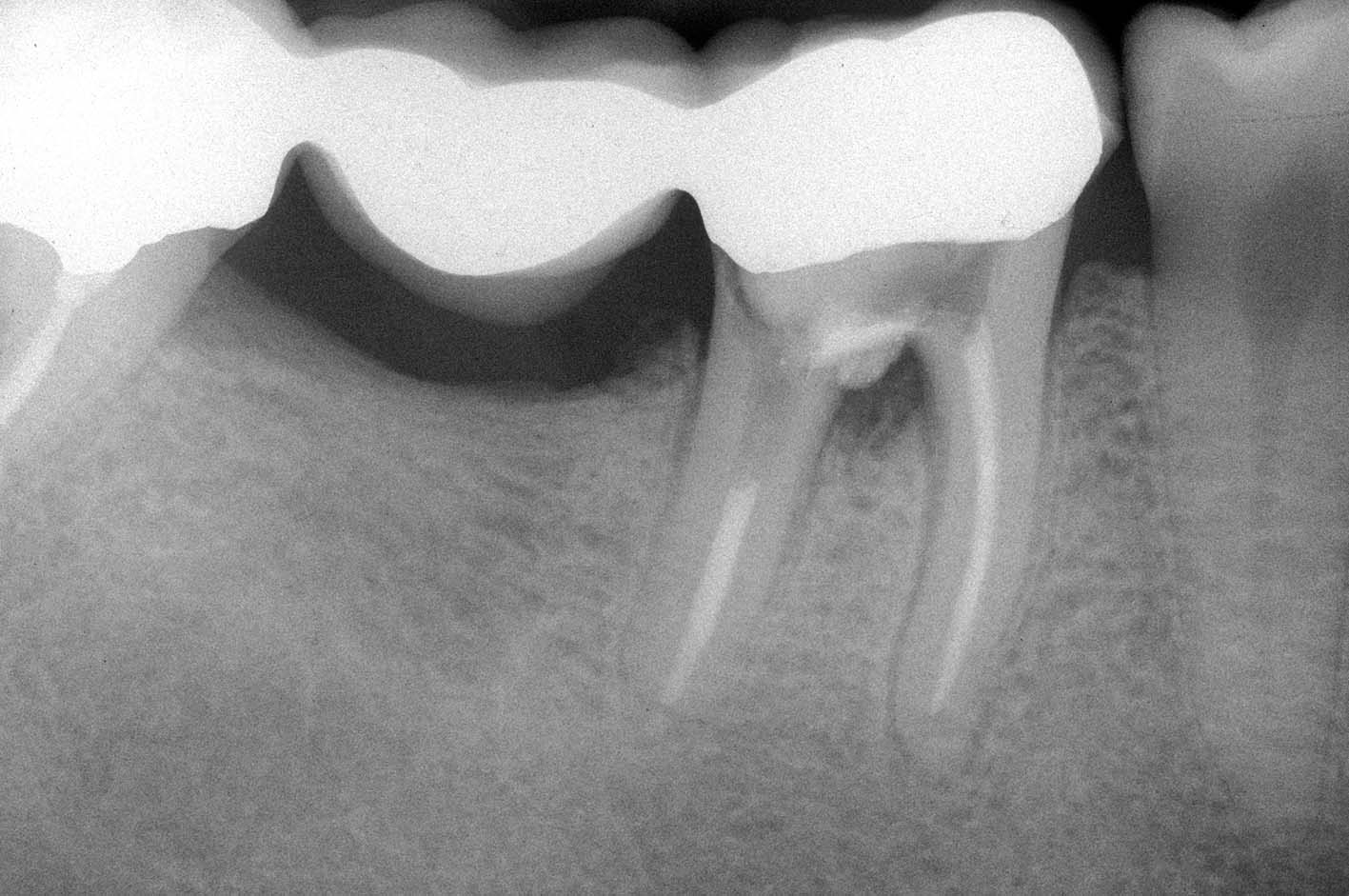
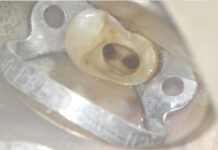
reperito il canale e iniziato il suo sondaggio (Figura 3), misurata la lunghezza di lavoro (Figura 4) ed eseguita la sua sagomatura. In preparazione dell’otturazione della perforazione con MTA, per evitare che frammenti di tale cemento cadessero nel canale preparato rischiando di ostruirlo, è stata posizionata al suo interno in maniera provvisoria della guttaperca termoplastica.
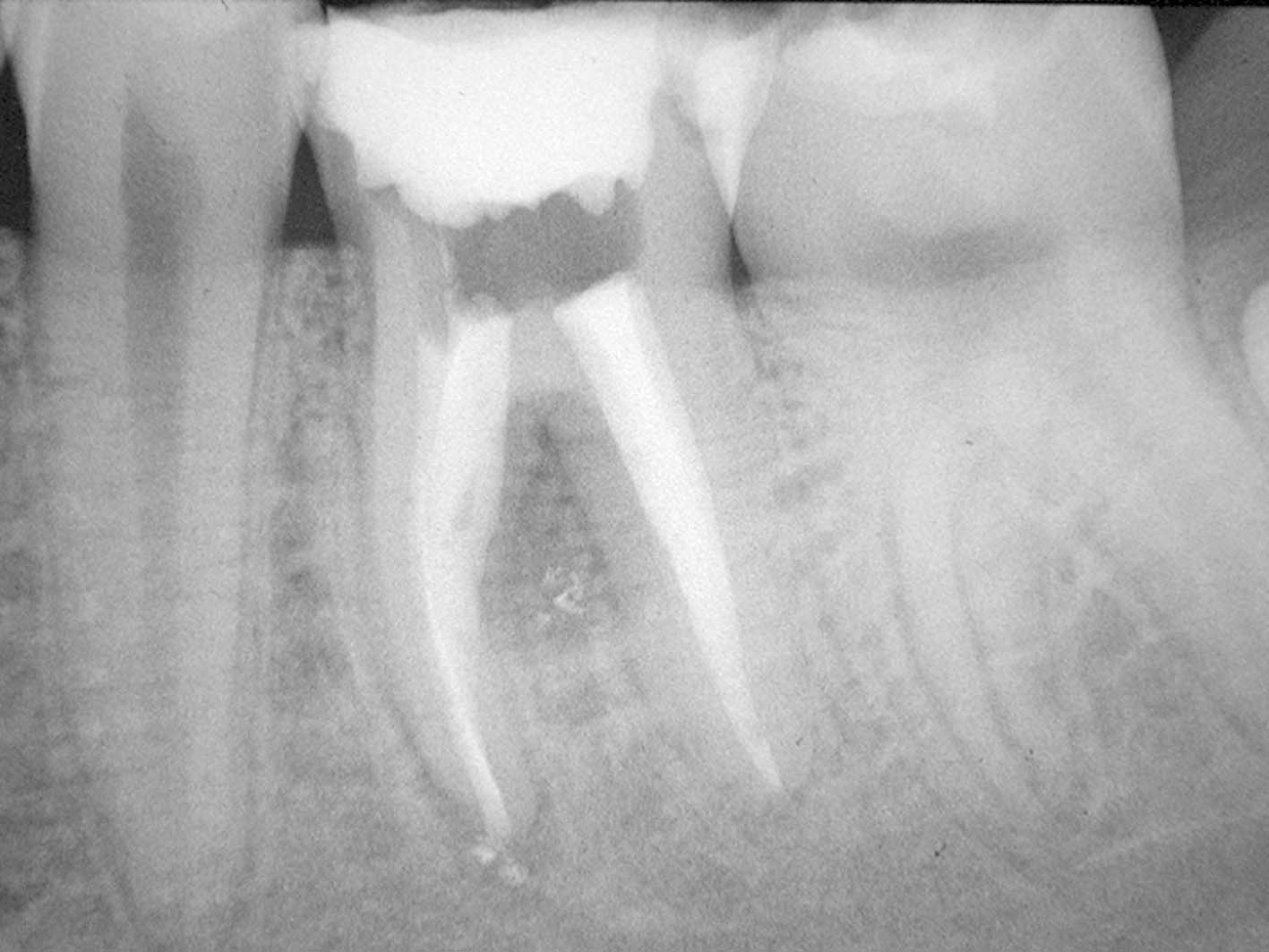
Con l’apposito carrier viene quindi posizionato l’MTA nel tragitto della perforazione, usando il tessuto di granulazione stesso come matrice per evitare sovrariempimenti (Figura 5). È stata quindi eseguita l’otturazione dei canali mesiali (Figura 6) e la rimozione dello strumento fratturato (Figura 7).
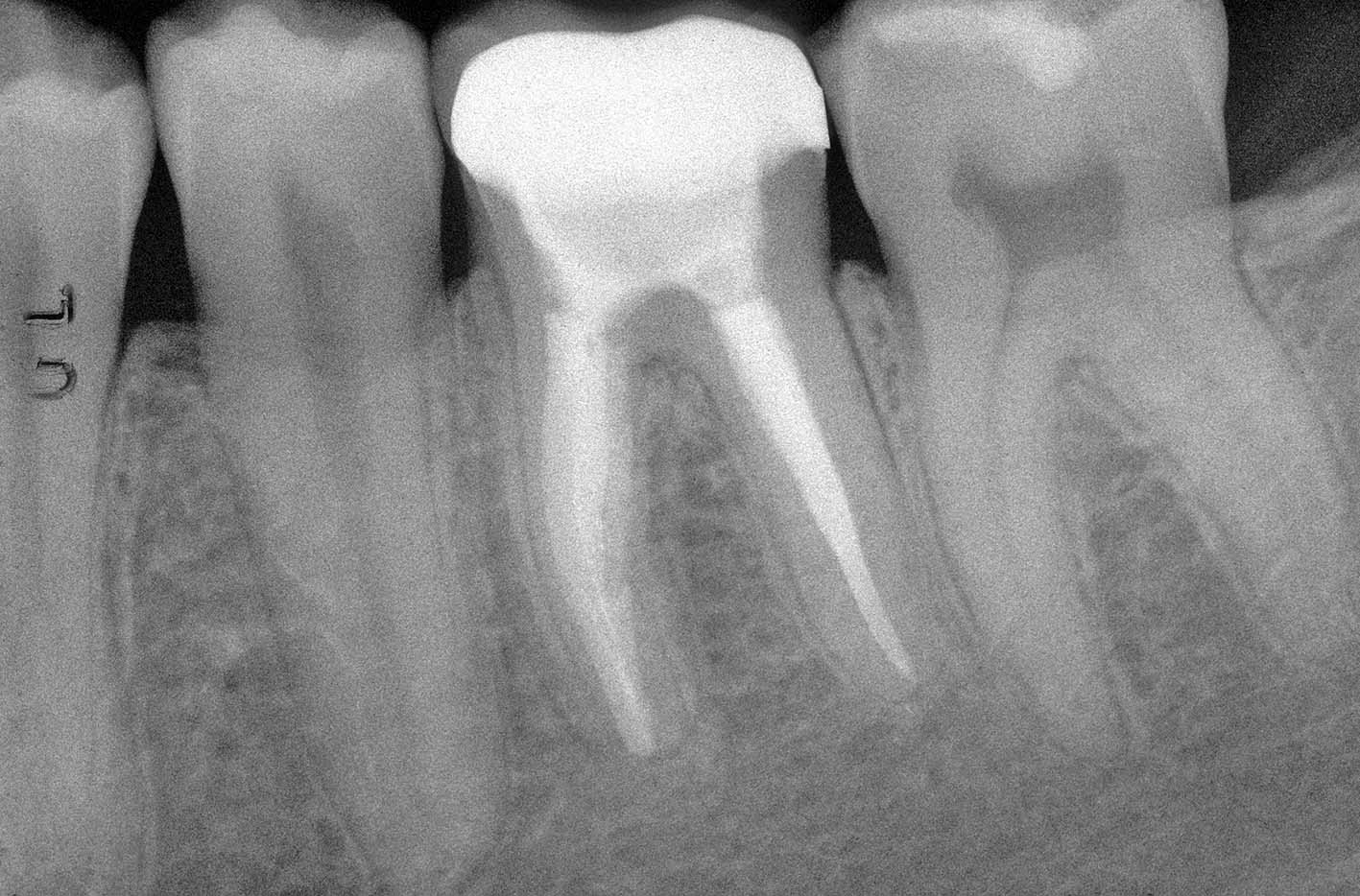
Dopo aver controllato l’indurimento del materiale MTA nella visita successiva, è stata completata l’otturazione del sistema dei canali radicolari (Figura 8). Il controllo a distanza di 7 anni conferma la perfetta guarigione (Figura 9).
Perforazioni del terzo apicale
Queste perforazioni possono avvenire nel corso della strumentazione di canali curvi, per l’esecuzione del cosiddetto “trasporto esterno” del forame apicale. Una volta eseguita la perforazione, se l’operatore riesce a ritrovare e preparare il canale originale (con l’utilizzo di strumenti sottili e precurvati, molta irrigazione e soprattutto molta pazienza), il danno provocato dalla perforazione sarà minimo in quanto, soprattutto se questa è piccola, si comporterà come un piccolo canale laterale che sarà facilmente otturato. Se invece il canale originale è rimasto intasato dai detriti di fango dentinale e gli strumenti ogni volta ripercorrono il cammino della perforazione, in tale caso il canale deve essere otturato con le metodiche tradizionali, e successivamente l’apice contenente la porzione non trattata del canale radicolare deve essere rimosso per via chirurgica, soprattutto se stiamo trattando un dente necrotico o se siamo di fronte a un ritrattamento.
D’altra parte, in accordo con quanto affermato da Nicholls,8 nel caso di un dente con polpa vitale il trattamento della perforazione dipende dall’estensione della porzione di canale situata apicalmente alla perforazione e dal momento in cui tale perforazione è stata eseguita, cioè se all’inizio o al termine della detersione e sagomatura. Se la distanza tra la perforazione e il forame apicale è maggiore di 2 mm, o se la perforazione è avvenuta dopo un discreto allargamento della porzione più apicale del canale (senza peraltro più riuscire a sondare il canale originale), è indicata l’otturazione del canale seguita dall’apicectomia con otturazione retrograda coronalmente al difetto. Se invece la perforazione avviene entro 2 mm e all’inizio della preparazione canalare, la mancata otturazione della porzione più apicale del canale avrà una prognosi non peggiore di quei casi privi di perforazione ma con un’otturazione leggermente corta rispetto al vero termine del canale radicolare.
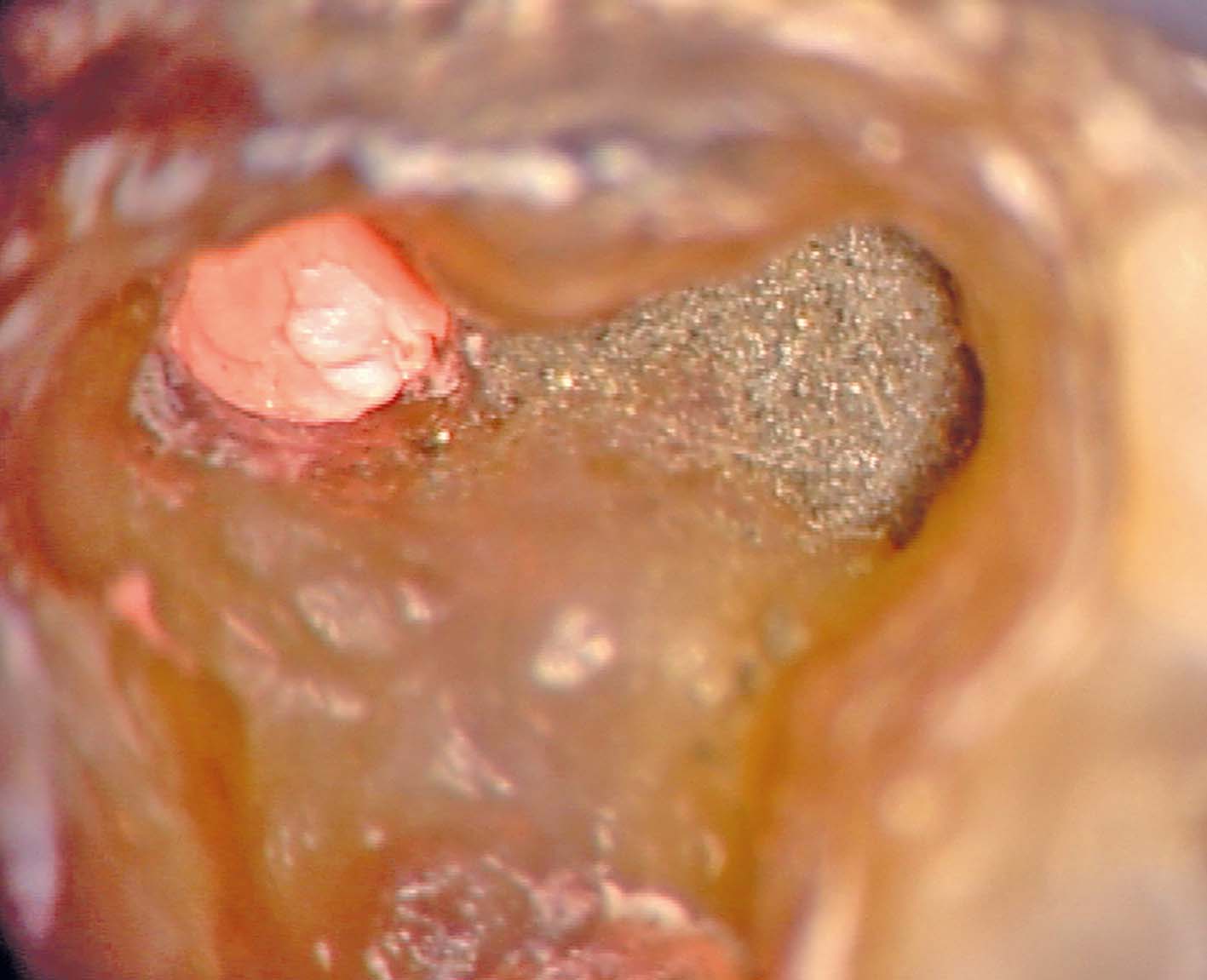
La radiografia pre-operatoria del primo molare superiore di destra (Figura 10) mostra la presenza di materiale radiopaco dalla forma irregolare, che il dentista precedente aveva interpretato come otturazione di un riassorbimento interno del canale palatino. La presenza di una fistola vestibolare (Figura 11) e di una costante dolenzia hanno spinto la paziente a sentire un diverso parere e la radiografia endorale presa con angolazione disto-mesiale mostrava la presenza del medesimo materiale nella zona della triforcazione, immerso in una zona di radiotrasparenza, rappresentata da tessuto di granulazione (Figura 12). All’apertura della cavità d’accesso appariva evidente una cospicua perforazione (Figura 13), attraverso la quale era stata introdotta della guttaperca termoplastica, avendo scambiato quell’orifizio per un imbocco canalare. Con l’aiuto del microscopio operatorio e utilizzando un “micro-debrider” (Dentsply, Maillefer) (Figura 14), sono stati rimossi i vari frammenti di guttaperca e la totale rimozione è stata controllata da un nuovo esame radiografico endorale (Figura 15).
È stato quindi introdotto nel sottostante tessuto di granulazione del collagene equino liofilizzato e riassorbibile (Figura 16), allo scopo di costruire una matrice sulla la quale poter posizionare il materiale riparativo della perforazione senza avere dei grossolani sovrariempimenti. Con l’apposito carrier, sempre sotto la guida del microscopio operatorio, è stato posizionato l’MTA (Figura 17) fino ad ottenere il completo sigillo della perforazione del pavimento camerale (Figura 18).
La radiografia postoperatoria mostra l’otturazione con MTA senza alcun sovrariempimento (Figura 19). Il controllo a distanza di circa un mese mostrava la guarigione della fistola e l’assenza di sondabilità della zona della biforcazione vestibolare (Figura 20). La radiografia di controllo eseguita dopo sei mesi mostra l’assenza di radiotrasparenza nella triforcazione a conferma della guarigione della lesione precedentemente sviluppatasi (Figura 21).
Perforazioni del terzo medio
Le perforazioni del terzo medio avvengono nella maggior parte dei casi durante la preparazione della cavità d’accesso o, più spesso, durante le fasi di detersione e sagomatura o, infine, durante la preparazione dello spazio per un perno con l’utilizzo di frese tipo Largo, Peeso, Gates Glidden o simili.
Nel secondo caso le perforazioni sono più frequenti nelle radici mesiali dei molari inferiori e nelle mesio-vestibolari dei molari superiori. Questo è dovuto alla mancata applicazione del “metodo anti-curvatura” (descritto da Abou-Rass, Frank e Glick2) e, quindi, alla mancanza dell’accesso rettilineo al terzo apicale del canale. Queste perforazioni possono capitare ancora più frequentemente oggi, da quando vanno di moda le cavità di accesso “minimamente invasive” dette anche “ninja access cavity”, con le quali gli strumenti lavorano in maniera eccessiva a contatto con la parete distale del canale rivolta verso la biforcazione, con conseguente stripping.
Le perforazioni in seguito alla preparazione dello spazio per un perno possono avvenire in qualsiasi dente. Tuttavia, ancora una volta, le radici più spesso colpite sono rappresentate dalle mesiali dei molari inferiori e dalle mesio-vestibolari dei molari superiori. Tali radici non devono mai essere allargate per poter ricevere un perno, in quanto il rischio di eseguire una perforazione è molto alto. Nei molari, le radici nelle quali con maggior sicurezza si può creare lo spazio per alloggiare un perno sono la distale degli inferiori e la palatina dei superiori. Tale spazio, tuttavia, deve sempre essere creato tenendo presente l’inclinazione del dente, la curvatura del canale, l’anatomia della radice, gli spessori della dentina oltre alle dimensioni della fresa9. La preparazione dello spazio per il perno deve consistere nella semplice rimozione del materiale dell’otturazione canalare. L’operatore deve evitare anche solo di toccare le pareti canalari e deve sfruttare lo spazio preparato dall’endodontista durante le manovre di sagomatura.
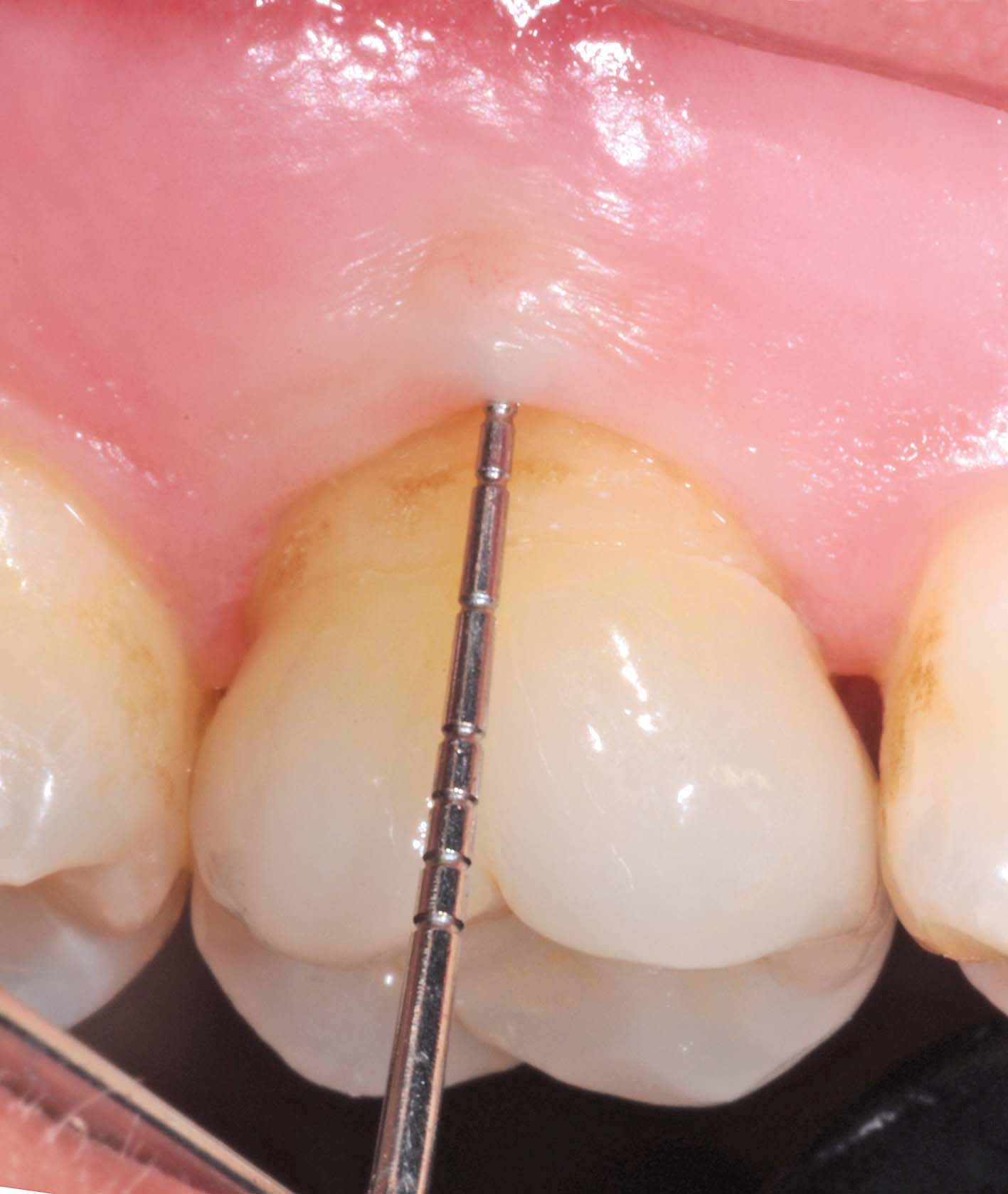
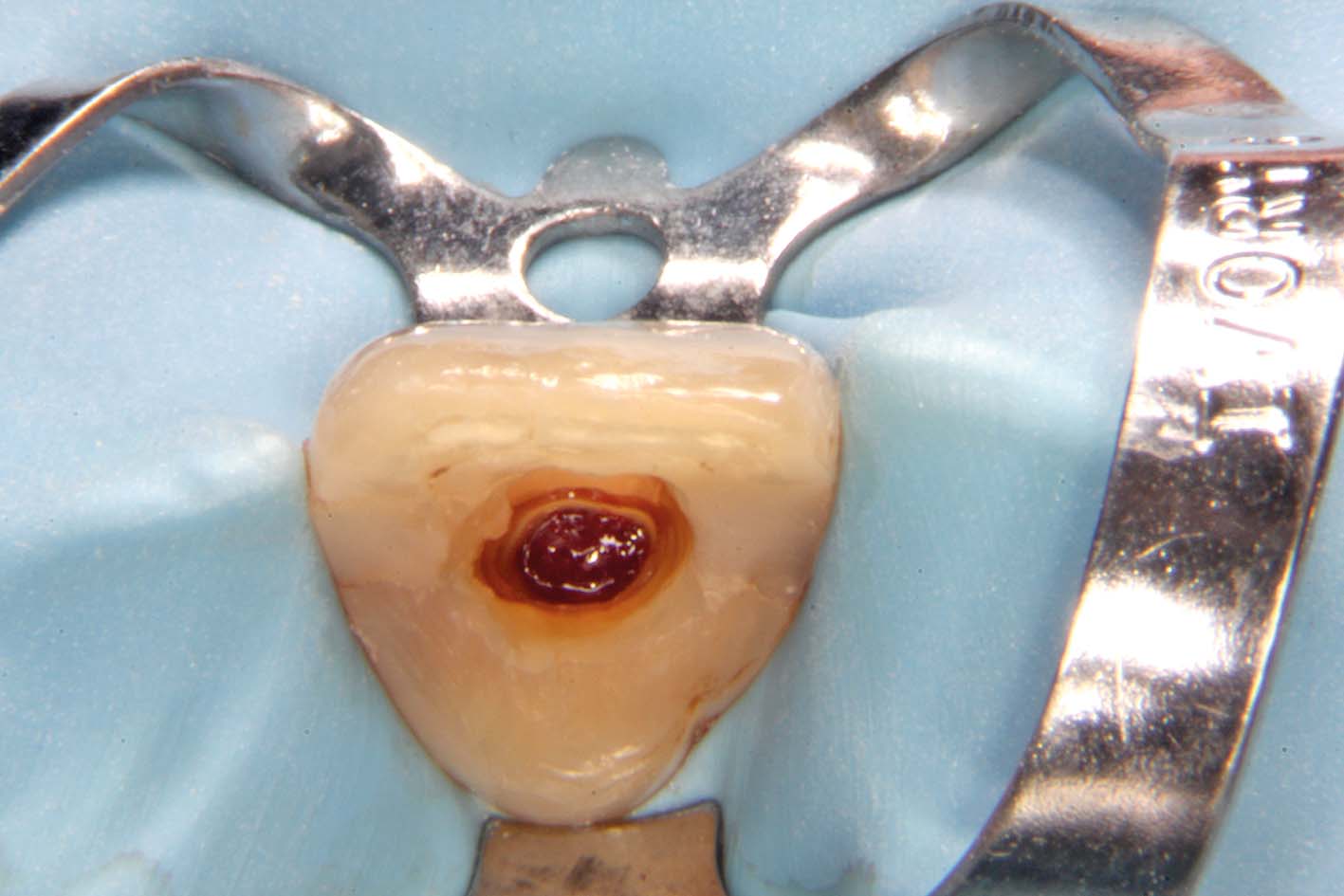
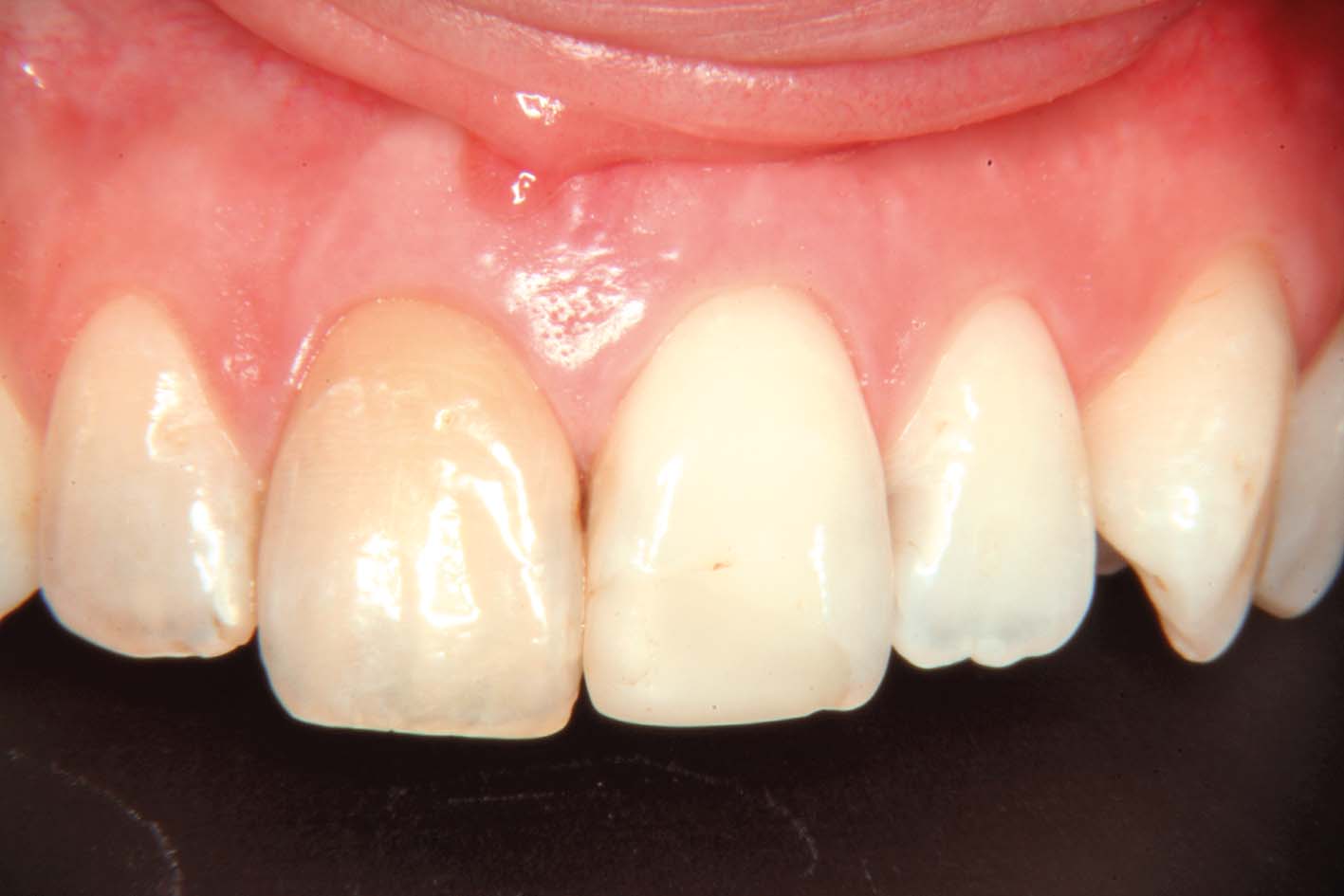
Nell’incisivo centrale superiore destro era stato introdotto
del materiale sbiancante prima ancora di eseguire l’otturazione del canale radicolare.
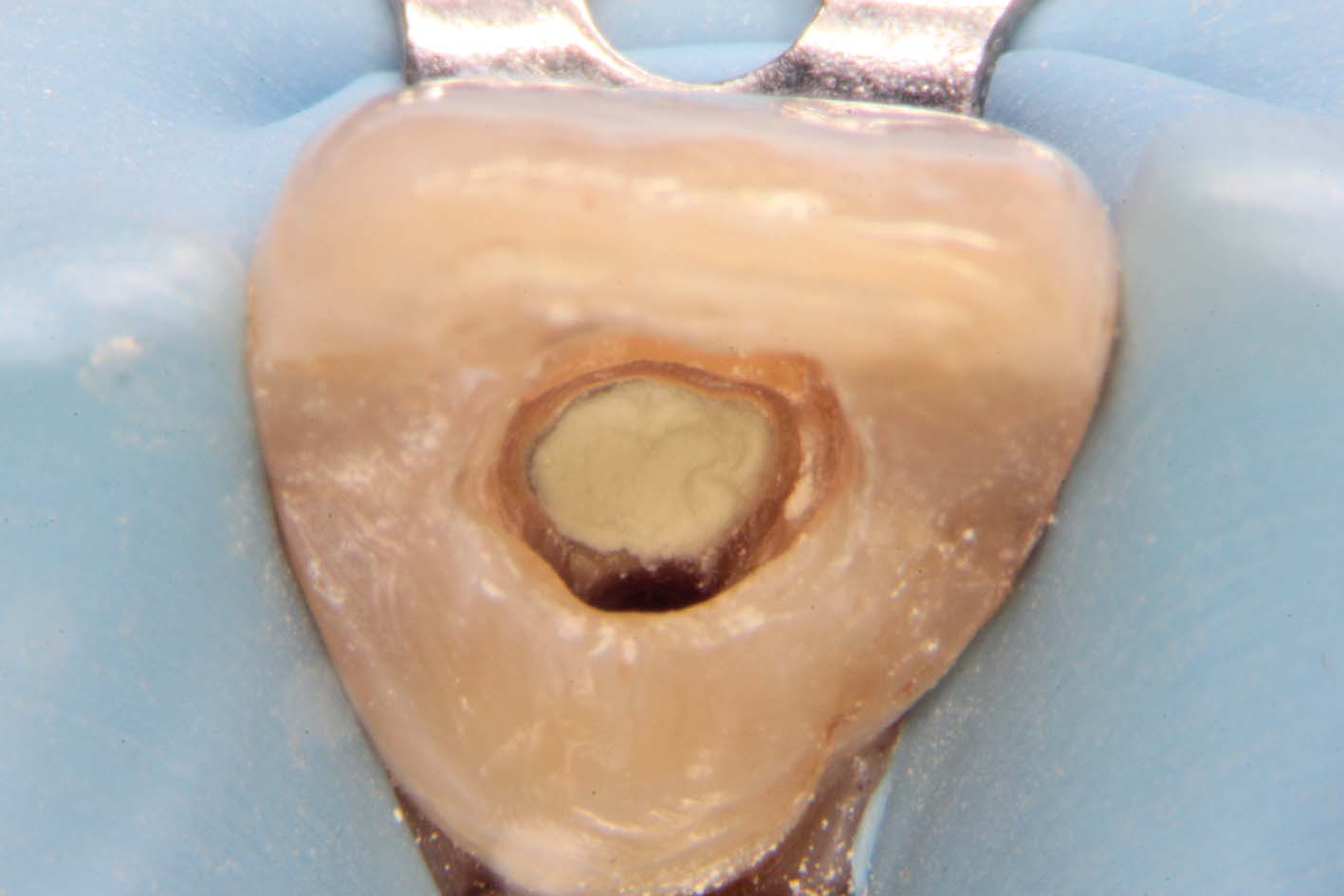
A protezione dei tessuti periapicali era stato messo del materiale composito all’imbocco del canale radicolare per evitare che i gas sviluppatisi dal materiale sbiancante potessero diffondersi in direzione apicale e creare danni ai tessuti circostanti (Figura 22).
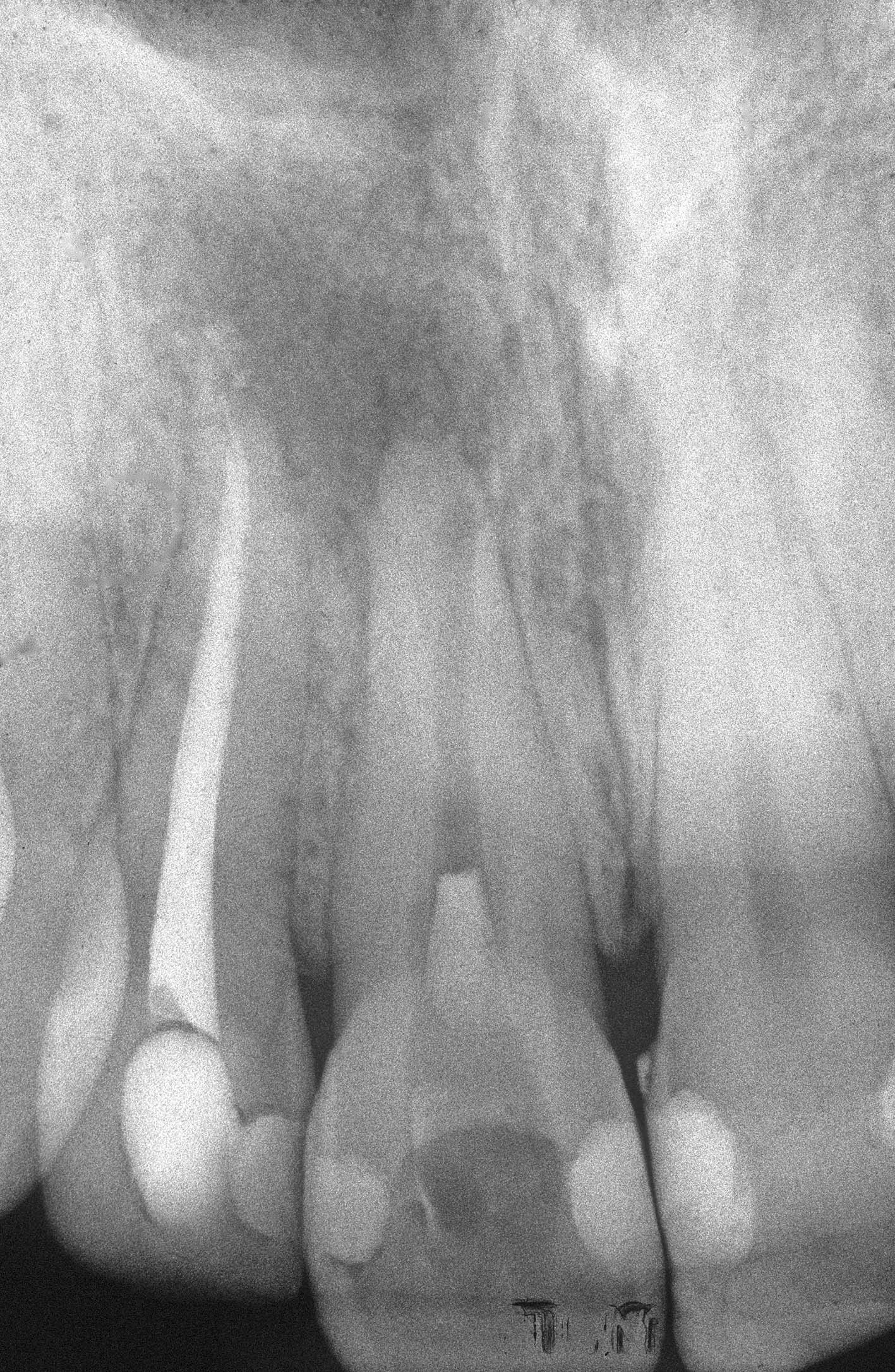
Al comparire di sintomi, nel tentativo di rimuovere il composito per avere accesso al canale, era stata eseguita una grande perforazione sull’aspetto vestibolare della radice, causata dall’erronea inclinazione della fresa usata troppo in direzione vestibolare (Figura 23).
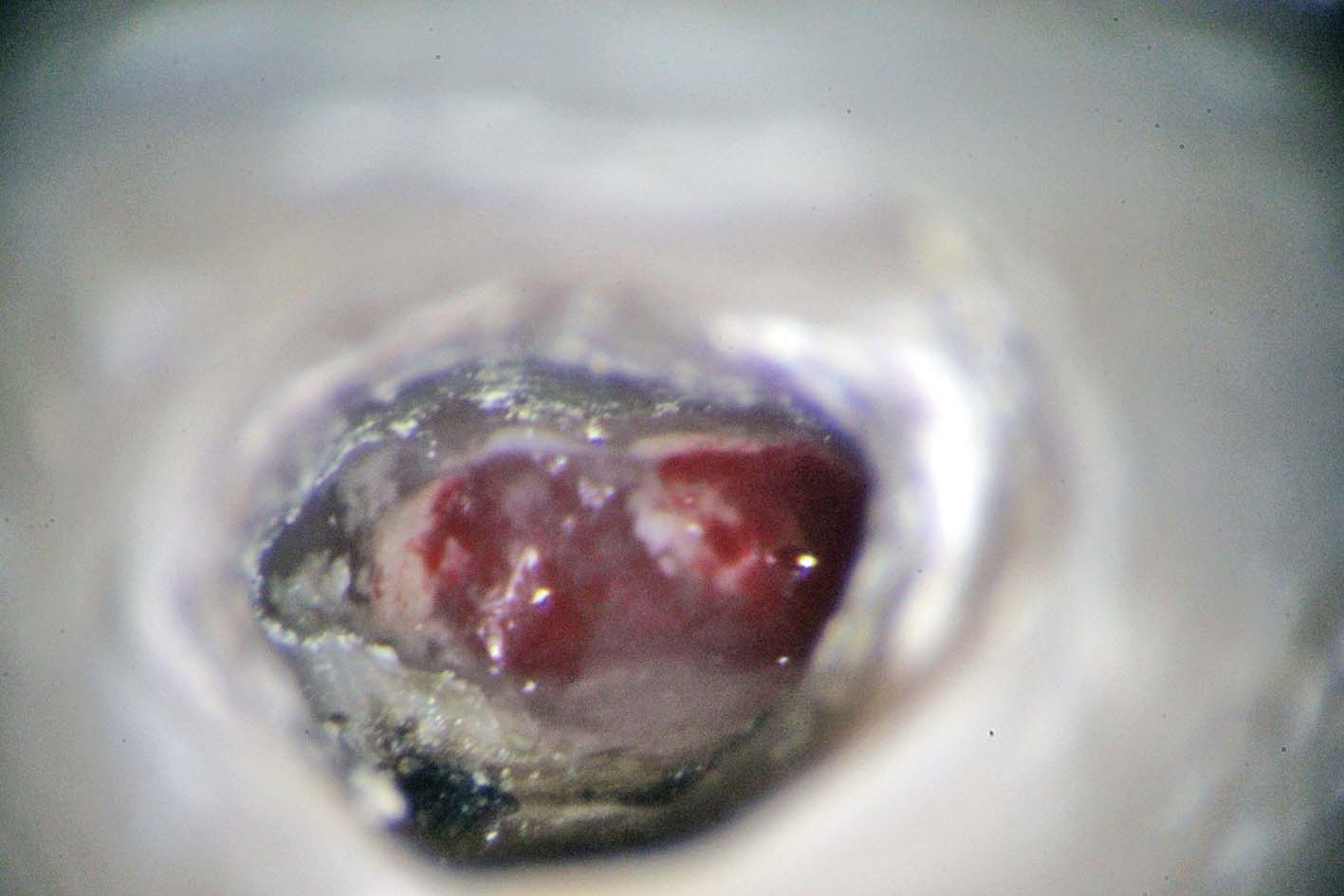
Allo scopo di rimuovere il tessuto di granulazione che aveva invaso il canale radicolare è stata usata una medicazione di idrossido di calcio per una settimana (Figura 24).
Questa, con la sua azione leggermente caustica sul tessuto, ha poi permesso la sua totale rimozione con un ottimo controllo del sanguinamento (Figura 25).
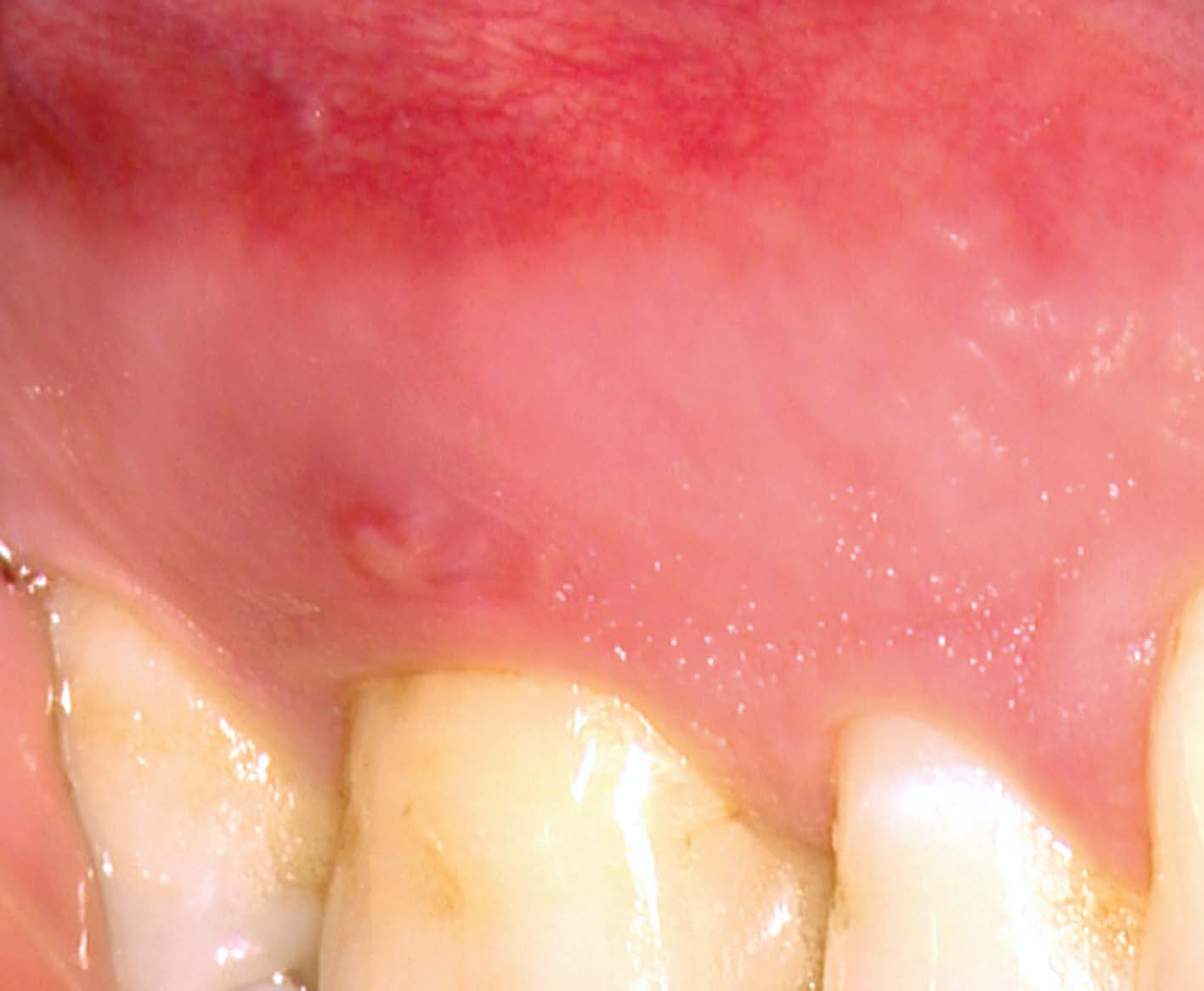
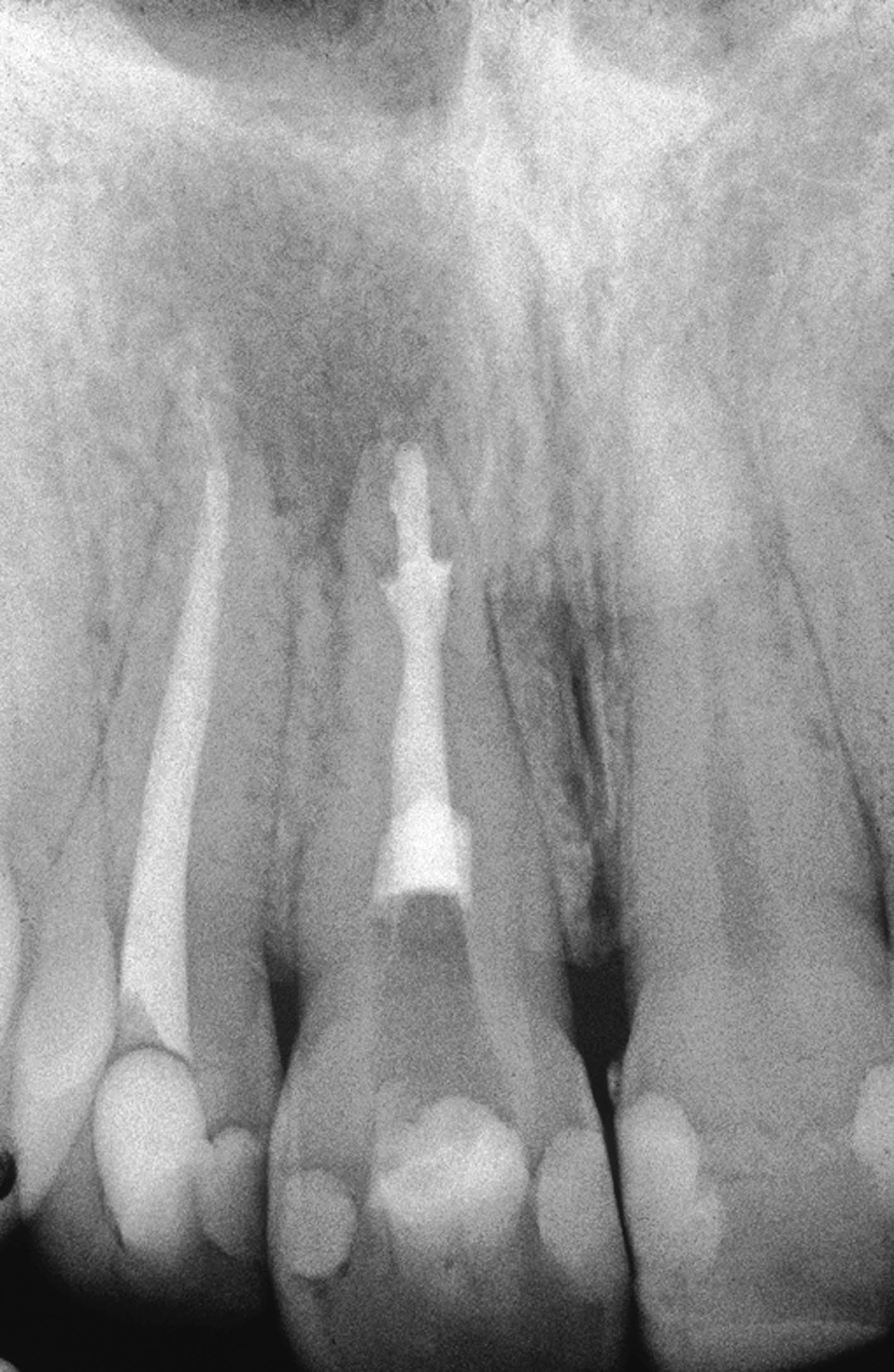
È stato quindi posizionato l’MTA bianco per sigillare la perforazione ed è stata completata la terapia del canale radicolare (Figura 26). I controlli clinico (Figura 27) e radiografico (Figura 28) dopo 3 anni mostrano la completa guarigione della lesione periapicale e il normale aspetto della gengiva antistante la sede della precedente perforazione.
Perforazioni del terzo coronale e delle biforcazioni
Tali perforazioni sono piuttosto frequenti a livello degli incisivi superiori, dove l’errore più spesso commesso è l’utilizzo della fresa con eccessiva angolazione vestibolare. Mentre è fisicamente impossibile eseguire una perforazione sul lato palatino, per la presenza del margine incisale che impedisce un’angolazione troppo palatina della fresa, è frequente l’osservazione della perforazione vestibolare per la tendenza a inclinare la fresa in tale direzione. Ciò accade soprattutto se non si fa uso di un adeguato mezzo ingrandente, oggi rappresentato dal microscopio operatorio, nel tentativo di reperire un canale apparentemente completamente calcificato in seguito a un pregresso trauma.
Perforazioni del terzo coronale possono anche accadere sul pavimento dei molari, quando gli orifizi canalari vengono cercati in posti sbagliati. Tipiche sono quelle nei molari superiori o inferiori, che avvengono per lo sfondamento del pavimento della camera pulpare. Come conseguenza del trauma meccanico, si ha una rapida distruzione del legamento parodontale.
L’osso alveolare immediatamente adiacente alla perforazione si riassorbe con conseguente perdita verticale di osso. Il processo infiammatorio quindi si estende coronalmente lungo le fibre del legamento parodontale, con distruzione del legamento, dell’osso alveolare e delle fibre gengivali sopracrestali. Come conseguenza di ciò, si ha la migrazione apicale dell’attacco epiteliale e le formazione di un grave difetto parodontale10.
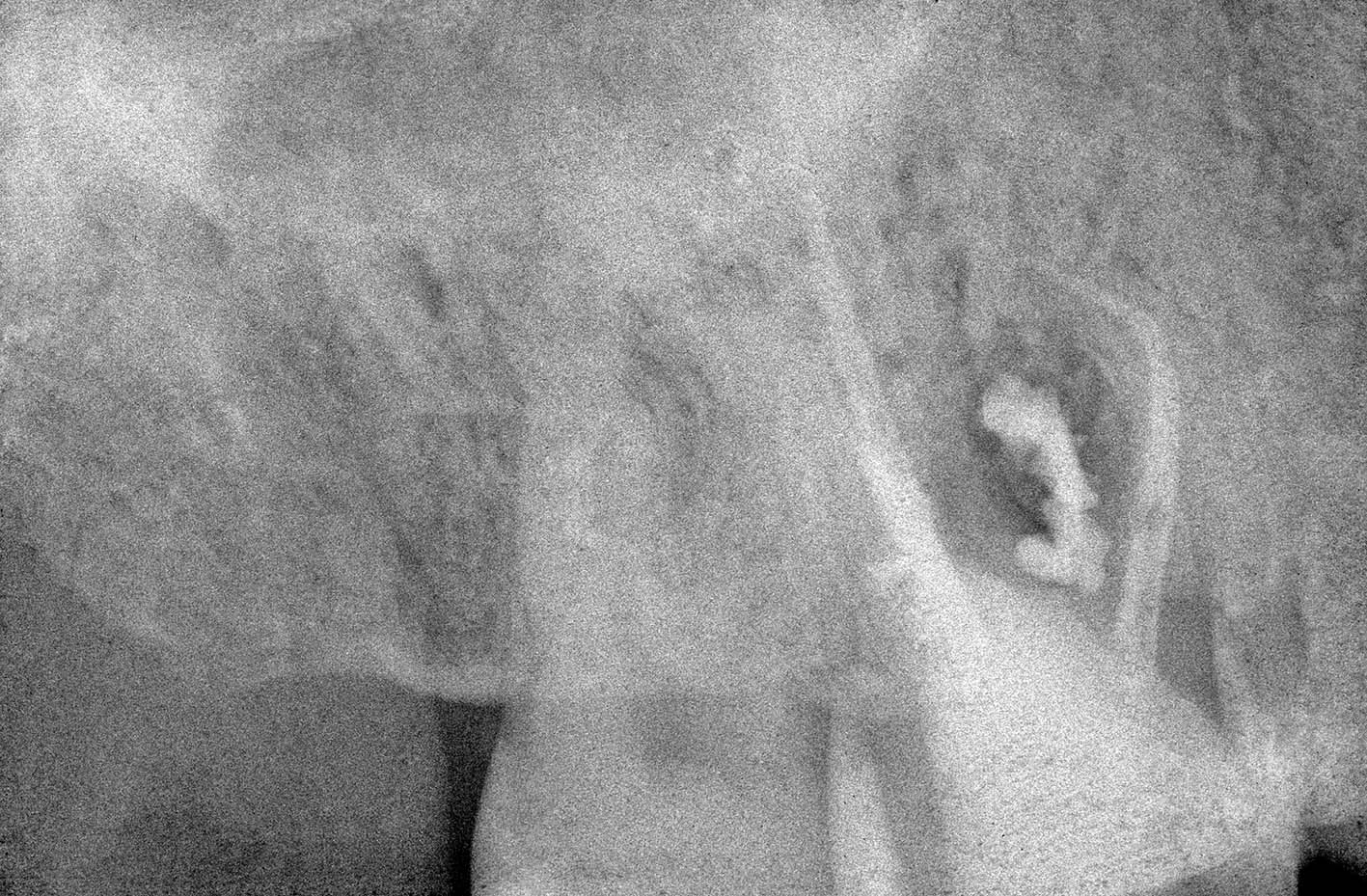
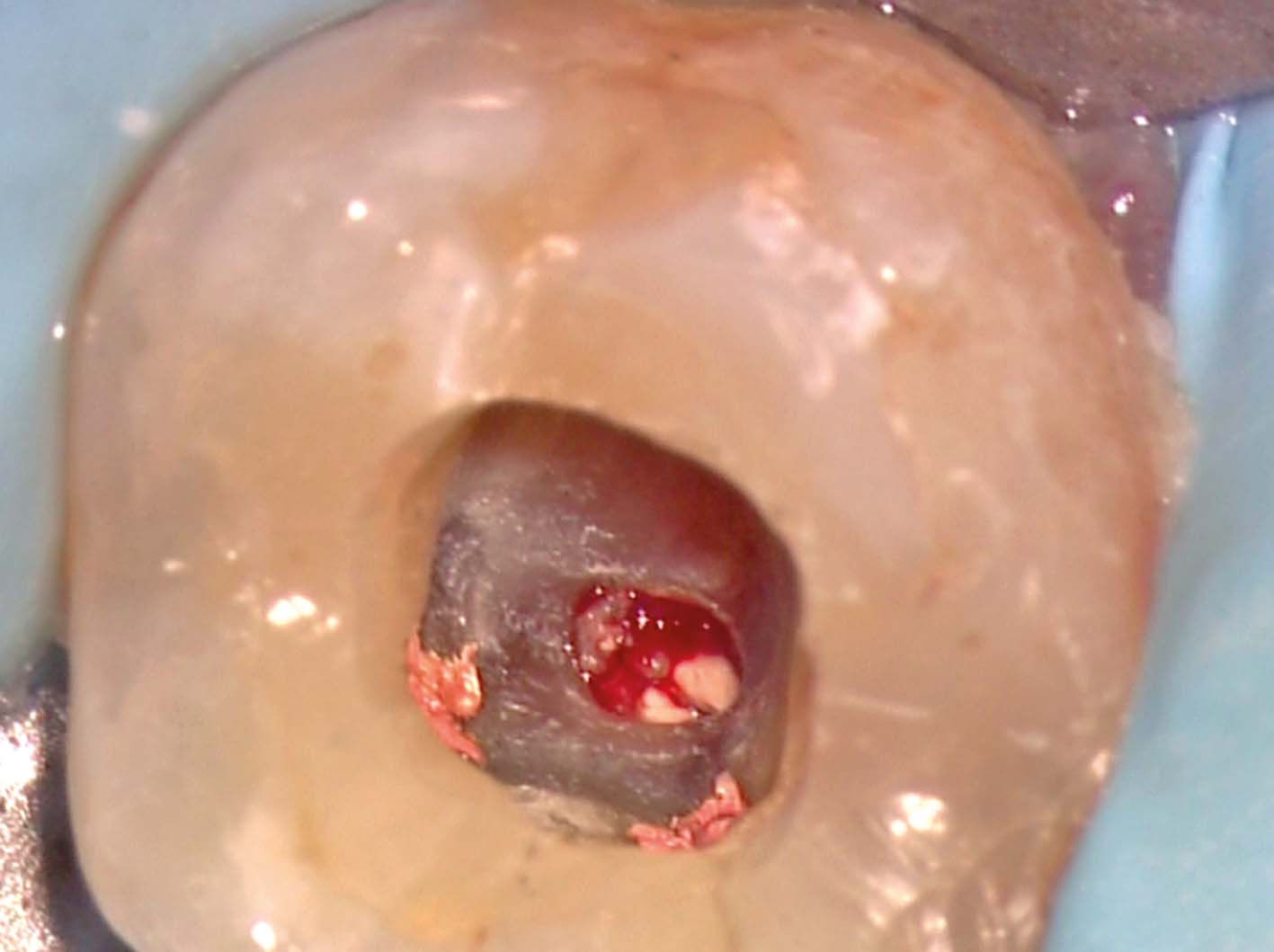
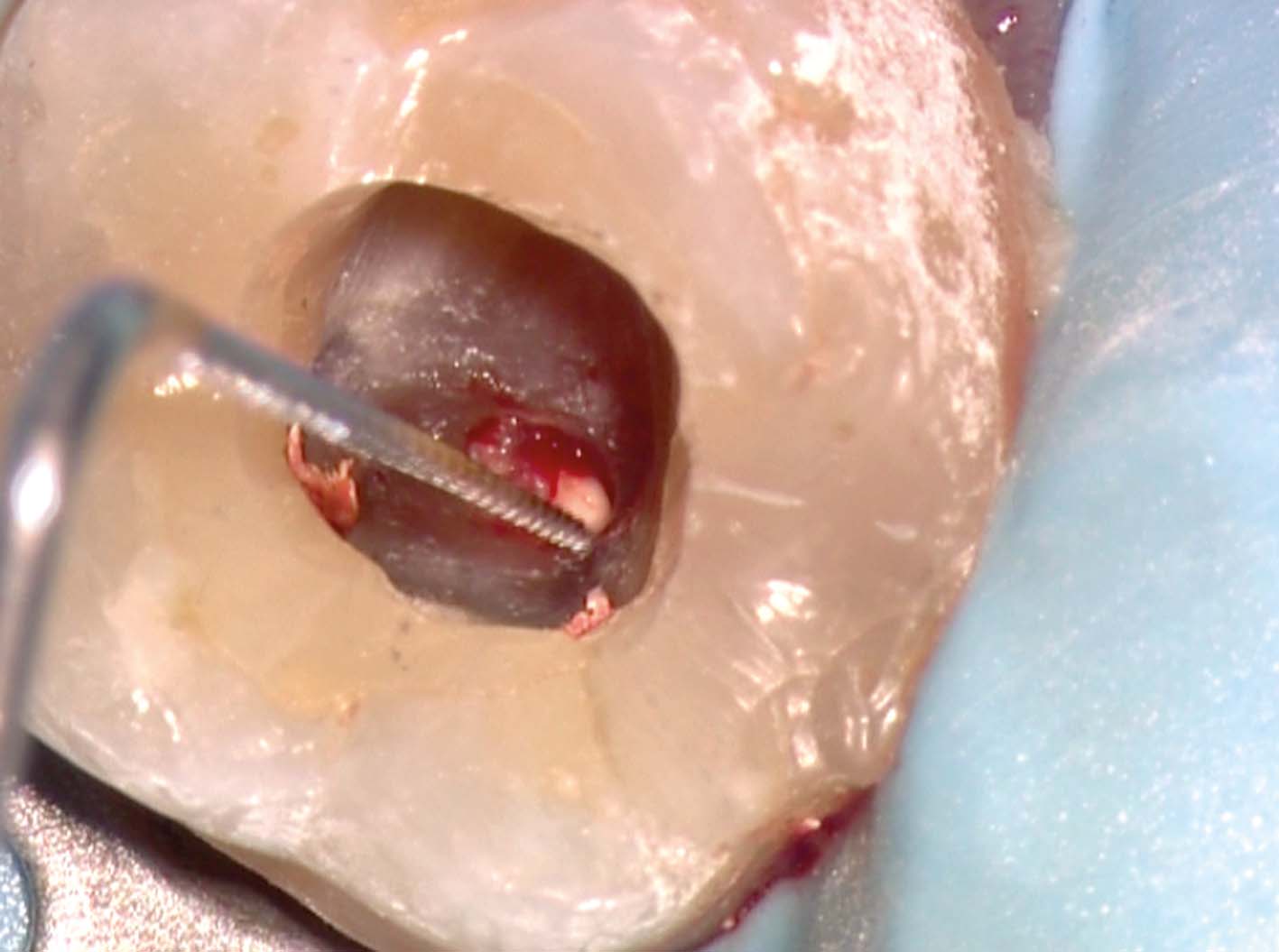
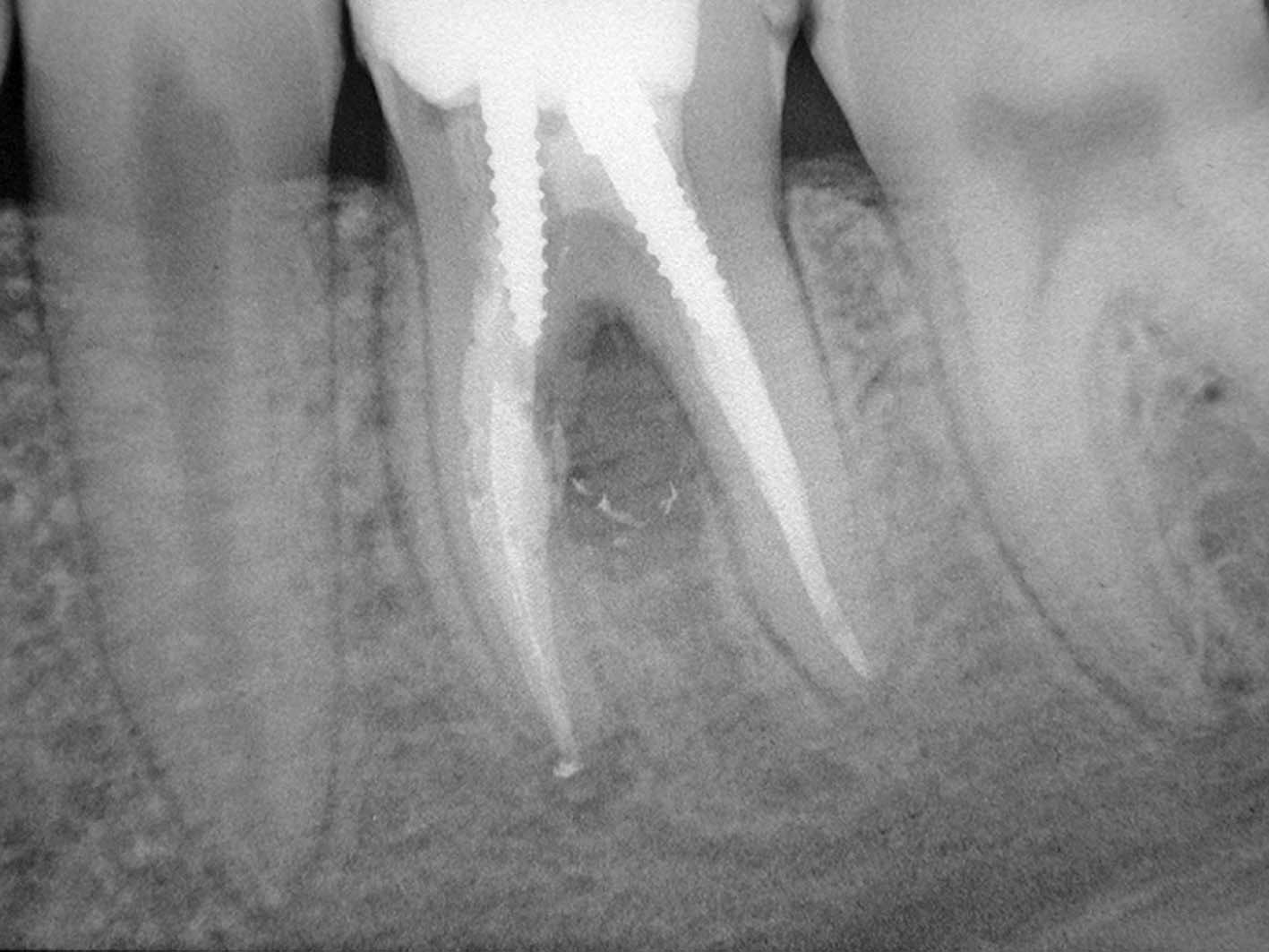
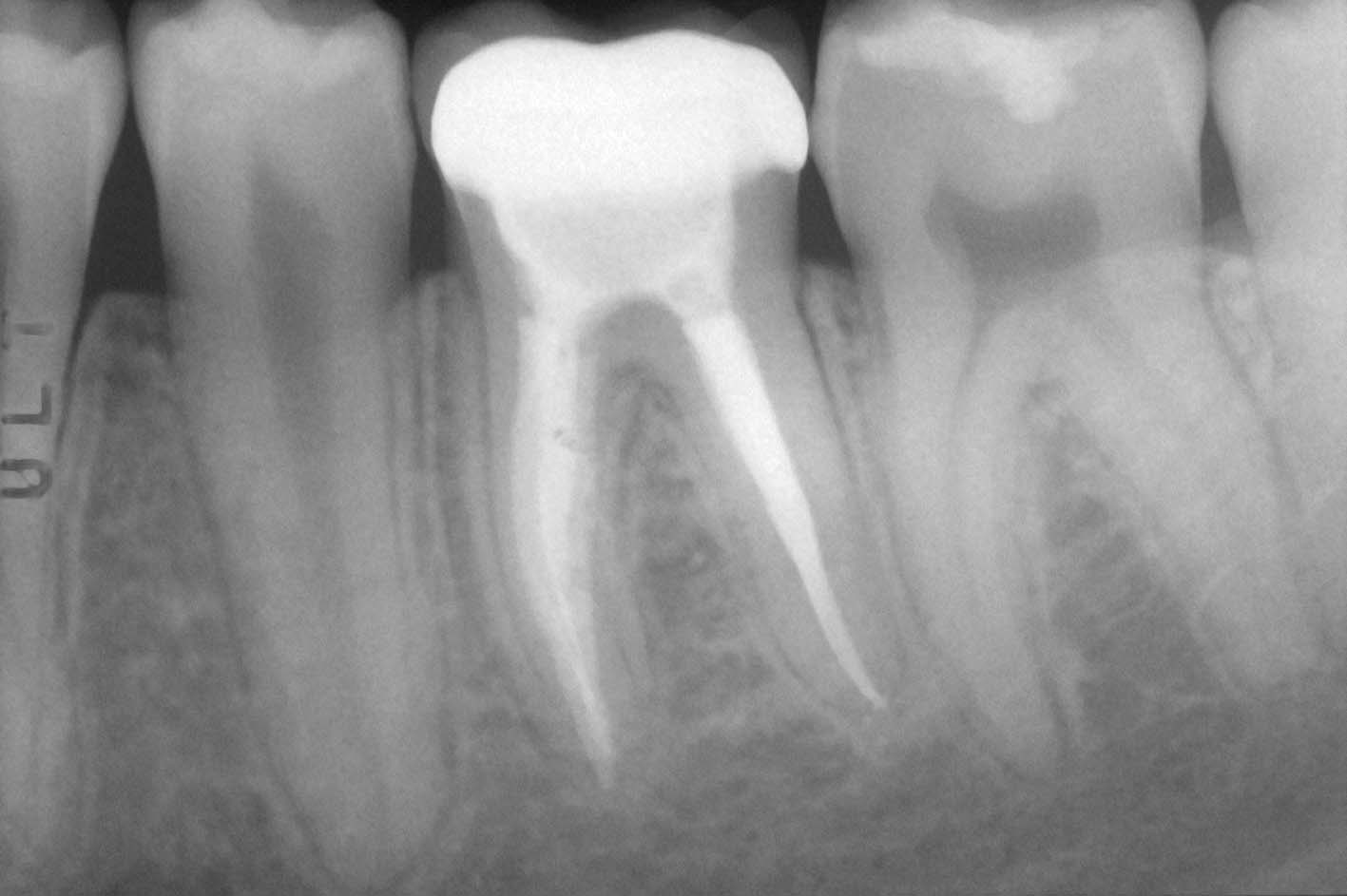
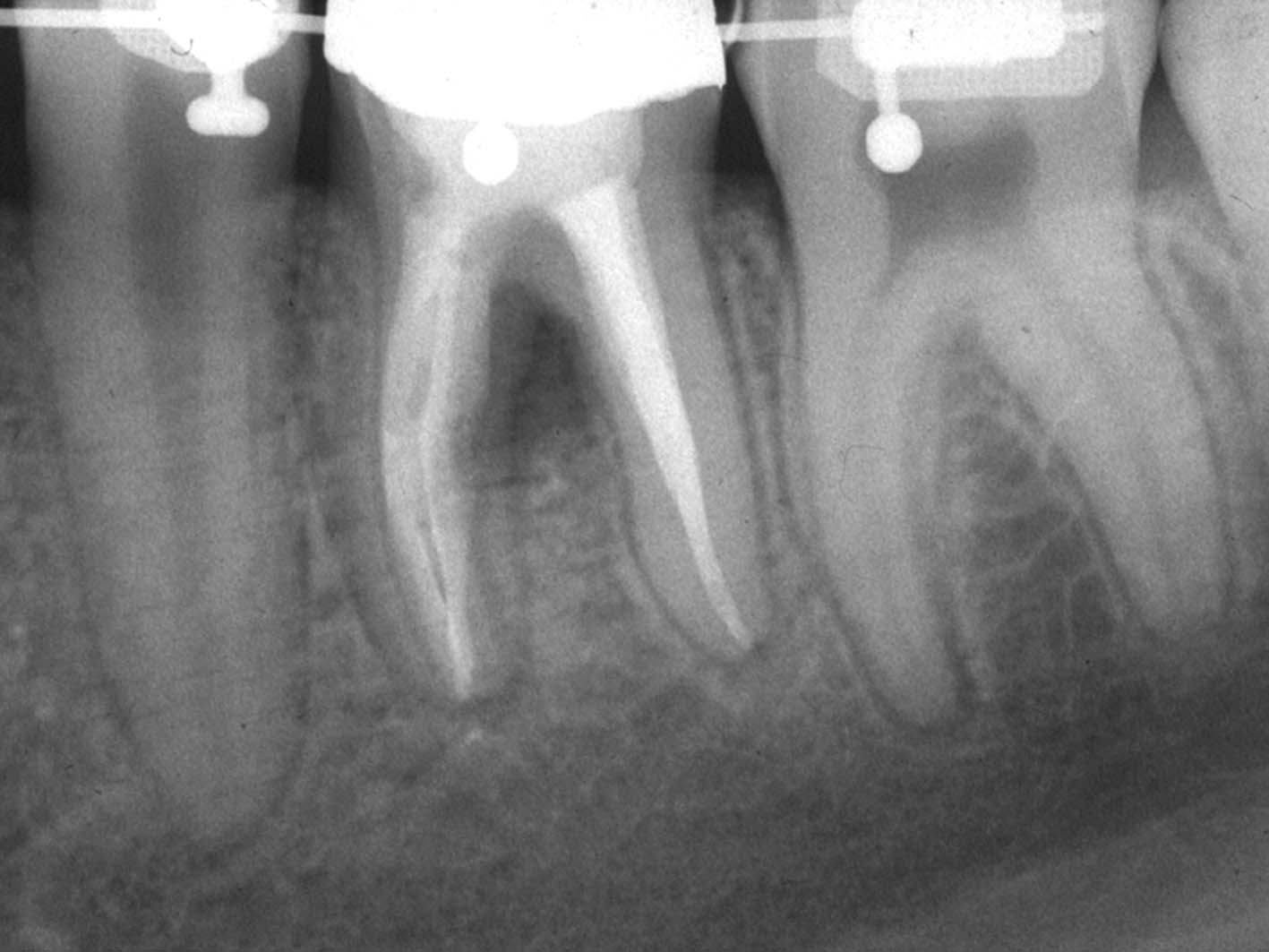
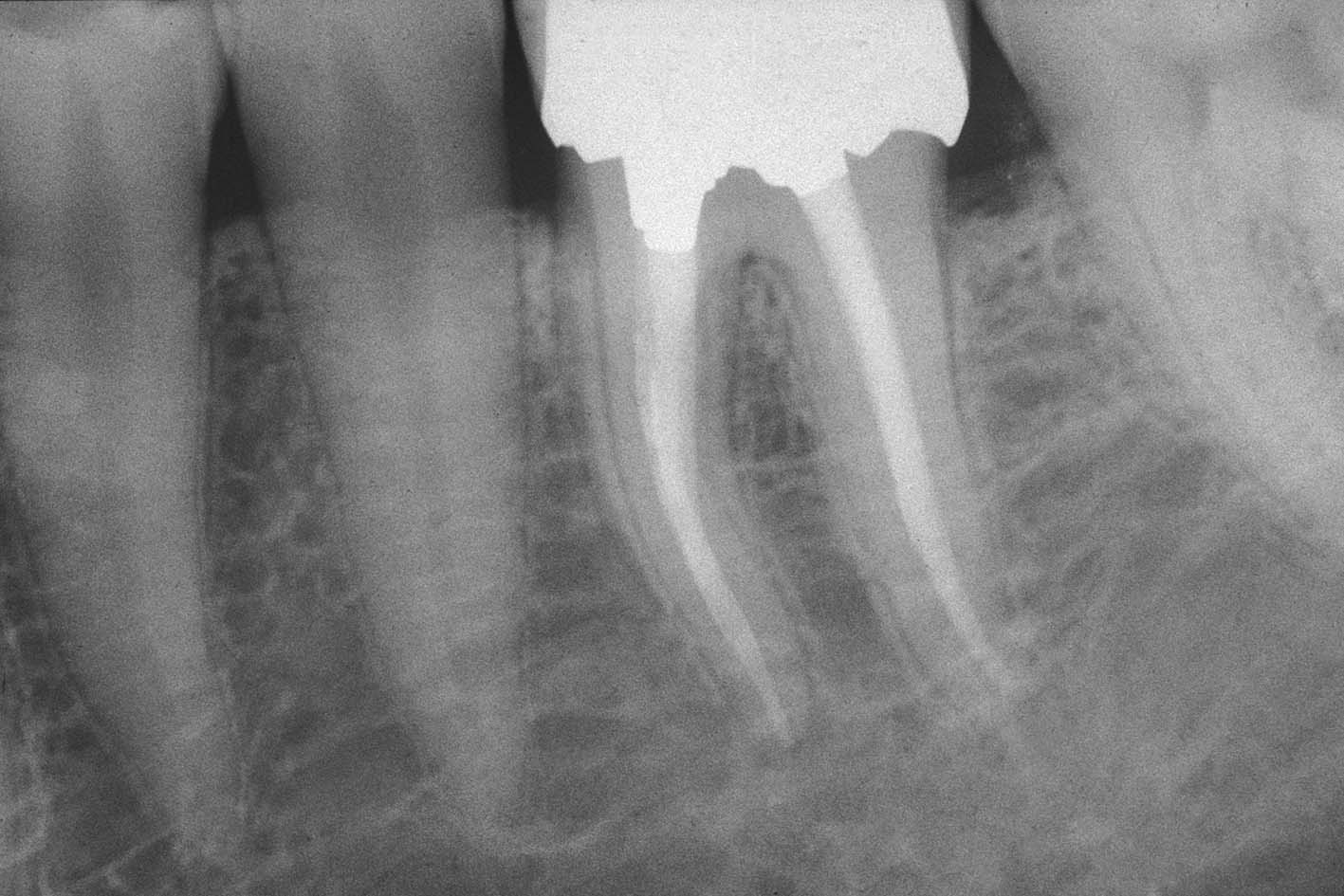
La radiografia preoperatoria del primo molare inferiore sinistro mostra la presenza di una vite canalare nella radice mesiale e di una radiotrasparenza della zona della biforcazione, causata dalla perforazione del terzo medio del canale radicolare (Figura 29) associata a una fistola vestibolare. È stata quindi rimossa la vite canalare (Figura 30), eseguito il ritrattamento e fatta una medicazione con idrossido di calcio per una settimana allo scopo di risolvere l’esistente infiammazione acuta ed elevare il livello del pH a valori più basici. All’appuntamento successivo, documentata la guarigione del tragitto fistoloso, si è proceduto all’otturazione dei canali radicolari con la tecnica della compattazione verticale della guttaperca calda, avendo l’accortezza di otturare il canale della perforazione solo apicalmente al difetto, per non danneggiare con guttaperca o cemento l’orofizio della perforazione (Figura 31). È stato eseguito quindi il “back packing” con MTA, otturando così automaticamente anche l’apertura della perforazione (Figura 32).
Il controllo radiografico dopo due anni mostrava la completa guarigione e la scomparsa della precedente radiotrasparenza della zona della biforcazione (Figura 33). La paziente si è poi sottoposta a terapia ortodontica e il controllo dopo tre anni mostrava la recidiva della lesione e la ricomparsa del tragitto fistoloso (Figura 34). Dopo quindi aver chiesto all’ortodontista di interrompere la trazione ortodontica su quel molare e di stabilizzare il dente, sotto controllo al microscopio operatorio è stato eseguito il ritrattamento del molare e in particolare è stato rimosso l’MTA con l’aiuto di apposite punte da ultrasuoni e ripetuta una nuova medicazione con idrossido di calcio per risolvere l’infiammazione acuta e modificare il pH. Quindi all’appuntamento successivo è stata rifatta l’otturazione dei canali radicolari con la solita tecnica e il “back packing” del canale perforato con MTA (Figura 35). Il controllo radiografico eseguito dopo 16 anni conferma nuovamente il successo
della terapia (Figura 36).
Prognosi
La prognosi delle perforazioni dipende da molti fattori, tra cui il loro livello (terzo coronale, medio o apicale), la loro sede (vestibolare, linguale, mesiale o distale), la forma e le dimensioni (piccola o grande) e infine il tempo trascorso tra l’esecuzione della perforazione e la sua riparazione. Inoltre la prognosi dipende dal materiale usato per la riparazione del difetto, dalla presenza o meno dell’infezione batterica e dalla presenza o meno di fuoriuscita del materiale utilizzato.
- Livello. La letteratura è concorde nell’affermare che le perforazioni del terzo coronale e del pavimento camerale hanno la prognosi più sfavorevole, a causa della loro vicinanza al solco gengivale4, 10-14. Se coronalmente al difetto rimane una buona quantità di tessuto connettivale e osso, ci sono minori possibilità che si instauri un danno parodontale permanente e la guarigione è facilitata. Per questo motivo la prognosi è migliore se la perforazione avviene nel pavimento della camera pulpare di un molare dal tronco lungo (per tronco lungo si intende la distanza tra la giunzione cemento-dentinale e l’altezza della biforcazione).
- Sede. La sede della perforazione non ha importanza se la riparazione avviene per via ortograda. D’altra parte, diventa d’importanza fondamentale se viene scelto l’approccio chirurgico. Sarà cioè facile trattare chirurgicamente una perforazione vestibolare, mentre sarà ben più difficile se non impossibile trattare la stessa perforazione nelle altre sedi, mesiale, distale o palatina o linguale.
- Forma e dimensioni. Come già accennato in precedenza, una perforazione ampia, priva di conicità e con un’apertura ellittica rende la sua riparazione particolarmente difficoltosa, in quanto diventa difficile ottenere un buon sigillo senza un sovrariempimento. Per questo motivo, tali perforazioni richiedono più spesso un approccio chirurgico.
- Tempo. Le perforazioni danno luogo a una reazione infiammatoria con conseguente perdita di attacco. Questo può portare allo sviluppo di una lesione combinata endo-parodontale che spesso richiede un intervento chirurgico con conseguente peggioramento della prognosi. Pertanto, l’intervallo di tempo tra l’esecuzione della perforazione e la sua riparazione deve essere il più breve possibile. Per questo motivo è caldamente raccomandato che questi difetti vengano otturati immediatamente,14 nel corso dello stesso appuntamento nel quale la perforazione è stata eseguita. Questo serve a prevenire la contaminazione batterica e quindi lo svilupparsi della lesione delle strutture adiacenti (attacco epiteliale, legamento parodontale e osso). Inoltre, se queste strutture sono ancora intatte, possono agire da matrice e impedire grossolani sovrariempimenti al momento dell’otturazione.
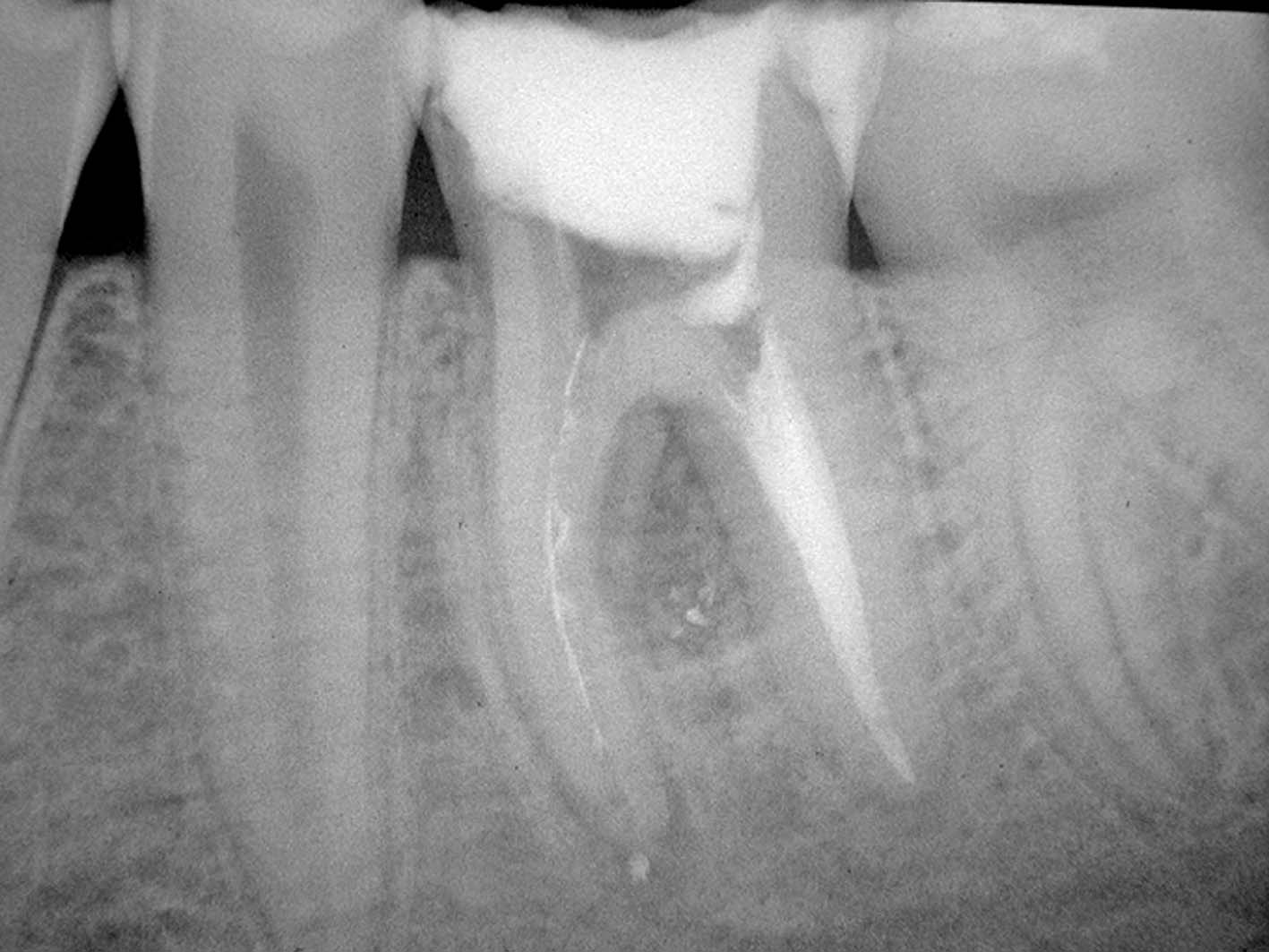
Nel tentativo di trovare gli imbocchi dei canali mesiali del primo molare inferiore è stata eseguita una perforazione all’interno del canale mesio-vestibolare (Figura 37). Uno strumento endodontico collegato al localizzatore apicale conferma la presenza e la profondità della perforazione (Figura 38). È stata eseguita la detersione e sagomatura dei tre canali radicolari (Figura 39) ed è stata fatta la prova dei coni (Figura 40), accertandosi dell’esistenza di un ottimo “tug back” del cono del canale destinato a otturare il canale mesio-vestibolare. Dopo aver parzialmente sezionato tale cono a un livello leggermente apicale rispetto alla profondità della perforazione, il cono è stato introdotto già coperto di cemento endodontico e piegato in direzione mesiale, in modo da non disturbare la perforazione esistente sull’aspetto distale della parete canalare (Figura 41). Dopo aver posizionato il cono alla profondità voluta, sfruttando l’esistente “tug back“ il cono si è diviso in due frammenti, uno apicale rimasto nel canale e uno coronale che è stato rimosso (Figura 42).
Dopo aver eseguito la compattazione della suddetta guttaperca (Figura 43), è stato eseguito il “back packing“ con MTA (Figura 44) otturando così automaticamente la perforazione esistente nel terzo medio del canale (Figura 45). Il controllo radiografico eseguito dopo due anni mostra la completa guarigione e la scomparsa della leggera radiotrasparenza che si era formata nella zona della biforcazione (Figura 46).
Materiali e tecniche
Quando si ripara una perforazione, la visibilità è estremamente importante ed essa è sicuramente migliorata dall’utilizzo di una buona illuminazione e di un adeguato mezzo ingrandente. Il microscopio operatorio ha sicuramente contribuito a rendere queste terapie ortograde molto più predicibili.
Beavers e coll.15 hanno dimostrato che se le lesioni guariscono a contatto con un materiale biocompatibile, e soprattutto in assenza di contaminazione batterica, si ha la completa guarigione del difetto successivo alla perforazione di una biforcazione o a una perforazione laterale vicina al solco gengivale, senza alcuna migrazione apicale dell’attacco epiteliale.
Per la riparazione delle perforazioni sono stati suggeriti molti materiali, tra cui il Cavit,16 l’amalgama,11,17 l’idrossido di calcio,18 la guttaperca.19
Indipendentemente dal materiale usato, i clinici si sono sempre trovati di fronte a due difficoltà.20
La prima era rappresentata dall’ottenere una buona emostasi e dall’evitare dei sovrariempimenti, obiettivi possibili utilizzando una barriera che si adattasse alla biforcazione o alla superficie radicolare. Questa doveva essere biocompatibile, riassorbibile, stimolare la crescita di nuovo osso ed essere posizionata per via ortograda attraverso la cavità d’accesso all’interno del difetto osseo a tre pareti.
Tale matrice interna fornisce una barriera che consente di controllare il posizionamento del materiale riparativo senza avere dei sovrariempimenti. Inoltre garantisce una buona emostasi e un perfetto controllo del sanguinamento. Le barriere più comunemente usate sono rappresentate dal collagene, dall’osso liofilizzato, dal fosfato tricalcico e dal fosfato di calcio.
La seconda difficoltà è rappresentata dalla scelta di un materiale restaurativo che sia facile da usare, che sigilli bene, che sia non riassorbibile, esteticamente accettabile, biocompatibile e che stimoli la formazione di nuovo tessuto.
I materiali comunemente usati per riparare le perforazioni sono stati l’amalgama (oggi caduta in disuso), il cemento resinoso SuperEBA (Bosworth Co.), compositi adesivi, e più recentemente il Mineral Trioxide Aggregate (MTA) (ProRoot, Dentsply Sirona) e bioceramiche (RRM, Brasseler). Attualmente, tutti i materiali elencati, con l’eccezione degli ultimi due, richiedono un campo asciutto per garantire un sigillo adeguato. Il materiale usato come barriera deve essere scelto in modo tale da garantire una preparazione asciutta, il posizionamento del materiale restaurativo e prevenire il sovrariempimento. Nella stragrande maggioranza dei casi l’MTA e le nuove bioceramiche non necessitano della barriera, soprattutto se vengono utilizzati sotto controllo al microscopio operatorio.
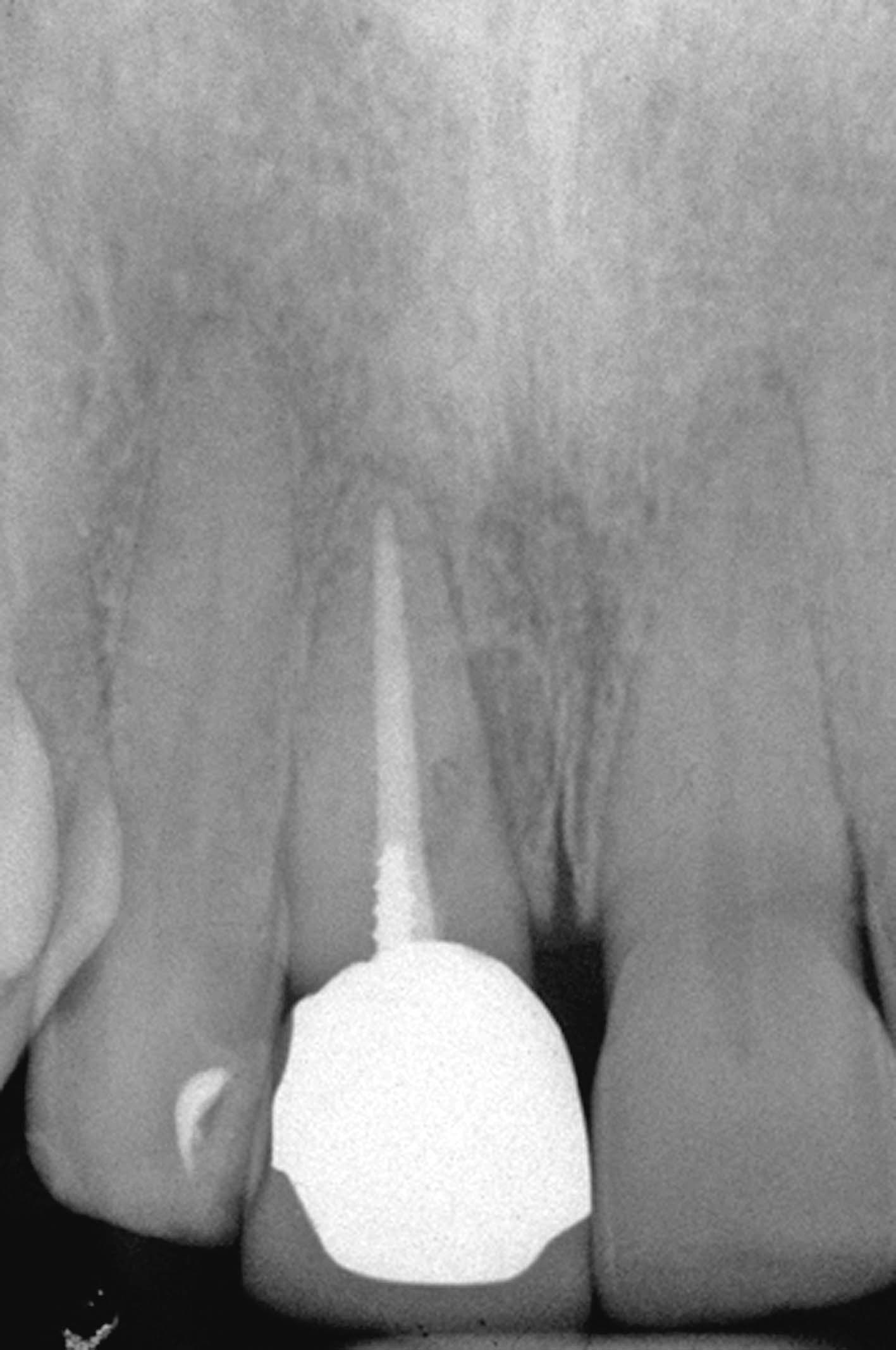
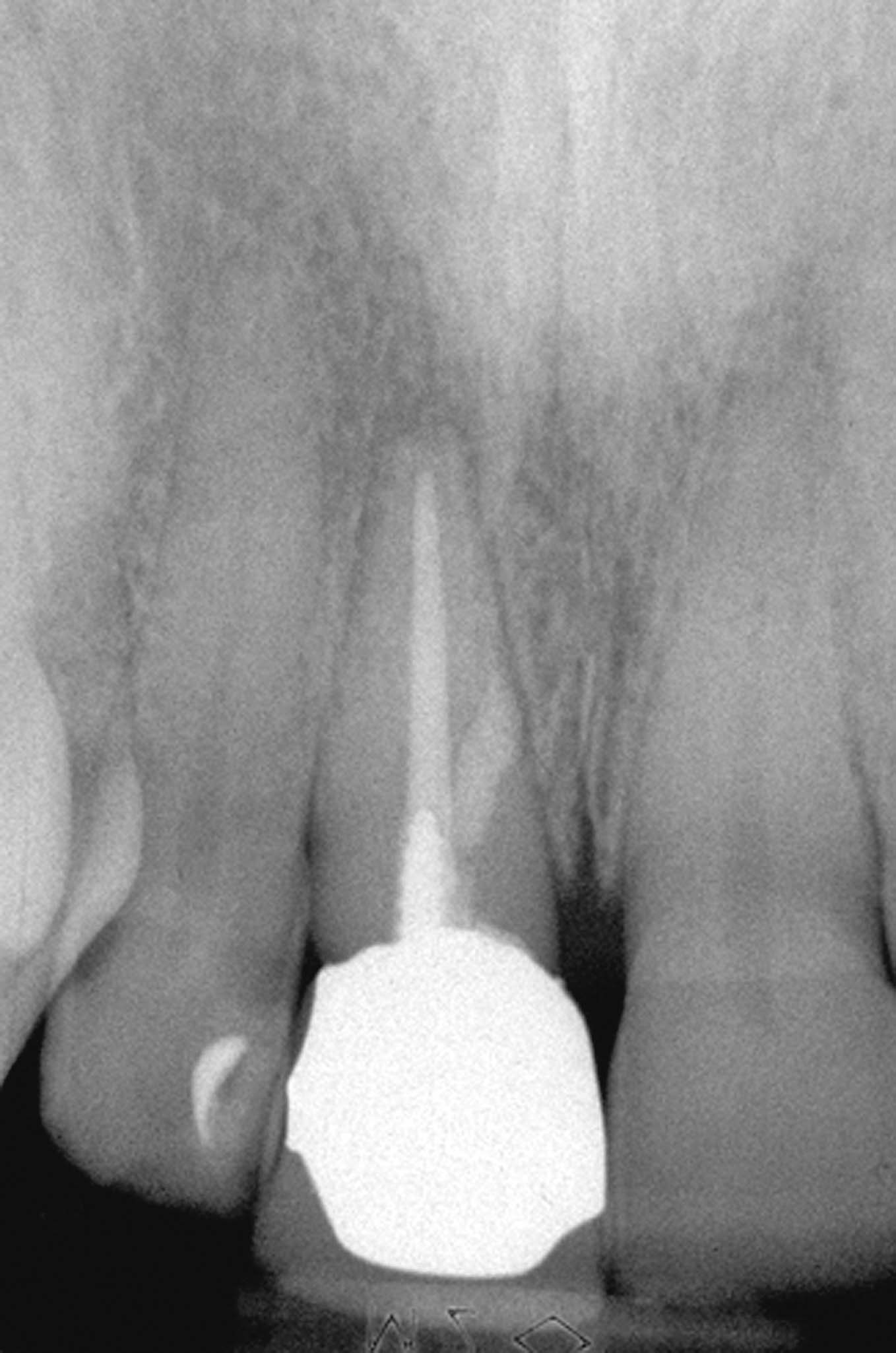
La radiografia preoperatoria dell’incisivo centrale superiore di destra mostra la presenza di una perforazione sull’aspetto mesiale del terzo medio della radice causata dalla erronea angolazione della fresa nel tentativo di creare lo spazio per l’alloggiamento della vite canalare (Figura 47).
Nel corso dell’intervento chirurgico viene accertata la presenza della perforazione e documentata la tipica forma ellittica dell’apertura esterna (Figura 48), provocata dalla fresa che ha perforato la parete canalare con un angolo di 45° circa.
Questo conferma, tra l’altro, la controindicazione all’otturazione ortograda del difetto. È stata quindi preparata la cavità con l’apposita punta da ultrasuoni (Figura 49) e poi otturata la perforazione con MTA bianco. Durante la sua compattazione è stata appoggiata al plugger la punta da ultrasuoni per migliorare l’adattamento del materiale alle pareti canalari e rimuovere le eventuali bolle d’aria incorporate nel materiale durante la sua miscelazione (Figura 50).
La radiografia postoperatoria mostra l’avvenuto sigillo della perforazione (Figura 51) e la radiografia di controllo eseguita dopo quattro anni mostra il successo della terapia (Figura 52).
Riparazione delle perforazioni mediante l’uso di barriera di collagene
Questa tecnica è particolarmente indicata quando, a causa della cronicità della perforazione, si è formata una grossa lesione a lato della radice perforata. Come è stato già accennato, la difficoltà in tale caso è rappresentata dal posizionamento di una solida barriera riassorbibile all’esterno, che assicuri una preparazione asciutta ed uno stop contro il quale condensare il materiale riparativo.
Pertanto è importante stabilire la profondità dal punto di repere al punto in cui il cono di carta risulta costantemente asciutto e che rappresenta il tragitto della perforazione che deve essere sigillato. Il CollaCote (Calcitek) è un collagene riassorbibile (in 10/14 giorni), che consente di ottenere una completa emostasi e un’efficace barriera contro la quale poter condensare il materiale riparativo, è relativamente poco costoso, biocompatibile e incoraggia la crescita di nuovo tessuto.
Il materiale è commercializzato sotto forma di tavolette che possono essere tagliate in piccoli pezzetti da spingere e compattare al di là della perforazione, nella lesione e nell’osso circostante. Per determinare esattamente il limite tra la struttura radicolare e il legamento parodontale, si usano i coni di carta. In questo modo si misura la distanza tra il punto di repere e la superficie radicolare. Il punto bagnato del cono di carta rappresenta il punto al di là del limite della struttura radicolare.
Per determinare il livello della perforazione si possono usare anche altri metodi, come i localizzatori elettronici apicali o liquidi radiopachi introdotti nel difetto per valutare la posizione, l’estensione e quindi il tipo di trattamento richiesto per poter risolvere la situazione clinica. Il metodo comunque oggi più usato e sicuramente più attendibile è rappresentato dalla “Cone Beam Computed Tomography” (CBCT).
Si seleziona quindi il più grande plugger che entra liberamente nel tragitto della perforazione senza impegnarsi contro le pareti dentinali. Basandosi quindi sulle dimensioni del difetto e sull’accesso disponibile, si ritagliano piccoli pezzettini di collagene che vengono veicolati attraverso la cavità d’accesso, spinti attraverso il tragitto della perforazione e compattati all’interno del difetto osseo a tre pareti.
Il plugger cioè compatta i pezzetti di collagene attraverso la perforazione all’interno della lesione al di fuori della superficie radicolare. Se stiamo trattando una grossa lesione ossea piena di tessuto di granulazione, vedremo tipicamente i primi pezzetti di collagene letteralmente sparire all’interno del tessuto stesso. I pezzetti di collagene vengono quindi posizionati in maniera incrementale, fino a riempire il difetto osseo, garantendo così una cavità asciutta per tutta l’estensione della cavità della perforazione. Se si usa la tecnica della barriera, la scelta del materiale riparativo si basa sull’esperienza e la preferenza personale, sulla sua facilità di posizionamento e manipolazione e sui vantaggi e gli svantaggi che un particolare materiale può comportare in quella data situazione clinica. Se si è scelto di utilizzare il SuperEBA, si deve avere l’accortezza di spatolare il cemento resinoso incorporando la maggior quantità possibile di polvere, in modo da ottenere una consistenza la più solida possibile. Si posizionano quindi dei piccoli coni di materiale all’estremità del plugger o di una piccola spatola e con questi si portano all’interno della cavità della perforazione fino a otturarla completamente.
Nonostante l’apparente correttezza della terapia endodontica, il primo molare superiore di destra presenta una certa dolenzia e richiede il suo ritrattamento (Figura 53). La precedente otturazione canalare era stata eseguita con Thermafil e nel corso del ritrattamento si è dimostrata impossibile la completa rimozione del carrier di plastica, evidentemente bene incastrato contro le pareti dentinali del canale mesiovestibolare. Nel tentativo di bypassarlo, stava per essere eseguita una falsa strada con successiva perforazione a livello circa del terzo apicale della radice mesiovestibolare (Figura 54).
Dopo aver completato il ritrattamento ortogrado arrivando là dove i canali avevano permesso di essere sondati e preparati (Figura 55), si è proceduto a eseguire la rimozione chirurgica della porzione apicale delle radici vestibolari e la loro otturazione retrograda con MTA (Figura 56). La radiografia di controllo eseguita dopo due anni mostra il successo della terapia (Figura 57).
Riparazione delle perforazioni mediante l’uso di MTA
La prognosi delle perforazioni è enormemente migliorata dopo l’introduzione dell’utilizzo del microscopio operatorio 21 e del materiale biocompatibile MTA,22 messo a punto da Torabinejad e coll.23 circa a metà degli anni ’90. Si tratta di un cemento endodontico estremamente biocompatibile, idrofilo e capace di stimolare processi di guarigione e osteogenesi.24,25 Si tratta di una polvere di fini triossidi e altre particelle idrofile che induriscono in presenza di umidità. L’idratazione della polvere, infatti, dà luogo a un gel colloidale che solidifica in una struttura dura in circa 3/4 ore. Tale cemento è diverso da tutti gli altri materiali usati per la sua biocompatibilità, per la sua attività antibatterica, per il suo adattamento marginale, per le sue capacità sigillanti ma soprattutto perché è idrofilo e quindi è resistente all’umidità.
Per quanto riguarda la biocompatibilità26,27, Koh e coll.28,29 e Pitt Ford e coll.30 hanno dimostrato che l’MTA non è citotossico nei confronti dei fibroblasti e degli osteoblasti e promuove la formazione del ponte dentinale quando usato negli incappucciamenti diretti.31 Altri studi 32-36 hanno dimostrato la formazione di cemento, legamento parodontale e osso adiacente all’MTA quando questo viene usato per sigillare delle perforazioni o come materiale per otturazione retrograda in endodonzia chirurgica.37
Riguardo all’attività antibatterica,4,38 Torabinejad e coll.39 hanno dimostrato che l’MTA è superiore all’amalgama, ai cementi a base di ossido di zinco-eugenolo e al SuperEBA. Ciononostante il suo spettro di azione è limitato e se si sospetta una contaminazione batterica, è consigliabile usare una medicazione con idrossido di calcio prima di posizionare l’MTA. L’idrossido di calcio inoltre è consigliato anche in presenza di infiammazione acuta, al solo scopo di innalzare il livello del pH. Il cemento MTA infatti non indurisce in presenza di un pH acido, quale è nel caso di una infiammazione acuta. Pertanto, se in presenza di una perforazione è presente anche una fistola, si consiglia di eseguire una medicazione con idrossido di calcio per una settimana in modo da portare il pH ad un livello più basico. L’adattamento marginale e le capacità di sigillo dell’MTA sono di gran lunga superiori a quelle dell’amalgama, dell’IRM e del SuperEBA3,4,6,34,40-43. Come già accennato prima, la caratteristica che contraddistingue l’MTA da tutti gli altri materiali usati per riparare le perforazioni iatrogene è rappresentata dal fatto che è idrofilo. I materiali usati per riparare le perforazioni, per sigillare la cavità retrograda in endodonzia chirurgica, per otturare gli apici immaturi o per proteggere il tessuto pulpare negli incappucciamenti pulpari diretti, sono tutti inevitabilmente in contatto col sangue o con altri fluidi tissutali.
L’MTA è l’unico materiale che non è influenzato dall’umidità né dalla contaminazione da parte del sangue.35 D’altra parte, l’MTA indurisce soltanto a contatto con l’umido. Pertanto, per le suddette caratteristiche e soprattutto per la sua idrofilia, l’MTA può oggi essere considerato il materiale di elezione per sigillare le perforazioni iatrogene o patologiche.44-47 La sequenza operativa per sigillare una perforazione della radice o del pavimento di una camera pulpare è la seguente.
Prima visita
- isolare il campo operatorio con la diga di gomma;
- detergere la sede della perforazione con le comuni irrigazioni a base di ipoclorito di sodio e, se i margini della perforazione sono raggiungibili, con le punte da ultrasuoni;
- nel caso di una contaminazione batterica, fare una medicazione con idrossido di calcio per una settimana;
- applicare 2-3 mm di spessore di MTA;
- controllare radiograficamente il corretto posizionamento del materiale;
- applicare una piccola pallina di cotone bagnato a contatto con l’MTA;
- posizionare il cemento provvisorio.
Seconda visita
- isolare nuovamente il campo con la diga di gomma;
- rimuovere il cemento provvisorio;
- accertarsi dell’avvenuto indurimento dell’MTA;
- completare la terapia.
Per quanto riguarda la sequenza operatoria, è importante fare una distinzione tra una perforazione avente la configurazione di una cavità con 4 pareti senza alcuna connessione con lo spazio del canale radicolare (ad esempio la perforazione del pavimento della camera pulpare di un molare) e la perforazione da “stripping” all’interno dello spazio canalare. La situazione è diversa se la perforazione è sul pavimento, e quindi è una cavità indipendente dall’orifizio canalare, o se invece è nel terzo medio del canale ed è causata da uno stripping per un eccessivo allargamento della parete canalare, dovuto a una sagomatura eseguita senza avere l’accesso rettilineo al terzo apicale del canale, senza cioè aver rimosso le interferenze coronali, senza aver eseguito il “coronal pre-flaring”, oppure per l’alloggiamento di un perno. In questo caso la perforazione non è una cavità indipendente dal canale radicolare, ma è situata sulla parete di dentina all’interno del canale stesso. Non è una cavità con quattro pareti ma è un assottigliamento dello spessore di dentina.
Nel primo caso (perforazione indipendente dall’imbocco del canale), è consigliabile otturare la perforazione prima di eseguire l’otturazione canalare, in quanto questo approccio è più facile e fa risparmiare tempo. Dal momento che, come è stato già detto, il tempo trascorso da quando la perforazione è stata eseguita e il momento in cui viene sigillata ha influenza negativa sulla prognosi, più passa il tempo e più facilmente la perforazione si può complicare con una contaminazione batterica con secondario coinvolgimento parodontale. Pertanto, dopo aver posizionato dei piccoli quantitativi di guttaperca agli imbocchi canalari, usando per esempio della guttaperca termoplastica, o nel caso di un ritrattamento, ancor prima di rimuovere la vecchia otturazione canalare, si ottura la cavità della perforazione con MTA e la precauzione presa prima servirà a evitare che della polvere di MTA cada involontariamente all’interno del vicino canale, ostruendolo. Dopo esserci accertati, nel corso della visita successiva, dell’avvenuto indurimento del materiale, a quel punto si procederà con le normali manovre di detersione, sagomatura e otturazione del sistema canalare come se la perforazione non fosse mai esistita.
Nel caso invece della perforazione da stripping per eccessivo assottigliamento della parete canalare, risulta estremamente difficile riparare la perforazione con MTA prima di aver otturato il canale con la metodica classica, senza intasare il canale stesso con il materiale riparativo. Pertanto è consigliabile eseguire prima l’otturazione del canale apicalmente alla perforazione e poi eseguire il “back packing” con MTA per otturare il resto del canale fino all’orifizio. In questo modo la cavità della perforazione viene a essere sigillata automaticamente. In questo caso, tutte le tecniche a caldo comunemente usate per l’otturazione canalare sono sconsigliate, ad eccezione della tecnica di condensazione verticale della guttaperca calda secondo Schilder. Infatti con la tecnica dell’Onda Continua con il SystemB secondo Buchanan e con la tecnica Thermafil sarebbe impossibile impedire l’otturazione del difetto stesso con la guttaperca e la sua fuoriuscita nei tessuti parodontali.
Con la tecnica di Schilder eseguita sotto microscopio operatorio, invece, si riesce a otturare il canale solo apicalmente alla perforazione, senza disturbare la cavità con guttaperca o con cemento. Per fare tutto ciò, è necessario controllare che il cono di guttaperca che andremo a usare abbia un ottimo “tug back”, ovvero un’ottima ritenzione e attrito contro le pareti canalari del terzo apicale. Si deve quindi misurare al microscopio il livello della perforazione e poi sezionare parzialmente il cono di guttaperca, apicalmente a tale livello, con delle piccole forbici o con un bisturi. Una volta introdotto nel canale già avvolto di cemento endodontico e posizionato alla lunghezza di lavoro, il cono di guttaperca viene fatto ruotare dalle nostre dita in modo che si separi in due porzioni, una resterà all’interno del canale apicalmente alla perforazione, grazie al suo “tug back”, mentre l’altra resterà tra le nostre dita. Dopo aver eseguito la compattazione verticale della porzione apicale, il canale viene riempito interamente con MTA fino al suo imbocco, venendo così a sigillare anche la zona della perforazione. A questo punto, si posiziona una pallina di cotone bagnato al di sopra dell’MTA, si sigilla la cavità d’accesso con cemento provvisorio e si rivede il paziente dopo qualche giorno allo scopo di controllare l’avvenuto indurimento dell’MTA. A questo punto il dente può essere restaurato come se la perforazione non fosse mai stata eseguita.
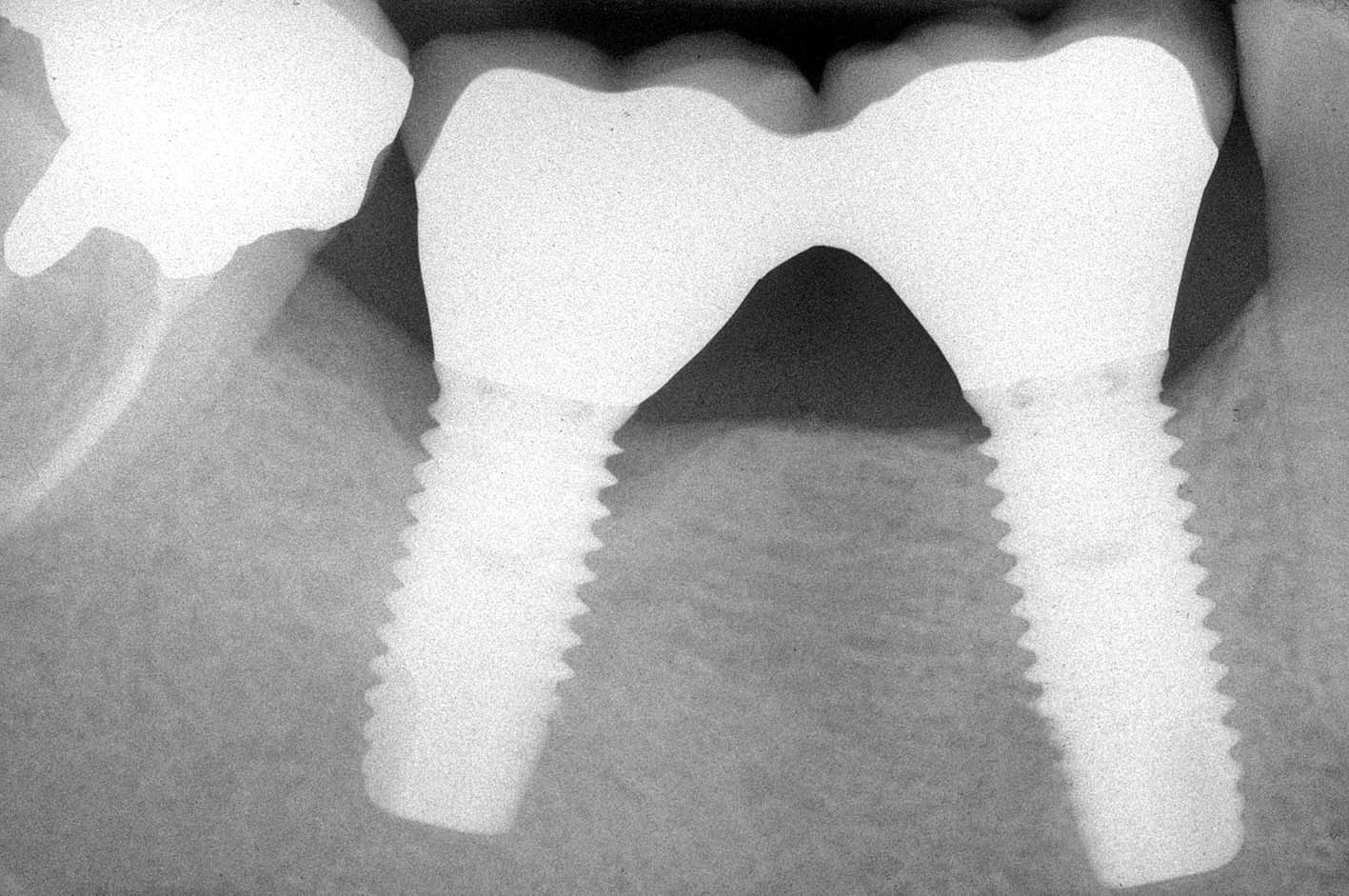
Il primo molare inferiore di destra mostra la presenza di una perforazione del pavimento della camera pulpare e il coinvolgimento della biforcazione (Figura 58). Tale perforazione risultava essere stata eseguita qualche tempo prima. Su richiesta del paziente viene tentata l’otturazione della perforazione con MTA (Figura 59), pur sapendo che la prognosi sarebbe stata infausta.
Al controllo radiografico dopo 6 mesi il materiale appariva parzialmente riassorbito e la compromissione parodontale ancora evidente (Figura 60). Dopo 4 anni il dente risulta essere stato estratto e sostituito con impianto (Figura 61).
Criteri per determinare il successo
Per raggiungere il successo nel trattamento di una perforazione, si devono rilevare i seguenti requisiti:48
- assenza di sintomi, tipo dolore spontaneo o alla palpazione o alla percussione;
- assenza di eccessiva mobilità;
- assenza di una comunicazione tra la perforazione e il solco gengivale;
- assenza di fistola;
- assenza di segni radiografici di demineralizzazione dell’osso adiacente alla perforazione;
- lo spessore del legamento parodontale adiacente al materiale da riparazione deve essere non più del doppio dello spessore del legamento circostante;
- il dente deve essere normalmente funzionante.
Se anche solo uno di questi criteri non è presente, la terapia non può essere considerata un successo.
Riparazione delle perforazioni mediante l’uso dei nuovi materiali in bioceramica
Recentemente sono apparsi sul mercato nuovi materiali a base di bioceramica che hanno dimostrato vantaggiose proprietà sia da un punto di vista fisico che biologico.49
Le bioceramiche sono una combinazione tra il silicato di calcio e il fosfato di calcio e trovano numerose applicazioni nel campo odontoiatrico.50 Tra questi, degno di nota è l’Endosequence BC Root Repair (Brasseler USA, Savannah, GA), disponibile per l’endodonzia dal 2010, che può essere utilizzato come materiale per otturazioni retrograde e per riparare danni radicolari iatrogeni. Esso contiene silicato di calcio, fosfato monobasico di calcio, ossido di zirconio, ossido di tantalo, insieme a riempitivi e agenti ispessenti. Molti studi condotti in vitro e in vivo in animali da esperimento hanno dimostrato che questo materiale è biocompatibile, non tossico, non retraibile e chimicamente stabile a contatto con i tessuti vitali51-53. Ha anche attività antibatteriche contro l’Enterococcus faecalis, probabilmente grazie al suo pH basico54,55. Inoltre, l’Endosequence ha molte proprietà cliniche che ne facilitano l’utilizzo: è pre-miscelato, ha caratteristiche di maneggevolezza simili ai materiali per restauri provvisori, ha un’ottimale radiopacità 50 e non causa scolorimento dei denti.56 Secondo alcuni ricercatori, i materiali a base di bioceramica, quando vengono in contatto con l’umidità, liberano idrossiapatite e danno un’adesione tra la dentina e il materiale da otturazione50. Il tempo d’indurimento sembra non essere costante e varia da un minimo di 4 ore ad un massimo di 48 ore56.
Se a questo punto mettiamo a confronto il ProRoot MTA e l’Endosequence, numerosi articoli basati su ricerche fatte su animali da esperimento arrivano alla conclusione che i due materiali portano a risultati sovrapponibili57,58. I tessuti adiacenti ai materiali esaminati non mostravano segni d’infiammazione o eventualmente solo minimi segni di infiltrato infiammatorio, indipendentemente dal materiale utilizzato. Inoltre, attorno al materiale involontariamente lasciato nei tessuti periradicolari durante l’intervento chirurgico si avevano poche o nessuna cellula infiammatoria. Per questo si può concludere che i materiali a base di bioceramica sono biocompatibili e la loro biocompatibilità è sovrapponibile a quella dell’MTA.
In un recente studio condotto su cani Chen e coll.59 hanno paragonato la guarigione dopo micro-chirurgia usando MTA e bioceramica EndoSequence come materiali per otturazione retrograda. Da questo paragone sono risultate alcune differenze. Nei gruppi trattati con bioceramica si era notato un’area più vasta del bisello radicolare ricoperta da tessuto simile al cemento radicolare, al legamento parodontale e all’osso rispetto ai gruppi trattati con MTA. Questi reperti istologici erano in accordo con i reperti radiografici ottenuti dopo Cone Beam, nei quali i casi trattati con bioceramica mostravano una migliore guarigione attorno all’apice radicolare e nell’area periapicale. Tuttavia i metodi radiografici comunemente usati, come le radiografie periapicali, non evidenziavano alcuna differenza. Si può quindi concludere che piccole differenze legate alla riformazione del legamento parodontale, del cemento e la qualità dell’osso non possono sempre essere apprezzate nelle radiografie periapicali. L’esame Cone Beam è diventato ampiamente disponibile e si sta diffondendo sempre più anche in Italia, grazie alla sua capacità di evidenziare con maggiore precisione e sensibilità la presenza di lesioni periapicali. Pertanto il successo di una terapia potrebbe essere sopravvalutato se paragonato alla sua valutazione dopo esame Cone Beam.60 D’altra parte, l’elevato costo del macchinario e le aumentate dosi di radiazioni che esso comporta per il paziente devono essere giustificati prima che l’esame Cone Beam diventi lo standard per valutare le guarigioni a distanza di tempo.
Infine, a onor del vero, va anche detto che, se da una parte numerosi studi condotti su animali da esperimento hanno dato risultati incoraggianti, a tutt’oggi mancano studi clinici sul comportamento di questi materiali su pazienti49. Attualmente non sono stati pubblicati studi clinici, ad esempio sulle percentuali di successo dopo l’utilizzo di bioceramiche come materiale per otturazioni retrograde, mentre esistono tantissime pubblicazioni che mostrano le altissime percentuali di successo dopo terapie eseguite con l’utilizzo dell’MTA. Questo, pertanto, secondo il parere dell’Autore, rimane ancora il materiale di elezione nelle sue varie indicazioni: incappucciamenti diretti, apici immaturi, perforazioni, otturazioni retrograde.
Conclusioni
Le perforazioni sono comunicazioni iatrogene tra il sistema dei canali radicolari e l’apparato di sostegno del dente che creano una porta di uscita “addizionale” nel sistema dei canali radicolari che richiedono di essere sigillate prima possibile. Una compromissione parodontale, insorgente dalla perforazione, può infatti con il tempo diventare irreversibile e compromettere seriamente la prognosi. Oggi, grazie all’ingrandimento fornito dal microscopio operatorio e ai materiali biocompatibili disponibili, la prognosi delle perforazioni è notevolmente migliorata e le percentuali di successo a lungo termine sono altissime, tanto da giustificare ogni nostro sforzo per salvare i denti interessati anziché sostituirli con impianti.
Corrispondenza
castellucciarnaldo@gmail.com
- Ruddle CJ. Microendodontic nonsurgical retreatment. In Microscopes in Endodontics, Dental Clin. North Am. WB Saunders, Philadelphia 1997; 41(3):429.
- Abou-Rass M., Frank Al, Glick DH. The anticurvature filing method to prepare the curved root canal. J. Am. Dent. Assoc. 1980; 101 (5):793.
- Adamo HL, Buruiana R, Schertzer L, Boylan RJ. A comparison of MTA, SuperEBA, composite and amalgam as root-end filling materials using a bacterial microleakage model. Int. Endod. J. 1999; 32:197.
- Al-Hezaimi K, Naghshbandi J, Oglesby S, et al. Human saliva penetration of root canals obturated with two types of mineral trioxide aggregate cements. J. Endod. 2005; 31:453.
- Al-Hezaimi K, Al-Shalan TA, Naghshbandi J, et al. Antibacterial effect of two mineral trioxide aggregate (MTA) preparations against Enterococcus faecalis and Streptococcus sanguis in vitro. J. Endod. 2006; 32:1053.
- Al-Kahtani A, Shostad S, Schifferle R, Bhambhani S. In-vitro evaluation of microleakage of an ortograde apical plug of mineral trioxide aggregate in permanent teeth with simulated immature apices. J. Endod. 2005; 31:117.
- Andreasen JO, Hjorting-Hansen E. Intraalveolar
root fractures: radiographic and histologic study of 50 cases. Oral Surg. 1967; 25:414. - Nicholls E. Treatment of traumatic perforations of the pulp cavity. Oral Surg. 1962; 15:603.
- Abou-Rass M, Jann JM, Jobe D, Tsutsui F. Preparation of space for posting: effect on thickness of canal walls and incidence of perforation in molars. J. Am. Dent. Assoc. 1982; 104:834.
- Jew RCK, Weine FS, Keene JJJr, Smulson MH. A histologic evaluation of periodontal tissues adiacent to root perforations filled with cavit. Oral Surg. 1982; 54:124.
- Eldeeb ME, Eldeeb M, Tabibi A, Jensen JR. An evaluation of the use of amalgam, Cavit, and calcium hydroxide in the repair of fourcation perforations. J. Endod. 1982; 8:460.
- Himel VT, Brady JJr., Weir JJr. Evaluation of repair of mechanical perforations of the pulp chamber floor using biodegradable tricalcium phosphate or calcium hydroxide. J. Endod. 1985; 11:161.
- Martin LR, Gilbert B, Dickerson AW. Management of endodontic perforations. Oral Surg. 1982; 54:668.
- Seltzer S, Sinai I, August D. Periodontal effects of root perforations before and during endodontic procedures. J. Dent. Res. 1970; 49:333.
- Beavers RA, Bergenholtz G, Cox CF. Periodontal wound healing following intentional root perforations in permanent teeth of Macaca Mulatta. Int. Endod. J. 1986; 19:36.
- Harris WE. A simplified method of treatment for endodontic perforations. J. Endod. 1976; 2:126.
- Benenati FW, Rtoane JB, Biggs JT, Simon JH. Recall evaluation of iatrogenic root perforations repaired with amalgam and gutta-percha. J. Endod. 1986; 12:161.
- Frank AL, Weine FS. Nonsurgical therapy for the perforative defect of internal resorption. J. Am. Dent. Assoc. 1973; 87:863.
- Lantz B, Persson P. Periodontal tissue reactions after surgical treatment of root perforations in dog’s teeth: a histologic study. Odont. Revy. 1970; 21:51.
- Ruddle CJ. Retreatment of root canal systems. J. Calif. Dent Assoc. 1997; 25:11.
- Ruddle CJ. Endodontic perforation repair: using the surgical operating microscope. Dentistry Today 1994; 13:48.
- Cantatore G, Castellucci A, Dell’agnola, Malagnino VA. Applicazioni cliniche dell’MTA. G. It. Endod. 2002; 16:29.
- Torabinejad M, Hong CU, Mcdonald F, Pitt Ford TR. Physical and chemical properties of a new root- end filling material. J. Endod. 1995; 21:349.
- Sarkar NK, Caicedo R, Ritwik P, et al. Physicochemical basis of the biologic properties of mineral trioxide aggregate. J. Endod. 2005; 31:97.
- Thomson TS, Berry JE, Somerman MJ, Kirkwood KL. Cementoblasts maintain expression of osteocalcin in the presenceof Mineral Trioxide Aggregate. J. Endod. 2003; 29:407.
- Ribeiro DA, Hungaro Duarte MA, Matsumoto MA, et al. Biocompatibility in vitro of mineral trioxide aggregate and regular and white Portland cements. J. Endod. 2005; 31:605.
- Ribeiro DA, Matsumoto MA, Hungaro Duarte MA, et al. Ex vivo biocompatibility tests of regular and white forms of mineral trioxide aggregate. Int. Endod. J. 2006; 39:26.
- Koh ET, Mcdonald F, Pitt Ford TR, Torabinejad M. Cellular response to mineral trioxide aggregate. J. Endod. 1998; 24:543.
- Koh ET, Torabinejad M, Pitt Ford TR, Brady K. Mineral trioxide aggregate stimulates a biological response in human osteoblasts. J. Biomed. Mater. Res. 1997; 37:432.
- Pitt Ford TR, Torabinejad M, Abedi HR, et al. Using mineral trioxide aggregate as a pulp-capping material. J. Am. Dent. Assoc. 1996; 127:1491.
- Karabucak B, Lim J, Iqbal M. Vital pulp therapy with minarel trioxide aggregate. Dent. Traumatol. 2005; 21:240.
- Camilleri J, Montesin FE, Papaioannou S, et al. Biocompatibility of two commercial forms of mineral trioxide aggregate. Int. Endod. J. 2004; 37:699.
- Holland R, De Souza V, Nery MJ, et al. Reaction of rat connective tissue to implanted dentin tubes filled with mineral trioxide aggregate or calcium hydroxide. J. Endod. 1999; 25:161.
- Torabinejad M, Watson TF, Pitt Ford TR. Sealing ability of mineral trioxide aggregate when used as a root-end filling material. J. Endod. 1993; 19:591.
- Torabinejad M, Higa RK, Mckendry DJ, Pitt Ford TR. Dye leakage of four root-end filling materials: effects of blood contamination. J. Endod. 1994; 20:159.
- Torabinajad M, Pitt Ford TR, Mckendry DJ, Abedi HR. Histologic assessment of mineral trioxide aggregate as root-end filling material in monkeys. J. Endod. 1997; 23:225.
- Baek S, Plenk H, Kim S. Periapical tissue responses and cementum regeneration with amalgam, SuperEBA, and MTA as root-end filling materials. J. Endod. 2005; 31:444.
- Sipert CR, Hussne RP, Nishiyama CK, Torres SA.:In vitro antimicrobial activity of fill canal, Sealapex, Mineral Trioxide Aggregate, Portland cement and EndoRez. Int. Endod. J. 2005; 38:539.
- Torabinejad M, Hong CU, Pitt Ford TR, Kettering JD. Antibacterial effects of some root-end filling materials. J. Endod. 1995; 21:403.
- Bates CF, Carnes DL, Del Rio CE. Longitudinal sealing ability of mineral trioxide aggregate as a root-end filling material. J. Endod. 1996; 22:575.
- Fisher EJ, Arens DE, Miller CH. Bacterial leakage of mineral trioxide aggregate as compared with zinc-free amalgam, intermediate restorative material and SuperEBA as a root-end filling material. J. Endod. 1998; 24:176.
- Torabinejad M, Smith PW, Kettering JD, Pitt Ford TR. Comparative investigation of marginal adaptation of mineral trioxide aggregate and other commonly used root-end filling materials. J. Endod. 1995; 21: 295.
- Wu MK, Kontakiotis EG, Wesselink PR. Long term seal provided by some root-end filling materials. J. Endod. 1998; 24: 557.
- Bargholz C. Perforation repair with mineral trioxide aggregate: a modified matrix concept. Int. Endod. J. 2005; 38:59.
- De-Deus G, Petruccelli V, Gurgel-Filho E,
Coutinho-Filho T. MTA versus Portland cement as repair material for furcal perforations: a laboratory study using a polymicrobial leakage model. Int. Endod. J. 2006; 39:293. - Main C, Mirzayan N, Shabahang S, Torabinejad M. Repair of root perforations using Mineral Trioxide Aggregate: a long-term study. J. Endod. 2004; 30:80.
- Yildirim T, Gencoglu N, Firat I, eta al. Histologic study of furcation perforations treated with MTA or SuperEBA in dogs’ teeth. Oral Surg. 2005; 100:120.
- Stromberg T, Hasselgran G, Bergstedt H. Endodontic treatment of traumatic root perforations in man: a clinical and roentgenological follow-up study. Sven. Tandlak. Tidskr. 1972; 65:457.
- Shinbori N, Grama AM, Patel Y, et al. Clinical outcome of endodontic microsurgery that uses Endosequence BC Root Repair Materiala s the root-end filling material. J. Endod. 2015; 41(5):607.
- Candeiro GG, Correia FC, Duarte MA, et al. Evaluation of radiopacity, pH, release of calcium ions, and flow of a bioceramic root canal saler. J. Endod. 2012; 38:842.
- Ma J, ShenY, Stojicic S, Haapasalo M. Biocompatibility of two novel root repair materials. J. Endod. 2011; 37:793.
- Damas BA, Weather MA, Bringas JS, Hoen MM. Cytotoxicity comparison of mineral trioxide aggregate and EndoSequence Bioceramic root repair materials. J. Endod. 2011; 37:372.
- Bosio CC, Felippe GS,Bortoluzzi EA, et al. Subcutaneous connective tissue reactions to iRoot SP, mineral trioxide aggregate (MTA) Fillapex, DiaRoot BioAggregate and MTA. Int. Endod. J. 2014; 47:667.
- Lovato KF, Sedgley CM. Antibacterial activity of EndoSequence Root Repair Material and ProRoot MTA against clinical isolates of Enterococcus faecalis. J. Endod. 2011; 37:1542.
- Nair U, Ghattas S, Saber M, et al. A comparative evaluation of the sealing ability of 2 root-end filling materials: an in vitro leakage study using Enterococcus faecalis. Oral Surg. Oral Med. Oral Pathol. Oral Radiol. Endod. 2011; 112:e74–7.
- Charland T, Hartwell GR, Hirschberg C. Patel R. An evaluation of setting time of mineral trioxide aggregate and EndoSequence root repair material in the presence of human blood and minimal essential media. J. Endod. 2013; 39:1071.
- Song M, Kim E. A prospective randomized controlled study of mineral trioxide aggregate and super ethoxy–benzoic acid as root-end filling materials in endodontic microsurgery. J. Endod. 2012; 38:875.
- Song M, Nam T, Shin S, Kim E. Comparison of clinical outcomes of endodontic microsurgery: 1 year versus long-term follow-up. J. Endod. 2014; 40:490.
- Chen I, Karabucak B, Wang C, Wang HG, et al. Healing after root-end microsurgery by using mineral trioxide aggregate and a new calcium silicate-based bioceramic materiala s root-end filling materials in dogs. J. Endod. 2015; 41(3):389.
- Patel S, Wilson R, Dawood A. et al: The detection of periapical pathosis using digital periapical radiography and cone beam computed tomography: part 2 – a 2 year post-treatment follow-up. In. Endod. J. 2012; 45:711.