Autori




Reparto di Parodontologia e Implantologia dell’Istituto Stomatologico Italiano – Milano
Direttore Scientifico: prof. Andrea Edoardo Bianchi
Abstract
Negli ultimi anni, gli impianti corti hanno acquisito un ruolo centrale nelle riabilitazioni implantari di pazienti affetti da gravi atrofie ossee, offrendo vantaggi concreti rispetto alle tecniche di rigenerazione ossea. A differenza dei sostituti ossei, gli short implant hanno dimostrato nel tempo una maggiore stabilità e un’incidenza minore di complicanze. In questo aggiornamento monografico analizzeremo le basi biologiche e le applicazioni cliniche di questa metodica, presentando inoltre un protocollo operativo aggiornato nell’ambito dell’odontoiatria digitale.
Short and ultra short implants: biological bases, biomechanics and clinical applications
In recent years, short implants have gained a central role in the implant rehabilitation of patients with severe bone atrophies, offering tangible advantages over bone regeneration techniques. Unlike bone substitutes, short implants have demonstrated greater long-term stability and a lower incidence of complications. In this monographic update, we will analyze the biological foundations and clinical applications of this approach, also presenting an updated operative protocol within the context of digital dentistry.
Gli impianti short e ultra short, ossia di lunghezza ridotta, hanno un ruolo sempre più centrale nelle riabilitazioni implantari di pazienti con atrofie ossee marcate. Rappresentano un’alternativa valida e meno complessa rispetto alle procedure di rigenerazione ossea, con minore rischio di complicanze. Gli autori esplorano le potenzialità di questa tecnica, presentando un protocollo operativo sviluppato nell’ambito dell’odontoiatria digitale.
Introduzione e razionale
La perdita di osso alveolare dopo l’estrazione dentale è un fenomeno molto comune e significativo. Studi clinici prospettici hanno dimostrato che, nei 12 mesi successivi all’estrazione, la larghezza della cresta alveolare può ridursi fino al 50%, pari a una perdita di 5-7 mm di tessuto osseo, con circa due terzi di questa riduzione che si verifica nei primi tre mesi. La riduzione del volume osseo alveolare dopo l’estrazione può interferire con il posizionamento degli impianti dentali e influenzare il successo del trattamento protesico, fisso o rimovibile, sia dal punto di vista funzionale che estetico. Per questo motivo, è sempre auspicabile prevenire la perdita di tessuto. Tuttavia, se non vengono adottate strategie di preservazione del sito estrattivo, come la rigenerazione tessutale guidata o il posizionamento immediato di impianti, la quantità di osso disponibile potrebbe non essere sufficiente per un corretto posizionamento implantare, rendendo necessari interventi di rigenerazione ossea più complessi e invasivi. Da questa esigenza, sono nate e si sono affermate nel tempo strategie alternative per superare i limiti delle metodiche rigenerative, come l’impiego di impianti corti. Questi consentono di ovviare alla ridotta disponibilità ossea, offrendo soluzioni più conservative e meno invasive. Diventa quindi fondamentale intervenire tempestivamente per preservare il volume osseo e garantire il successo delle future riabilitazioni protesiche.
Background della ricerca
Una revisione della Cochrane condotta da Esposito M et al. nel 2009 conclude affermando che le tecniche di aumento osseo possono essere efficaci, ma non è ancora chiaro quale sia la migliore; gli impianti corti, inoltre, rappresentano una valida alternativa all’aumento verticale di osso nella mandibola atrofica. La revisione ci ricorda poi come le complicanze, soprattutto nelle tecniche di aumento verticale, siano frequenti.
Lo stesso autore, più recentemente (2019), ha poi effettuato una revisione di studi clinici randomizzati per confrontare il successo clinico di protesi fisse supportate da impianti di lunghezza compresa tra 4 e 8 mm con quelli di protesi supportate da impianti più lunghi inseriti in mandibole atrofiche verticalmente aumentate, dopo un follow-up di cinque anni. A cinque anni dal carico, i tassi di fallimento protesico e implantare erano simili tra i due gruppi, ma il numero e la gravità delle complicanze, così come la perdita ossea marginale peri-implantare, erano maggiori negli impianti lunghi inseriti in mandibole con aumento di osso verticale. Gli stessi autori aggiungono che saranno necessari studi più ampi e follow-up più lunghi (fino a 10 anni dopo il carico) per confermare o smentire questi risultati preliminari. Tuttavia, nel frattempo, gli impianti corti potrebbero rappresentare l’opzione preferibile.
Mendes PA et al. nel 2023 hanno effettuato un’ulteriore analisi degli studi presenti in letteratura, illustrando come gli impianti extra-corti si siano dimostrati altrettanto efficaci rispetto agli impianti standard inseriti in zone con innesto osseo, anche a lungo termine. Inoltre, hanno presentato meno complicanze biologiche, tempi di trattamento più brevi e una maggiore stabilità della cresta ossea peri-implantare.
A tal proposito, per quel che concerne la classificazione, come specificato anche da un ITI Consensus Report del 2018, ormai si tende a parlare di impianti short e ultra short con misure uguali o al di sotto dei 6 mm. Negli anni, infatti, le classificazioni sono state aggiornate e il range per considerare un impianto come corto è stato rivisto, rispetto agli 8 mm di un tempo.
La letteratura sembra d’accordo nell’affermare che il ruolo degli impianti corti è ormai cruciale nelle riabilitazioni implantari in osso atrofico, sia per quanto concerne la morbilità del paziente, sia per il successo clinico e medio e lungo termine.
Scopo della ricerca
Scopo di questo contributo è documentare l’opportunità offerta da un protocollo implanto-protesico graftless, che prevede l’impiego di impianti dentali corti, per la risoluzione di gravi atrofie dei mascellari. Come abbiamo visto, negli ultimi decenni è stato enfatizzato sia l’utilizzo di biomateriali sia di innesti di osso autologo; questi ultimi sono da sempre considerati il gold standard nelle tecniche di normalizzazione delle creste edentule a scopo implantoprotesico. La revisione della letteratura e i controlli clinici a distanza di pazienti trattati con innesti hanno spesso evidenziato l’instabilità dell’osso perimplantare che più facilmente sembra andare incontro a riassorbimento osseo o a fenomeni di perimplantite.
Per ovviare a questo problema, sempre più contributi clinici in letteratura propongono l’ancoraggio implantare in zone anatomiche complesse come l’area pterigoidea, zigomatica o transinusale; in realtà la chirurgia di questi distretti presuppone una curva di apprendimento specifica e operatori altamente esperti, in grado di gestire le gravi complicanze che possono derivare. L’utilizzo di impianti short e ultra short, invece, intende coniugare il concetto di mini-invasività, grazie allo studio digitalizzato dell’osso residuo, al potenziale biologico dell’osso nativo, indirizzando la modificazione del tessuto perimplantare attraverso l’induzione di un corretto carico protesico in grado di modificare la morfostruttura.
Gli impianti short e ultra short vogliono quindi conseguire il successo riabilitativo implantoprotesico là dove siano ancora presenti minime quote di osso nativo in zone crestali mascellari sub-antrali o in creste distali altamente atrofiche mandibolari, senza la necessità di una chirurgia preimplantare avanzata di integrazione con innesti per la normalizzazione del distretto atrofico.
La corretta comprensione delle regole che sottendono il successo degli impianti short e ultra short nelle varie tappe, dallo studio del caso alla corretta scelta dell’impianto attraverso uno studio di chirurgia guidata, fino a concretizzarsi in un carico protesico dilazionato secondo le regole biologiche dell’adattamento appositivo dell’osso, permette di formulare innovativi piani di trattamento nella risoluzione delle gravi atrofie ossee.
Gli impianti short e ultra short
Il protocollo di impianti short e ultra short è una metodica clinica che prevede l’utilizzo di impianti dentali limitati a 4-6 mm di lunghezza, prodotti e approvati dalle normative CEE ed FDA. Tale metodica, ormai consolidata nella comunità scientifica, prevede un protocollo chirurgico dedicato per la preparazione del sito ricettore, meglio se in chirurgia guidata o pilotata, con frese dotate di stop di profondità in modo da minimizzare la possibilità di provocare danni iatrogeni su strutture anatomiche di rispetto nel mascellare e nella mandibola.
L’utilizzo di questi impianti trova la sua massima espressione nella mandibola con gravi atrofie, determinate non solo dall’edentulia, ma soprattutto dall’utilizzo incondizionato di protesi rimovibili a supporto mucoso scheletriche o semplicemente incongrue, dalla guarigione di gravi processi osteitici di varia natura, da agenesie dentarie, traumi e interventi di resezione parziali per patologie che colpiscono il distretto.
Analoga indicazione è stata individuata nelle zone posteriori del mascellare superiore, dove l’atrofia grave si accompagna al riassorbimento crestale e alla pneumatizzazione del seno mascellare conseguenti alla perdita degli elementi naturali e quindi alla mancanza dei segnali provenienti dal parodonto.
A nostro avviso, gli impianti short e ultra short devono trovare anche un campo di applicazione più attuale nella risoluzione di edentulie in zone ad alto impatto estetico, in particolare in adulti giovani o di media età, quindi con una lunga aspettativa di vita.
L’evidence-based dentistry ha infatti dimostrato che, dopo circa sette anni dall’incorporazione degli impianti, i pazienti vanno maggiormente incontro a fenomeni di perimplantiti. La presenza di impianti standard (8-12 mm) rende gli operatori più cauti sia nell’indicare un intervento precoce di rimozione implantare sia nel ricorrere a tecniche di rigenerazione ossea, che peraltro non hanno ancora dimostrato una prevedibile re-osteointegrazione, probabilmente per l’impossibilità di ottenere una superfice implantare sterile.
L’atteggiamento che permane è quello di una prudente attesa accompagnata da una blanda terapia causale, lasciando di fatto proseguire l’avanzamento del cono di riassorbimento osseo, che di norma si approfonda lentamente in assenza di dolorabilità e con ascessi solo saltuari. L’impianto in questi casi viene rimosso solo alla perdita dell’ultima porzione di osteointegrazione anchilotica, quando la mobilità dello stesso sopravviene assieme a una dolorabilità spiccata. Di contro, di norma il danno tessutale osseo da una configurazione a imbuto iniziale si esprime con la perdita delle sottili pareti di corticale, esitando nel tempo in una guarigione che, il più delle volte, non permette un nuovo ripristino implanto-protesico congruo dal punto di vista estetico-funzionale.
Il nostro gruppo di lavoro è stato tra i promotori della sensibilizzazione del paziente più giovane a questo nuovo atteggiamento terapeutico, che vede nell’impianto più corto, quindi più facilmente rimovibile, non tanto l’insuccesso più precoce bensì il successo a lungo termine, considerando la possibilità di conservare il substrato per un nuovo ancoraggio implanto-protesico. Allo stesso modo, abbiamo applicato con successo questa metodica nella risoluzione implanto-protesica in un gruppo di pazienti adulti, più avanti con l’età rispetto al gruppo precedente, dove l’improvvisa perdita di denti decidui persistiti in arcata fino a quel momento aveva creato la necessità di risolvere una situazione di monoedentulia in un substrato osseo occupato dall’elemento dentario definitivo rimasto incarcerato in inclusione ossea e spesso ormai anchilotico.
Questa opzione, che senza presupposti biologici validi non avrebbe senso considerare, si è dimostrata una valida alternativa alla più invasiva chirurgia estrattiva preimplantare, condizione assoluta per posizionare impianti standard.
Presupposti biologici
L’osso è un tessuto che possiede la capacità intrinseca di adattarsi all’ambiente al quale è soggetto (Wolff 1870). Questa capacità di convivere con successo con le forze esterne è raggiunta e mantenuta solamente grazie al modellamento e rimodellamento adattativo del tessuto stesso, in risposta alle richieste meccanico-funzionali (Chamay e Tschanz 1972; Goodship et al. 1979; Churches e Howlet 1981; Lanyon et al. 1982). Come risultato, il tessuto osseo è continuamente costretto a un processo ricostitutivo tale da garantire massa idonea alle nuove esigenze funzionali intervenute (Rubin e Lanyon 1984, Rubin 1988).
Questo fenomeno rappresenta l’espressione dell’attività delle sue cellule che, apponendo o riducendo la quantità di matrice mineralizzata, adattano l’architettura dell’osso in modo che possa offrire la massima resistenza alle sollecitazioni con la minima quantità di materiale da costruzione (Lozupone e Favia 1982).
Il substrato osseo, che dopo l’incorporazione chirurgica dell’impianto ha organizzato soltanto la sua parte tessutale più prossima al titanio, in base alla specificità molecolare di questo (Albrektsson et al. 1982; Albrektsson 1983; Albrektsson e Hansson 1986; Albrektsson e Jacobsson 1987; Sennerby 1991), al momento del carico dovrà inevitabilmente riorganizzarsi verso un tessuto competente per rispondere alle esigenze meccaniche funzionali, in relazione alla nuova situazione biomeccanica intervenuta.
La maggior percentuale di insuccessi con protocolli che prevedono un carico differito degli impianti si verifica soprattutto nel primo periodo di funzionalizzazione (Brånemark et al. 1977; Adell et al. 1981). Questa complicanza è da attribuirsi a un’incapacità dell’osso perimplantare, riparato dopo l’incorporazione dell’inserto in condizioni di silenzio funzionale, di supportare un lavoro biomeccanico erogato improvvisamente, al momento della protesizzazione. Ciò conferma che, se i rapporti interfacciali tra impianti in titanio e tessuto osseo sono strettamente legati alle caratteristiche chimico-fisiche di superficie di questo materiale (Osborn e Newsley 1980; Furlong e Osborn 1991), la compatibilità di una riabilitazione implantare, in termini di stabilità secondaria e duratura nel tempo in condizioni di carico, è invece prerogativa del raggiungimento di un equilibrio ottimale tra sollecitazioni meccaniche e grado di competenza ossea a sopportarle (Bianchi et al. 1994a, 1994b, 1994c, 1994d, 1994e).
Il substrato osseo, che dopo l’incorporazione chirurgica dell’impianto ha organizzato soltanto la sua parte tessutale più prossima al titanio, in base alla specificità molecolare di questo (Albrektsson et al 1982; Albrektsson 1983; Albrektsson e Hansson 1986; Albrektsson e Jacobsson 1987; Sennerby 1991), al momento del carico dovrà inevitabilmente riorganizzarsi verso un tessuto competente per rispondere alle esigenze meccaniche funzionali, in relazione alla nuova situazione biomeccanica intervenuta. Gli impianti clinicamente stabili e che istologicamente hanno raggiunto un’anchilosi funzionale lavorano come un’unica struttura con l’osso circostante.
Questo insieme, che comprende l’inserto alloplastico e il tessuto di sostegno osseo, perfettamente adattato e rimodellato attorno alle superfici del biomateriale, può essere considerato come un unico sistema biomeccanico, definito unità osso-impianto (Bianchi et al. 1994a, 1994b, 1994c, 1994d, 1994e).
Sebbene quindi il problema della biocompatibilità degli impianti in titanio sia legato alle caratteristiche di superficie di questo materiale (Leventhal 1951; Berg e Emnéus 1967; Hench 1980; Osborn e Newsley 1980; McQueen et al. 1982), la compatibilità in termini di stabilità secondaria duratura nel tempo in condizioni di carico è prerogativa della formazione della suddetta unità osso-impianto.
Il processo, una volta che si è completato, diventa difficilmente alterabile in virtù della capacità del sistema di apportare modificazioni parcellari. Il sistema, definito unità osso-impianto, da un punto di vista biomeccanico rappresenta un meccanismo di trasferimento dei carichi funzionali al resto delle strutture mascellari; a differenza dei denti naturali, la mancanza del legamento parodontale fa sì che la trasmissione delle sollecitazioni occlusali si realizzi senza alcun meccanismo di ammortizzamento, direttamente al segmento osseo (Bianchi et al. 1994a, 1994b, 1994c, 1994d, 1994e). Questo sistema biomeccanico, che può apparentemente risultare deficitario, qualora l’impianto e il tessuto di sostegno siano considerati come due sistemi meccanici separati, con l’impianto che fa da tramite di dissipazione dei carichi tra la protesi e l’osso, diviene invece un punto di forza, se si considera che l’impianto e il tessuto osseo circostante funzionano come un unico sistema operativo, che opera in un solo tempo il trasferimento delle sollecitazioni occlusali al resto delle architetture mascellari.
In questo modo, l’assoluta rigidità dell’unità osso-impianto prevede come sistema di ammortizzamento e dissipazione del carico l’intera struttura di sostegno mascellare, ampliando l’originario concetto di osteointegrazione che, per quanto corretto, trova alcuni limiti in una visione condizionata ai soli rapporti interfacciali. L’unita osso-impianto rappresenta quindi l’espressione dell’applicazione di corrette basi biologiche, chirurgiche e funzionali, in associazione all’utilizzo di presidi alloplastici dotati di caratteristiche di bioinerzia superficiale (Bianchi et al. 1999).
Il successo clinico in una riabilitazione implanto-protesica si viene quindi a determinare indipendentemente dalla macromorfologia (forma) e micromorfologia (superfice) dell’impianto, bensì in base all’applicazione di un corretto protocollo sia al momento dell’incorporazione del morfotipo alloplastico sia negli step successivi, che determinano nella funzionalizzazione lo svolgersi di eventi biologici specifici; tutto ciò permette il raggiungimento e il mantenimento della condizione di unità osso-impianto, rappresentata da una stabile anchilosi funzionale, che si esprime istologicamente con analogie di carattere morfostrutturale.
Tutto questo è clinicamente raggiungibile mediante protocolli chirurgici che prevedano sterilità e raggiungimento di una stabilità primaria dell’impianto, che quindi verrà lasciato quiescente nei tempi previsti dalle scuole di osteointegrazione; diversa è la fase di funzionalizzazione, che non può invece essere standardizzata, ma deve seguire regole consone per ottenere una risposta biologica corretta all’erogazione del carico protesico.
L’utilizzo di tecniche implanto-protesiche a oggi disponibili come gli impianti short o ultra short (6 o 4 mm) non deve rappresentare quindi una visione dottrinaria dell’implantologia, ma un indirizzo in primo luogo determinato dalla versatilità del protocollo, adottato anche in relazione alla curva di apprendimento dell’operatore non solo in termini di protocollo chirurgico ma anche e soprattutto riguardo la conoscenza degli aspetti biologici che sono in grado di regolare una risposta adattiva del substrato osseo.
Nello specifico, l’osso perimplantare, superata la fase postchirurgica immediata attraverso eventi di tipo solo riparativo, rimane per il periodo definito di guarigione in silenzio funzionale, fino all’applicazione della sovrastruttura protesica.
Da questo momento l’inserto alloplastico, trasferendo al substrato un carico, determina una modificazione morfostrutturale dell’osso perimplantare (Brunski 1991).
La capacità di rimodellamento è intrinseca al tessuto osseo (Currey 1984a, 1984b ), mentre è ad appannaggio del protesista la possibilità di influenzare l’organizzazione in senso appositivo e non demolitivo (Hoshaw 1992). Ciò deve avvenire attraverso una funzionalizzazione controllata, alla ricerca di una situazione biomeccanica di equilibrio (Misch 1990).
Il tessuto osseo, distante dal momento della noxa chirurgica, ha esaurito, infatti, gran parte della spinta rigenerativa propria degli eventi riparativi e ristabilito un turnover metabolico rallentato dalla condizione di quiescenza per l’assenza di carico (Spector 1988) L’innesco di nuove attività cellulari di adattamento, in grado di modificare l’architettura dell’osso più prossimo alla superficie del biomateriale, necessita di un certo intervallo e di una richiesta graduale di lavoro.
La funzionalizzazione deve avvenire priva di condizioni di carico assiale eccessivo o di momenti flettenti che generano sovraccarico. Per evitare microfratture e riassorbimento dell’osso attorno alla porzione più crestale dell’impianto, è opportuno modulare questa richiesta approntando i provvisori in leggera sottocclusione e completamente svincolati da funzioni di guida. Si promuove così soltanto l’azione ritmica degli stimoli funzionali, generati durante la masticazione, per l’interposizione del bolo che ristabilisce il contatto tra le arcate antagoniste.
La conferma è che la maggior percentuale di insuccessi di impianti osteointegrati si realizza soprattutto nel primo periodo di funzionalizzazione (Albrektsson e Sennerby 1991). Tutto ciò lascia ipotizzare che in questi casi l’osso riparato, in condizioni di quiescenza attorno agli impianti, non è in grado, da un punto di vista biomeccanico, di sopportare il carico che deriva dalla protesizzazione degli stessi, oppure che il rimodellamento adattativo non è stato adeguatamente efficace da fornire una sufficiente massa e organizzazione ossea locale alle nuove condizioni di sollecitazione meccanica. La funzionalizzazione ritardata dell’impianto implica la trasformazione dello stato d’integrazione tessutale, dettato dalla riparazione postchirurgica in quiescenza, a quello di anchilosi funzionale con riorganizzazione traiettoriale dell’osso perimplantare.
Tipologie ossee D2 o D3 hanno capacità di adattamento più rapido di un osso D1 e più prevedibili di un osso D4.
In condizioni favorevoli il carico progressivo esaurisce la sua azione nell’arco di 3-6 mesi; un substrato particolarmente spongioso, come per esempio l’osso di tipo D1, può richiedere tempi prolungati fino a 12 mesi. Inoltre, altri parametri estrinseci al tessuto osseo, come il rapporto tra la resistenza dell’ancoraggio e lo sviluppo del braccio di leva delle corone, e le caratteristiche dell’arcata antagonista e dell’occlusione devono essere presi in debita considerazione nell’attuazione del programma di posizionamento degli impianti e di funzionalizzazione.
Ciò premesso, nello studio del piano di trattamento dei pazienti con gravi atrofie ossee, per quanto riguarda la risoluzione riabilitativa con impianti short e ultra short è necessario affidarsi a una metodologia clinica molto più rigida rispetto a quella adottata per gli impianti standard.
Il protocollo chirurgico deve essere definito attraverso lo studio quantitativo e qualitativo dell’osso residuo, sia con metodi di acquisizione con CBCT sia mediante programmi specifici che permettono di studiare il posizionamento degli impianti con asse di inserzione parallelo, in modo da semplificare la successiva fase protesica provvisoria e definitiva.
Riteniamo quindi opportuno declinare con estrema semplicità le fasi di raccordo tra i presupposti biologici prima enunciati e il protocollo clinico operativo che si vuole attuare.
Protocollo clinico-operativo
Presupposti clinici
È stata condotta una ricerca clinica retrospettiva su impianti osteointegrati Global D TwinKon. La scelta della tipologia implantare è stata dettata dalla macromorfologia dell’impianto che ha caratteristiche strutturali idonee per supportare carichi occlusali esasperati dalle corone protesiche, di norma più estese nella porzione apico-coronale. Inoltre, questa morfologia implantare prevede la bagnabilità della superfice con due cicli di mordenzatura SA2 acidificata, che favorisce la deposizione osteoblastica e garantisce uno standard di decontaminazione assoluto.
La micromorfologia rugosa si interrompe prima di un collo platform-switching lucido e dotato di poligono in testa, che permette di eseguire sia corone singole su monconi o avvitate sia di accettare pilastri MUA per protesi fisse di più elementi. Tale collo lucido permette una guarigione già transmucosa che annulla il cono di riassorbimento perimplantare, che, se pur fisiologico, condurrebbe alla riduzione della superfice di osteointegrazione con un rimodellamento adattivo in senso apicale.
La ricerca clinica, di cui riportiamo in questo aggiornamento solo alcuni esempi significativi, è stata realizzata grazie al supporto annuale all’Attività Scientifica dell’Istituto da parte dell’azienda.
Una volta chiarita la natura dello studio, vengono descritte di seguito alcune fasi cliniche, coadiuvate dall’implementazione delle tecnologie digitali, che, come vedremo, risultano fondamentali per questo tipo di protocollo.
L’accoppiamento dei file STL e DICOM: perché è così importante?
Quando si pianifica un intervento implantare, un passaggio fondamentale è l’accoppiamento – o fusione – dei file STL provenienti da scansioni intraorali o da modelli e dei file DICOM ottenuti da CBCT.
Questo processo permette di unire due insiemi di dati in un unico sistema di riferimento spaziale, così da poter lavorare in modo protesicamente guidato e con la massima precisione.
Il principio è sempre lo stesso, sia che si tratti di un paziente con edentulia parziale sia che si parli di un edentulo totale.
Ciò che cambia è la metodologia, perché nei primi casi i denti residui forniscono punti di riferimento naturali, mentre negli edentuli totali bisogna ricorrere a strategie alternative.
Caso 1: il paziente con edentulia parziale
Qui l’obiettivo è semplice: allineare la CBCT con la scansione intraorale, così da avere una base sicura per la pianificazione chirurgica e protesica. Come si procede?
Prima si raccolgono i dati: la CBCT del mascellare o della mandibola, dove siano ben visibili denti e strutture dure, e la scansione intraorale in formato STL, che restituisce con precisione denti e tessuti molli.
Entrambi i file vengono caricati nel software di pianificazione (tra i più usati: BlueSkyPlan, coDiagnostiX, Exoplan, 3Shape Implant Studio).
A questo punto si ricostruisce il volume 3D dai DICOM e si importano gli STL.
Arriva quindi il momento dell’allineamento: il software esegue un “best-fit alignment” sfruttando punti anatomici comuni, come cuspidi, creste alveolari o restauri dentali. Spesso viene utilizzato un algoritmo di riconoscimento delle superfici (ICP-Iterative Closest Point), che però può essere affinato manualmente.
Infine, si verifica la correttezza della fusione, controllando che margini gengivali, cuspidi e scanalature combacino perfettamente.
Caso 2: il paziente completamente edentulo
In questo caso la situazione è più complessa, perché mancano i denti, cioè i punti di repere più affidabili per l’allineamento. Per questo motivo si ricorre a protocolli specifici, con tre principali approcci.
1. Dual Scan Protocol con markers radiopachi:
- la protesi totale viene preparata inserendo 3/6 markers radiopachi in posizioni asimmetriche (meglio se in composito radiopaco, più pulito rispetto alla guttaperca);
- si esegue una prima CBCT con la protesi in bocca e una seconda della sola protesi;
- il software utilizza i markers per sovrapporre i due dataset, consentendo in seguito anche l’allineamento con la scansione STL della protesi.
È il metodo più preciso ed è considerato il gold standard.
2. Allineamento basato su tessuti molli o cresta edentula:
- si esegue una CBCT del paziente senza protesi (o con un bite trasparente);
- si scansiona la cresta edentula in STL;
- l’allineamento avviene manualmente, utilizzando punti come la tuberosità o il palato.
È un metodo meno accurato rispetto al protocollo con markers.
3. Protesi come guida radiologica:
- si realizza una copia della protesi in resina trasparente, con markers radiopachi, che funge da guida radiologica;
- il paziente esegue la CBCT con la guida in situ;
- la guida viene poi scansionata in STL e il software utilizza i markers per allinearla alla CBCT.
Suggerimenti derivanti dalla nostra pratica clinica
- Negli edentuli totali, quando possibile, è sempre meglio adottare il Dual Scan Protocol.
- La CBCT dovrebbe essere impostata a bassa dose, ma con alta risoluzione (voxel inferiori a 200 μm), in modo da migliorare la precisione dell’allineamento.
- Alcuni software (come Blu Sky Plan e coDiagnostiX) offrono algoritmi più evoluti che semplificano e velocizzano il processo di matching delle immagini acquisite con 3Shape.
Una checklist utile
Per non tralasciare passaggi importanti, è utile avere una lista operativa a portata di mano.
Paziente edentulo parziale: fusione CBCT + STL intraorale.
Paziente completamente edentulo:
- opzione A: Dual Scan Protocol (consigliata).
- opzione B: matching su tessuti molli/cresta edentula.
- opzione C: guida radiologica.
Verifica finale: controllare sempre la corrispondenza delle superfici e correggere eventuali disallineamenti.
Gestione dei casi con molti restauri metallici
La presenza di corone, ponti o amalgama può creare artefatti che peggiorano la qualità della CBCT e complicano l’allineamento. Ecco alcuni accorgimenti:
- ottimizzare le impostazioni tecniche della CBCT per ridurre gli artefatti da metallo;
- aumentare milliamperaggio;
- rimuovere tutti gli oggetti mobili (protesi, bite, piercing, ponti provvisori);
- utilizzare morsi in silicone trasparente per stabilizzare le arcate durante la scansione;
- assicurarsi che il paziente sia ben centrato e immobile;
- valutare l’uso dell’algoritmo MAR (Metal Artifact Reduction) utile per la fusione STL–DICOM, ma da disattivare temporaneamente se si effettuano misurazioni densitometriche, per evitare alterazioni nella valutazione dell’osso.
In questo modo, l’intero processo di fusione tra STL e DICOM diventa non solo più chiaro, ma anche più sistematico e replicabile nella pratica clinica quotidiana.
Protocollo protesico per il carico dilazionato
Durante la fase di riparazione della ferita chirurgica, l’assenza di movimenti relativi dell’impianto – definita stabilità primaria – deve essere ottenuta con modalità diverse di ancoraggio; quindi, negli impianti short e ultra short, sono maggiormente indicate metodiche chirurgiche implantari che prevedono frese per l’alesaggio del sito ricettore degli impianti non solo del diametro del nocciolo implantare, ma anche sovra e sotto dimensionate.
Terminata la fase di riparazione, detta clinicamente periodo di guarigione, l’osteointegrazione in condizione di carico protesico, definita anche stabilità secondaria, è mantenuta dal substrato osseo nel primo periodo a condizione che l’intensità, la direzione e il verso delle sollecitazioni occlusali che gravano sull’impianto e che vengono propagate all’osso siano tali da stimolare il tessuto osseo in senso appositivo, senza provocare tensioni e deformazioni all’interfaccia in grado di indurre un adattamento in senso demolitivo.
Il successo clinico in una riabilitazione implanto-protesica, a maggior ragione se realizzata con impianti short e ultra short, si viene a determinare indipendentemente dalla macromorfologia dell’impianto, bensì in base all’applicazione di un corretto protocollo di carico.
Nell’utilizzo di impianti short e ultra short il protesista non deve essere ancorato a una visione ordinaria dell’implantologia, ma tenere conto degli aspetti biologici e conseguire l’adattamento osseo, di norma nei dodici mesi successivi al carico protesico, con protocolli di carico dilazionato implantare dalla sottocclusione alla morfologia protesica definitiva.
Tale condizionamento graduale del substrato, definito da Misch (1990) progressive bone loading attuato mediante la protesi provvisoria, consente una maggiore prevedibilità dell’adattamento funzionale del tessuto osseo verso la condizione di resistenza al carico. La funzionalizzazione deve quindi avvenire attraverso la modificazione graduale della morfologia delle corone protesiche provvisorie (Balshi 1990).
La funzionalizzazione deve avvenire inizialmente priva di carico assiale eccessivo o di momenti flettenti che generano sovraccarico. Il manufatto è inizialmente allestito con una superficie occlusale ridotta e in modica sottocclusione nei posteriori e svincolato da compiti funzionali di guida negli anteriori.
Si promuove così l’azione ritmica degli stimoli funzionali generati dalla masticazione per l’interposizione del bolo che ristabilisce il contatto tra le arcate.
Questo assume nel tempo, attraverso successive modifiche, le caratteristiche adatte all’ambito protesico in cui è inserito; i tempi e le modalità di funzionalizzazione, cioè gli intervalli e l’entità delle modifiche morfologiche tra un manufatto protesico provvisorio e uno successivo, dovranno essere considerati in funzione della qualità osseo.
Casi clinici
Di seguito vengono riportati due casi clinici emblematici, affrontati presso il Reparto di Parodontologia e Implantologia dell’Istituto Stomatologico Italiano, ove la progettazione digitale degli short implant si è rivelata indispensabile sia per minimizzare la morbilità del paziente sia per ottenere il successo clinico testimoniato dai follow-up. Nel primo caso viene trattata una paziente caucasica, 57 anni, che presenta i canini superiori inclusi; in seguito alla estrazione dell’elemento 6.3, si è resa necessaria la riabilitazione implanto-protesica del 2.3 (Figura 1).
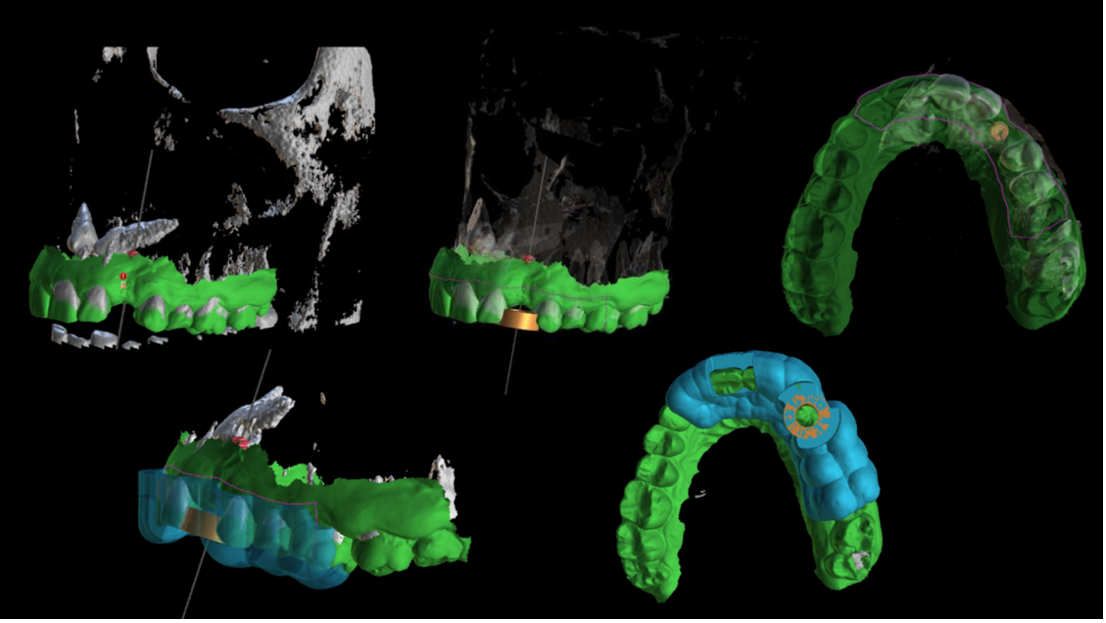
Tuttavia, la paziente rifiutava l’estrazione del 2.3 incluso e pertanto è stato proposto un protocollo con short implant (Figure 2-3).

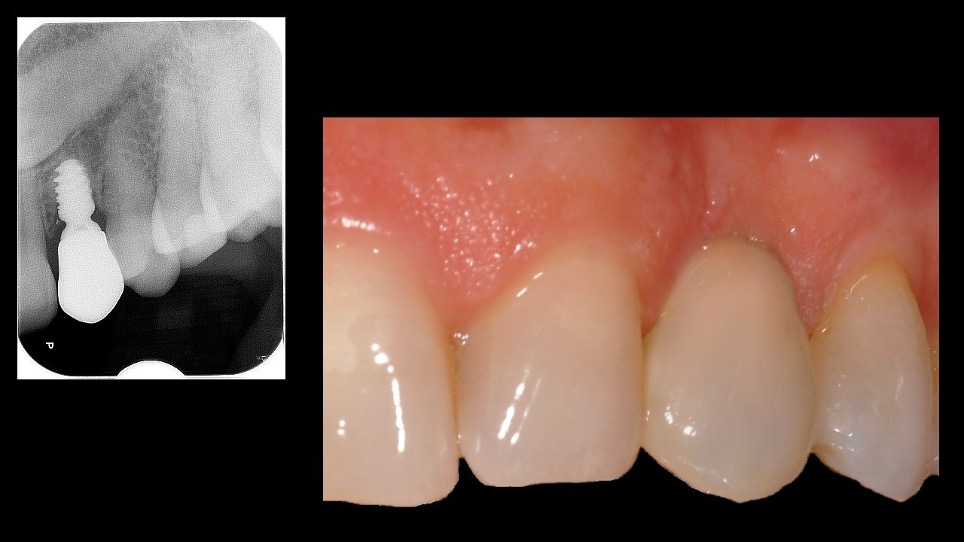
Nel secondo caso, invece, viene affrontata una situazione clinica complessa (Figura 4).
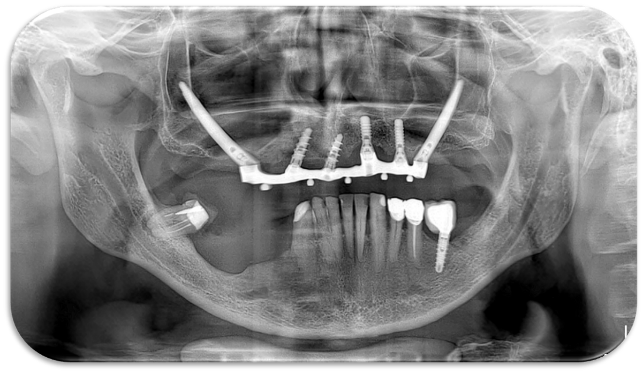
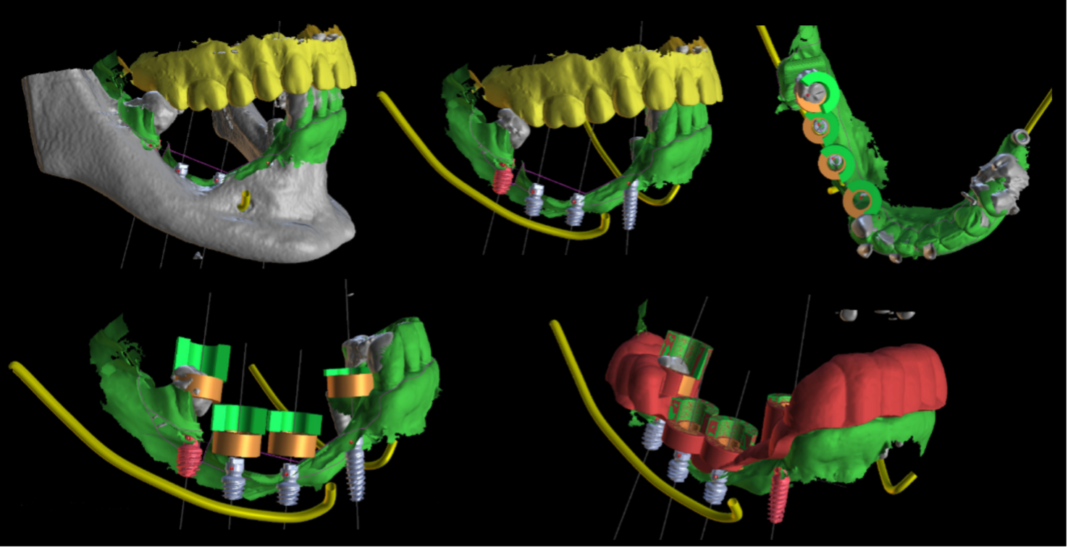
Il paziente, maschio, 63 anni, di etnia caucasica, è stato riabilitato dapprima con impianti tradizionali e impianti zigomatici; successivamente, viene programmato un intervento di implantologia guidata (Figura 5) per gestire la grave atrofia del settore 4 (Figure 6-7).
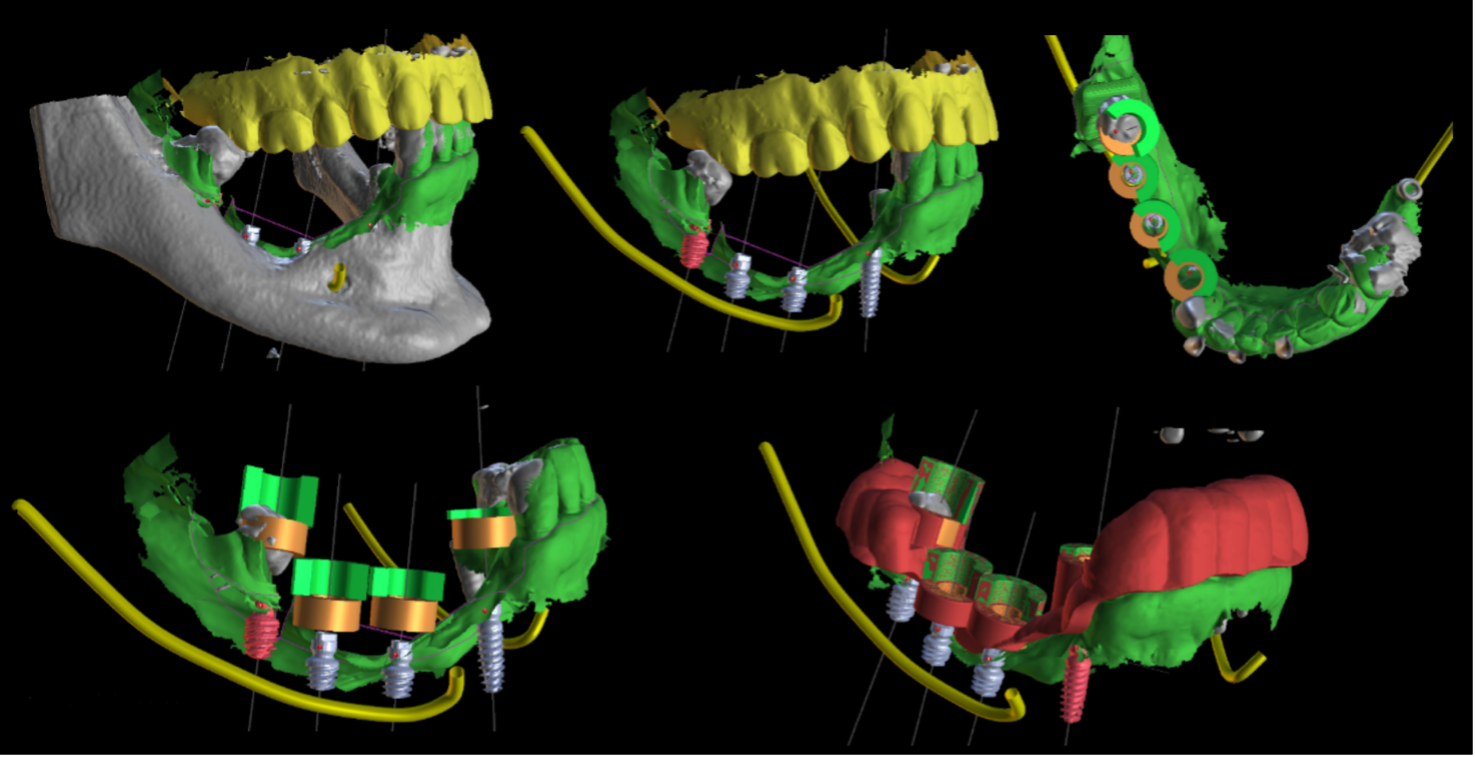
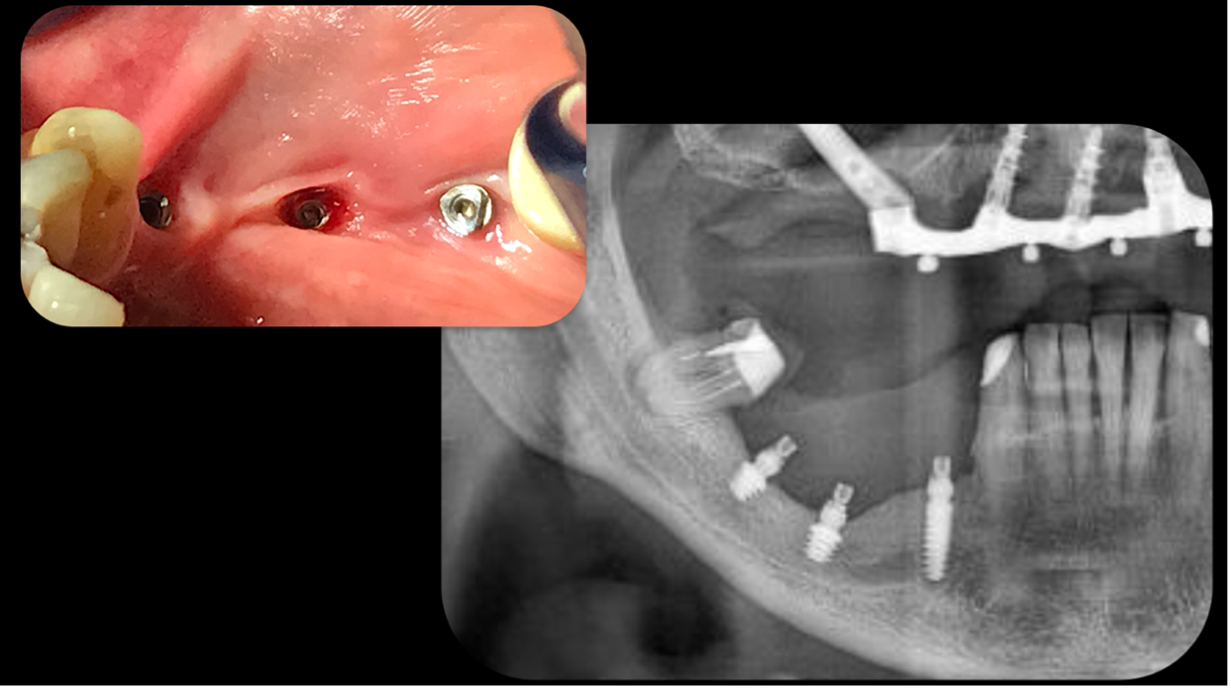
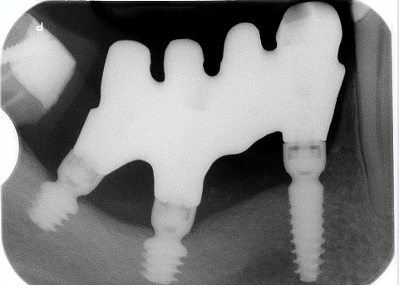
La metodica con impianti Global D descritta in entrambi i casi ha permesso di disporre di una trousse implantare con frese in grado di realizzare una sottopreparazione o una sovrapreparazione del sito di incorporazione implantare in base alla densità ossea da affrontare nel mascellare e nella mandibola (Figura 8).

Conclusioni
Alla luce di quanto descritto, sia da un punto di vista biologico che clinico-pratico, è possibile comprendere meglio quanto sia vantaggiosa, in termini di morbilità e di minore invasività, la gestione della riabilitazione implanto-protesica con impianti short e ultra short.
In base alle più recenti evidenze scientifiche è inoltre ormai chiaro, laddove vi siano le corrette indicazioni, come lavorare sul solo osso nativo del paziente, e non su un substrato osseo rigenerato, non solo rappresenti un presupposto fondamentale per la predicibilità clinica del risultato, ma sia fondamentale per ridurre considerevolmente le complicanze postoperatorie e i fallimenti.
La condizione necessaria affinché si possa portare a termine un protocollo come quello descritto è, tuttavia, la scelta di un carico differito, che nel caso del mascellare superiore può comportare fino a 12 mesi di attesa.
La tecnologia, infine, permette di coniugare le conoscenze biologiche e le esperienze cliniche per favorire, anche tra gli operatori più esperti, un migliore flusso di lavoro, a tutto vantaggio della sicurezza, della qualità e della comunicazione medico-paziente.
- Adell R, Lekholm U, Rockler B, Brånemark PI. A 15-year study of osseointegrated implants in the treatment of edentulous jaws. Int J Oral Surg. 1981;10(6):387-416.
- Albrektsson T, Brånemark PI, Hansson HA, Ivarsson B, Jönsson U. Ultrastructural analysis of the interface zone of titanium and gold implants. Adv Biomater. 1982;4:167-177.
- Albrektsson T, Hansson HA. An ultrastructural characterization of the interface between bone and sputtered titanium or stainless steel surfaces. Biomaterials. 1986;7(3):201-205.
- Albrektsson T, Jacobsson M. Bone-metal interface in osseointegration. J Prosthet Dent. 1987;57(5):597-607.
- Albrektsson T, Sennerby L. State of the art in oral implants. J Clin Periodontol. 1991;18(6):474-481.
- Albrektsson T. Direct bone anchorage of dental implants. J Prosthet Dent. 1983;50(2):255-261.
- Balshi TJ. Overload management of osseointegrated fixtures to achieve optimum bone remodelling through multistage prosthodontic loading. In: Loney WR, Tolman DE, eds. Tissue Integration in Oral, Orthopaedic and Maxillofacial Reconstruction. Chicago, IL: Quintessence Publishing; 1990:364-371.
- Berg S, Emneus H. Some Aspects on Titanium as an Implant Material. Avesta, Sweden: Avesta Jernverk AB; 1967.
- Bianchi A, Gallini G, Fassina R, Sanfilippo F. Analisi al SEM dell’interfaccia osso-impianto di una vite sottoposta a carico funzionale immediato. Dentista Moderno. 1994;9:1499-1503.
- Bianchi A, Fassina R, Sanfilippo F. Istomorfologia del tessuto osseo perimplantare: osservazioni in microscopia ottica a luce ordinaria e polarizzata. Dentista Moderno. 1994;10.
- Dolci G, Favero GA, eds. I World Congress of Osseointegration: Proceedings. Venice, September 29–October 2, 1994. Ronchi dei Legionari, Italy: Ergon; 1994:395-399.
- Bianchi A, Fassina R, Sanfilippo F. Distribuzione delle sollecitazioni da impianti al substrato osseo: analisi comparativa tra modelli fotoelastici e risultati istologici al MO e al SEM. In: Dolci G, Favero GA, eds. World Congress of Osseointegration: Proceedings. Venice, September 29–October 2, 1994. Ronchi dei Legionari, Italy: Ergon; 1994:401-404.
- Bianchi A, Gallini G, Fassina R, Sanfilippo F. Risposta ossea a impianti a vite autofilettante. Dentista Moderno. 1994;8:1313-1320.
- Bianchi A. Recenti acquisizioni sul rimodellamento osseo con impianti bioinerti a finalità di funzionalizzazione biomeccanica [thesis]. Milano, Italy: Università degli Studi di Milano; 1994.
- Bianchi AE. Implantologia e Implantoprotesi. Basi biologiche, biomeccanica, applicazioni cliniche. Torino, Italy: UTET; 1999.
- Brånemark PI, Hansson B, Adell R, Breine U, Lindström J, Hallen O, Öhman A. Osseointegrated implants in the treatment of the edentulous jaw. Experience from a 10-year period. Scand J Plast Reconstr Surg Hand Surg. 1977;16(suppl):1-132.
- Brunski JB. Influence of biomechanical factors at the bone-biomaterial interface. In: Davies JE, ed. The Bone-Biomaterial Interface. Toronto, Canada: University of Toronto Press; 1991:391-404.
- Chamay A, Tschanz P. Mechanical influences in bone remodelling: experimental research on Wolff’s law. J Biomech. 1972;5(2):173-180.
- Churches AE, Howlett CR. The response of mature cortical bone to controlled time varying loading. In: Cowin SC, ed. Mechanical Properties of Bone. New York, NY: American Society of Mechanical Engineers; 1981:81-92.
- Currey JD. The Mechanical Adaptations of Bones. Princeton, NJ: Princeton University Press; 1984.
- Currey JD. Can strains give adequate information for adaptive bone remodelling? Calcif Tissue Int. 1984;36(suppl 1):118-122.
- Esposito M, Buti J, Barausse C, Gasparro R, Sammartino G, Felice P. Short implants versus longer implants in vertically augmented atrophic mandibles: a systematic review of randomized controlled trials with a 5-year post-loading follow-up. Int J Oral Implantol (Berl). 2019;12(3):267-280.
- Esposito M, Grusovin MG, Felice P, Karatzopoulos G, Worthington HV, Coulthard P. Interventions for replacing missing teeth: horizontal and vertical bone augmentation techniques for dental implant treatment. Cochrane Database Syst Rev. 2009;(4):CD003607.
- Furlong RI, Osborn JF. Fixation of hip prostheses by hydroxyapatite ceramic coatings. J Bone Joint Surg Br. 1991;73(5):741-745.
- Goodship AE, Lanyon LE, McFie JH. Functional adaptation of bone to increased stress: an experimental study. J Bone Joint Surg Am. 1979;61(4):539-546.
- Hench LL. The interfacial behaviour of biomaterials. J Biomed Mater Res. 1980;14(5):803-811.
- Hoshaw S. Investigation of Bone Modeling and Remodelling at a Loaded Bone-Implant Interface [thesis]. Troy, NY: Rensselaer Polytechnic Institute; 1992.
- Lanyon LE, Goodship AE, Pye CJ, McFie JH. Mechanically adaptive bone remodelling. J Biomech. 1982;15(3):141-154.
- Leventhal GS. Titanium, a metal for surgery. J Bone Joint Surg Am. 1951;33(2):473-479.
- Lozupone E, Favia A. Density of trabecular framework and osteogenetic activity in the spongiosa of long bones subjected to drastic changes in mechanical loading in the dog. Anat Anz. 1982;152(3):245-261.
- McQueen D, Sundgren JE, Ivarsson B, Lundström I, Ekenstam B, Svensson A, Brånemark PI, Albrektsson T. Auger electron spectroscopic studies of titanium implants. In: Lee AJC, Albrektsson T, Brånemark PI, eds. Second European Conference on Biomaterials: Clinical Applications of Biomaterials. New York, NY: John Wiley & Sons; 1982.
- Mendes PA, Silva VEA, Viegas da Costa D, Morais de Pinho M, Chambrone L, Zenóbio EG. Effectiveness of extra-short (<6 mm) implants compared to standard-length implants associated with bone graft: systematic review. Int J Oral Maxillofac Implants. 2023;38(1):29-36.
- Misch CE. Density of bone: effect on treatment plans, surgical approach, healing and progressive bone loading. Int J Oral Implantol. 1990;6(2):23-31.
- Osborn JF, Newesley H. Dynamic aspects of the implant-bone interface. In: Heimke G, ed. Dental Implants: Materials and Systems. München, Germany: Hanser Verlag; 1980:111-123.
- Rubin CT, Lanyon LE. Regulation of bone formation by applied dynamic loads. J Bone Joint Surg Am. 1984;66(3):397-402.
- Rubin CT. The benefits and consequences of structural adaptation in bone. In: Fitzgerald RH Jr, ed. Non-Cemented Total Hip Arthroplasty. New York, NY: Raven Press; 1988:41-48.
- Sennerby L. On the Bone Tissue Response to Titanium Implants [thesis]. Gothenburg, Sweden: University of Gothenburg; 1991.
- Spector M, Harmon SL, Kieheutner A. Characteristics of tissue growth into Proplast and porous polyethylene implants in bone. J Biomed Mater Res. 1979;13(5):677-692.
- Wolff J. Über die innere Architektur der Knochen und ihre Bedeutung für die Frage vom Knochenwachstum. Virchows Arch Pathol Anat Physiol Klin Med. 1870;50:389-450.