Gli idrogel sono materiali polimerici organizzati in reti tridimensionali capaci di inglobare e trattenere grandi quantità di acqua senza dissolversi. Questa elevata idratazione conferisce loro una consistenza morbida ed elastica, molto simile a quella dei tessuti biologici, rendendoli particolarmente adatti all’interazione con i tessuti orali.
Dal punto di vista strutturale, un idrogel ad uso odontoiatrico è generalmente costituito da tre elementi fondamentali.
- Matrice polimerica: rappresenta lo “scheletro” del materiale e può essere costituita da polimeri naturali (come acido ialuronico, chitosano, collagene o fibrina), polimeri sintetici (ad esempio derivati del polietilenglicole) oppure da una combinazione di entrambi. I polimeri naturali garantiscono elevata biocompatibilità e buona interazione cellulare, ma sono meno stabili. I polimeri sintetici, invece, permettono di modulare con precisione le proprietà meccaniche (tunable rheology), offrendo maggiore resistenza strutturale e migliore capacità di incorporare principi attivi, risultando quindi più versatili dal punto di vista clinico. I materiali ibridi combinano i vantaggi di entrambe le categorie.
- Sistema di reticolazione: di tipo chimico o fisico, collega tra loro le catene polimeriche formando la rete tridimensionale. Il grado di reticolazione, o cross-linking, è un parametro chiave poiché influenza direttamente la stabilità del materiale, la sua resistenza meccanica e la velocità di degradazione. In pratica, un idrogel molto reticolato è più stabile, resistente e a lenta degradazione, utile quando si desidera un rilascio prolungato di principi attivi (ad esempio nel trattamento delle tasche parodontali). Al contrario, un idrogel poco reticolato è più morbido, si degrada più rapidamente ed è preferibile come supporto temporaneo alla rigenerazione tissutale o quando è richiesto un rilascio più rapido, come nelle procedure di endodonzia rigenerativa.
- Componenti funzionali: conferiscono all’idrogel la sua specifica funzione clinica. Possono includere farmaci antimicrobici o antinfiammatori, fattori di crescita, peptidi bioattivi o, in ambito sperimentale, cellule staminali.
In termini pratici, ciò significa che un idrogel può essere progettato come semplice veicolo farmacologico a rilascio controllato oppure come vero e proprio scaffold biologico, capace di guidare e sostenere i processi rigenerativi.
Perché gli idrogel sono rilevanti in odontoiatria
L’interesse odontoiatrico verso gli idrogel è cresciuto rapidamente negli ultimi anni per tre motivi principali.
- Biocompatibilità: sono ben tollerati dai tessuti orali; la loro natura idrofila riduce la risposta infiammatoria e favorisce adesione e vitalità cellulare.
- Rilascio controllato di farmaci: la rete polimerica permette di incorporare farmaci, fattori di crescita o altri principi attivi e di rilasciarli localmente in modo graduale, aumentando l’efficacia terapeutica e riducendo gli effetti collaterali sistemici.
- Supporto alla rigenerazione tissutale: possono fungere da scaffold biologici, ospitando cellule staminali e guidando la formazione di nuovo tessuto pulpare, osseo e parodontale.
Nel loro insieme, queste proprietà pongono le basi per approcci innovativi nella gestione di carie, patologie parodontali, endodonzia rigenerativa e rigenerazione ossea, promettendo interventi sempre più mirati e biologicamente guidati.
Applicazioni cliniche: dove gli idrogel fanno davvero la differenza
Rilascio di farmaci nelle tasche parodontali
Gli idrogel mucoadesivi consentono di prolungare la permanenza dei farmaci all’interno delle tasche parodontali, migliorando l’efficacia di antimicrobici o antinfiammatori. In particolare, i sistemi termoreversibili (liquidi a temperatura ambiente e gelificanti alla temperatura corporea) permettono una somministrazione minimamente invasiva.
Un esempio clinico consolidato è rappresentato dai gel a base di doxiciclina applicati direttamente nella tasca dopo levigatura radicolare, in grado di garantire un rilascio prolungato del farmaco e di degradarsi spontaneamente senza necessità di rimozione.
Endodonzia rigenerativa: oltre l’otturazione canalare
All’interno dei canali radicolari, gli idrogel possono fungere da impalcatura tridimensionale per cellule staminali e fattori di crescita. Studi preclinici dimostrano che idrogel specifici favoriscono l’infiltrazione cellulare, la formazione di tessuto vascolarizzato simile alla polpa e la deposizione di un layer di odontoblasti in apposizione alla dentina.
Questa strategia apre la strada a terapie biologiche alternative alla terapia endodontica convenzionale, soprattutto in presenza di apici immaturi, con potenziale recupero di vitalità e funzione del dente.
Rigenerazione ossea e parodontale
Idrogel combinati con peptidi bioattivi o matrici a base di acido ialuronico sono stati impiegati come supporto alla rigenerazione parodontale, stimolando la formazione di nuovo osso e legamento parodontale in difetti alveolari o peri-implantari. La possibilità di veicolare agenti antimicrobici consente inoltre un controllo locale dell’infiammazione e dell’infezione.
Implantologia e chirurgia orale
In ambito chirurgico, gli idrogel funzionalizzati possono essere usati per supportare la rigenerazione ossea post-estrattiva, ridurre la carica batterica nei siti chirurgici, rilasciare localmente analgesici e antinfiammatori.
Sebbene molti di questi approcci siano ancora in fase di sperimentazione clinica, i risultati preliminari indicano un potenziale concreto nella riduzione delle complicanze postoperatorie.
Guarigione dei tessuti molli
Gli idrogel mucoadesivi stimoloresponsivi o fotosensibili creano un microambiente protettivo e idratato che favorisce la riepitelizzazione, riduce l’infiammazione e accelera la guarigione dei tessuti molli.
I materiali stimolo-responsivi modulano il rilascio di farmaci in risposta a variazioni locali di pH o temperatura, mentre gli idrogel fotosensibili si attivano in risposta alla luce, ad esempio solidificandosi o rilasciando principi attivi solo quando esposti a specifiche lunghezza d’onda.
Studi preclinici suggeriscono che questi sistemi possano superare i limiti dei trattamenti tradizionali soggetti a rapido dilavamento nel cavo orale.
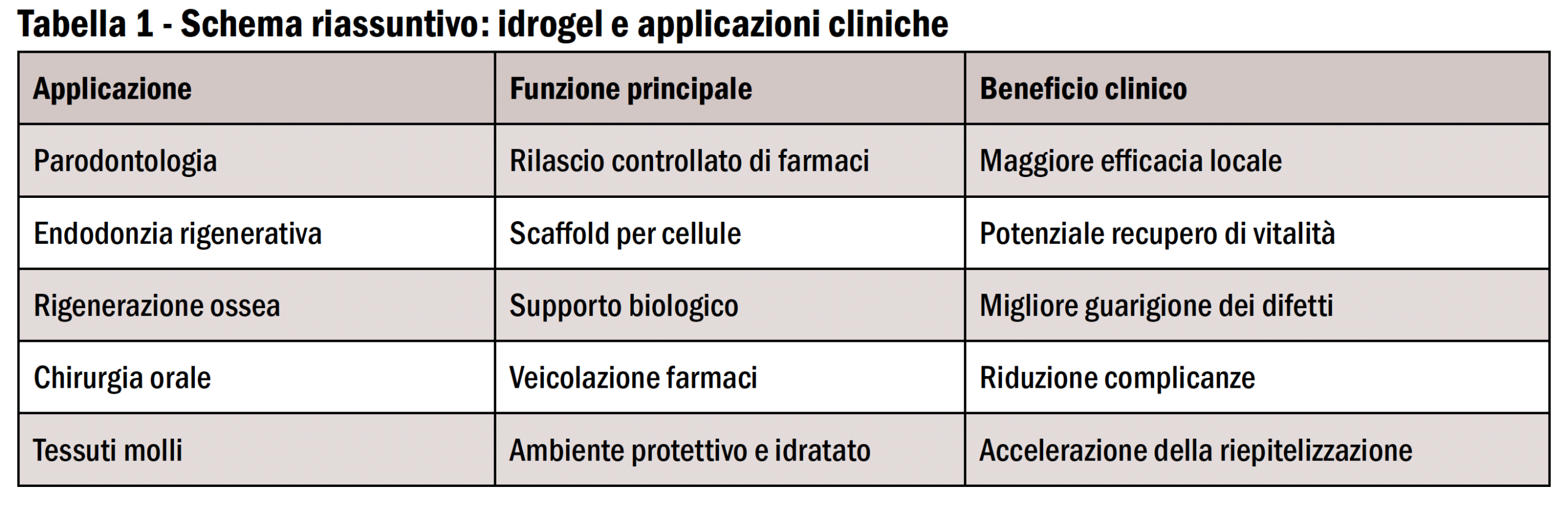
La Tabella 1 riporta le principali applicazioni cliniche degli idrogel
Sfide e limiti attuali
Nonostante i risultati molto promettenti, permangono alcune criticità, tra cui la variabilità della stabilità degli idrogel nell’ambiente orale dinamico, la limitata disponibilità di studi clinici controllati a lungo termine e i requisiti regolatori e produttivi, soprattutto per i sistemi caricati con cellule o fattori di crescita.
Prospettive future: verso un’odontoiatria biologicamente guidata
Le linee di ricerca più promettenti includono lo sviluppo di idrogel intelligenti sensibili a stimoli locali, l’impiego del bioprinting 3D per la realizzazione di scaffold personalizzati e la progettazione di idrogel multifunzionali in grado di combinare rigenerazione tissutale e controllo batterico in un’unica applicazione. Queste innovazioni potrebbero portare a soluzioni point of care sempre più personalizzate, integrando diagnosi e terapia in un’odontoiatria rigenerativa avanzata.
Conclusioni
Gli idrogel rappresentano una delle evoluzioni più interessanti dei biomateriali in odontoiatria. La loro capacità di interagire in modo biologicamente favorevole con i tessuti, di veicolare farmaci in maniera mirata e di supportare la rigenerazione tissutale li rende strumenti concreti per migliorare la pratica clinica quotidiana. Pur essendo necessari ulteriori studi clinici, le evidenze attuali indicano che gli idrogel non sono solo materiali del futuro, ma risorse sempre più rilevanti per un’odontoiatria moderna, minimamente invasiva e biologicamente orientata.
 In uno studio in vitro, gli autori hanno sviluppato un idrogel a base di fibrina contenente il peptide antimicrobico GH12, con l’obiettivo di supportare la rigenerazione della polpa dentale garantendo al contempo il controllo dell’infezione endodontica.
In uno studio in vitro, gli autori hanno sviluppato un idrogel a base di fibrina contenente il peptide antimicrobico GH12, con l’obiettivo di supportare la rigenerazione della polpa dentale garantendo al contempo il controllo dell’infezione endodontica.
Il materiale ha dimostrato buone caratteristiche di maneggevolezza, stabilità e adattabilità, risultando idoneo anche per l’impiego in anatomie endodontiche complesse. Dal punto di vista microbiologico, ha mostrato una significativa attività antibatterica, con concentrazione minima inibente (MIC) pari a 75 µg/mL per E. faecalis, 4.25 µg/mL per P. gingivalis e 28.15 µg/mL per S. gordonii.
La valutazione biologica ha evidenziato un’elevata biocompatibilità, con una vitalità superiore al 90% delle cellule staminali mesenchimali della polpa (DP-MSCs) incorporate nel gel dopo 48 ore, associata a un rilascio graduale e controllato del peptide GH12.
Questo idrogel combina quindi controllo dell’infezione, protezione cellulare e supporto rigenerativo, configurandosi come una strategia promettente per l’endodonzia rigenerativa. Tuttavia, saranno necessari studi clinici per confermarne l’efficacia e la sicurezza.
Un recente studio descrive un idrogel a base di carbossimetil-chitosano progettato per rilasciare simultaneamente doxiciclina (antibiotico) e atorvastatina (antinfiammatorio e rigenerativo) nel trattamento della malattia parodontale.
I risultati in vitro hanno dimostrato un rilascio sostenuto e controllato dei farmaci per oltre 72 ore, associato a una significativa attività antibatterica nei confronti di P. gingivalis, uno dei principali patogeni parodontali.
Dal punto di vista biologico, l’idrogel ha mostrato una elevata biocompatibilità, con una vitalità dei cheratinociti umani superiore al 97%.
Nel complesso, questo approccio dualdrug appare particolarmente promettente per la terapia parodontale localizzata, poiché combina controllo dell’infezione, modulazione dell’infiammazione e supporto alla rigenerazione tissutale.
Gli autori sottolineano tuttavia la necessità di studi in vivo e clinici per confermare l’efficacia osservata in laboratorio.
Uno studio clinico randomizzato ha valutato l’efficacia di un idrogel bioattivo funzionalizzato con peptide RGD (arginina–glicina–acido aspartico), noto per favorire l’adesione cellulare, in associazione a una tecnica chirurgica minimamente invasiva (MIST) nel trattamento di difetti intraossei parodontali (stadio III e IV).
Quarantacinque difetti sono stati suddivisi in tre gruppi (n° 15), rispettivamente trattati con MIST da sola, MIST + idrogel placebo e MIST + idrogel RGD.
Dopo 6 mesi, tutti i gruppi hanno mostrato miglioramenti clinici in termini di riduzione della profondità di tasca (PD), guadagno di attacco clinico (CAL) e riempimento del difetto osseo (DBF). Tuttavia, il gruppo trattato con idrogel RGD ha ottenuto risultati migliori, con un maggiore incremento del DBF e un guadagno di CAL statisticamente significativo rispetto agli altri gruppi.
Dal punto di vista biochimico, nei siti trattati con idrogel RGD sono stati riscontrati livelli più elevati di BMP2 (Bone Morphogenetic Protein-2), suggerendo una più efficace attivazione dei processi rigenerativi.
Nel complesso, questo studio fornisce evidenze cliniche concrete a supporto dell’utilizzo di idrogel bioattivi nella rigenerazione parodontale, confermando il valore aggiunto dell’integrazione tra biomateriali avanzati e chirurgia minimamente invasiva.
- Gli idrogel imitano le proprietà dei tessuti biologici e sono altamente biocompatibili;
- consentono il rilascio locale e controllato di farmaci, riducendo gli effetti sistemici;
- possono fungere da scaffold per la rigenerazione di polpa, osso e parodonto;
- rappresentano un ponte concreto tra ricerca biomedica e pratica clinica quotidiana.
- Ye S, Wei B, Zeng L. Advances on Hydrogels for Oral Science Research. Gels. 2022 May 15;8(5):302. doi: 10.3390/gels8050302.
- Chen A, et al. Hydrogels for Oral Tissue Engineering: Challenges and Opportunities. Molecules. 2023.
- Chen H et al. Adaptable Hydrogel with Strong Adhesion of Wet Tissue for Long-Term Protection of Periodontitis Wound. Adv Mater. 2025 Jan;37(1):e2413373. doi: 10.1002/adma.202413373. Epub 2024 Nov 20.
- Liu L, et al. Applications of Hydrogels in Drug Delivery for Oral and Maxillofacial Diseases. Gels. 2023. PMID: 36826316.
- Liu X, Huang X, Liu N, Zhu L, Zhao S, Tang S, Wang P. Advances in smart stimuli-responsive materials for oral wound healing. Front Chem. 2025 Dec 5;13:1725373. doi: 10.3389/fchem.2025.1725373. eCollection 2025.
- Sordi MB, Cruz A, Fredel MC, Magini R, Sharpe PT. Three-dimensional bioactive hydrogel-based scaffolds for bone regeneration in implant dentistry. Mater Sci Eng C Mater Biol Appl. 2021 May;124:112055. doi: 10.1016/j.msec.2021.112055. Epub 2021 Mar 24.
- Virvescu DI et al. Gel Delivery Systems in Dental Medicine: From Controlled Release to Regenerative Applications. Gels. 2025 Nov 19;11(11):925. doi: 10.3390/gels11110925.
- Ye S, Wei B, Zeng L. Advances on Hydrogels for Oral Science Research. Gels. 2022 May 15;8(5):302. doi: 10.3390/gels8050302.