Hector F. Rios
Department of Periodontics & Oral Medicine, School of Dentistry,
University of Michigan, Ann Arbor, MI, USA
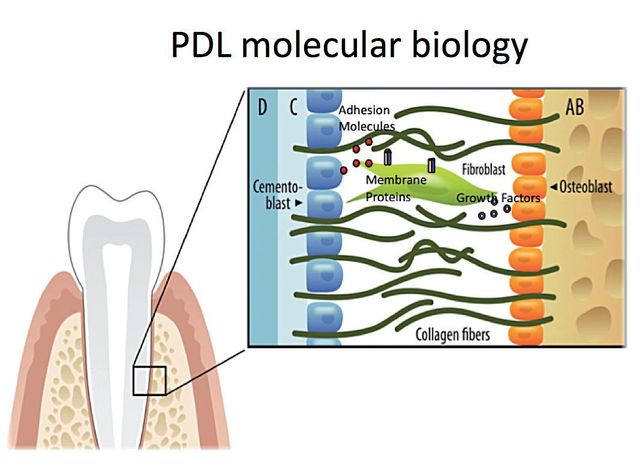
Le malattie parodontali sono un possibile fattore di rischio modificabile per la morbilità e mortalità in numerose malattie sistemiche1-4 con un evidente impatto sulla qualità della vita del paziente5,6. Complessivamente colpiscono più dell’80% della popolazione adulta in tutto il mondo e circa il 13% mostra gravi malattie concomitanti con la perdita precoce dei denti7. Nella parodontite i cambiamenti nocivi che avvengono sui tessuti di sostegno dei denti sono il risultato di specifici assalti microbici8-10. Queste situazioni in un ospite suscettibile alla malattia distruggono l’integrità funzionale e strutturale dell’apparato di supporto del dente11. È noto che la struttura e le proprietà dei tessuti parodontali sono strettamente legate alle cruciali interazioni tra cellule e matrice12-16. I meccanismi con cui questi microrganismi minacciano e compromettono la modulazione di tali eventi sinergici non sono del tutto noti. La regolazione corretta di queste interazioni in un ambiente meccanicamente dinamico, come il parodonto, determina la risposta adattiva dento-alveolare, coordinando la funzione di importanti proteine bioattive quali i fattori di crescita, citochine e proteasi (Figura 1)17-20. Le proteine che regolano queste interazioni sono complessivamente note come molecole matricellulari21-24. L’obiettivo di questo studio è di presentare e discutere le evidenze a riguardo della molecola matricellulare periostina nel contesto del parodonto.
Cos’è la periostina?
La periostina è una proteina dalla funzione relativamente poco conosciuta, che ha analogie con la fasciclina-I, una proteina del sistema nervoso centrale degli insetti, presente in modo significativo negli organismi superiori25. La proteina è omologa a βig-h3, una molecola indotta da TGF-β che promuove l’adesione e la diffusione dei fibroblasti. Quindi si crede che la periostina funzioni come una molecola di adesione durante la formazione dell’osso e possa supportare l’attacco e la diffusione di una linea di cellule osteoblastiche26. È stato dimostrato che la periostina purificata e ricombinata è un legante per le integrine αvβ3 e αvβ5, promuovendo l’adesione e la mobilità integrinodipendente27. Numerosi report hanno mostrato livelli elevati di periostina in neuroblastoma28, cancro ovarico epiteliale27 e carcinoma polmonare29 non a piccole cellule che ha subito una trasformazione mesenchimale epiteliale (EMT) e metastasi. Inoltre, è stato dimostrato che la periostina promuove notevolmente la sopravvivenza cellulare attraverso il percorso Akt/PKB30. È stata inoltre associata con il deposito della matrice extracellulare (ECM) successivo all’infarto miocardico ed è stato riportato che, a seguito di una tale patologia acuta, la proteina risulta essere essenziale per la guarigione31,32.
Perché la periostina?
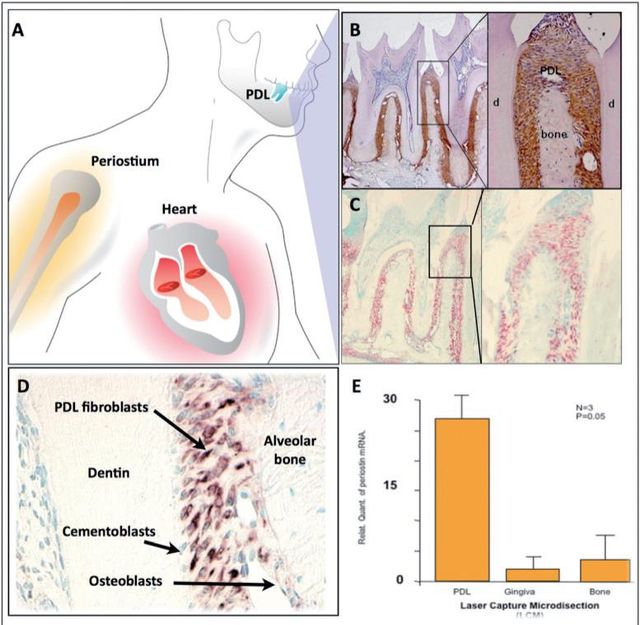
Inizialmente è stato mostrato che la periostina si trova nei denti in fase di sviluppo nei siti di interazione epitelio mesenchimale, elemento che suggerisce che questa proteina potrebbe giocare diversi ruoli come molecola di risposta principale durante lo sviluppo del dente e potrebbe essere legata al deposito e all’organizzazione di altre molecole di adesione durante il mantenimento del parodonto33. Si è trovato che l’mRNA della periostina era regolato negativamente dal Fattore di Crescita Epidermico (EGF) e 1,25-(OH)2 D3 era sovraregolato da TGF-β1 e BMP- 225,26,34. È interessante segnalare come le analisi immunoistochimiche hanno mostrato che, in esemplari di topi adulti, la proteina periostina è di preferenza localizzata nel periosto e nel PDL26, suggerendo ruoli potenziali nel mantenimento e nel rimodellamento di queste strutture. Si è scoperto che tra tutte le proteine conosciute espresse nel PDL, la periostina è quella che mostra la più grande specificità e per questa ragione è comunemente usata come marcatore per il PDL. La periostina, nel contesto parodontale, è espressa specificamente dai fibroblasti del PDL, suggerendo così un ruolo potenziale nella funzione del PDL26,33(Figura 2). Recentemente è stato sottolineato che le attività promotrici della periostina erano potenziate dalla iperespressione di Twist, risultando in una maggiore espressione di periostina in vitro35. Inoltre, in vivo, Twist e periostina sono risultati co-espressi e strettamente regolati dai cambiamenti delle forze occlusali36, elemento che ha portato i ricercatori a ritenere il Twist il fattore trascrittore della periostina. Inoltre la periostina presenta una distribuzione diversa durante il movimento ortodontico dei denti; è sovraregolata nelle aree di compressione e sottoregolata in quelle di tensione37. L’osservazione attraverso immunoelettromicroscopia del PDL maturo ha confermato la localizzazione di periostina tra i processi citoplasmatici dei fibroblasti e cementoblasti parodontali e le fibrille collageniche adiacenti38. Quindi la periostina potrebbe esercitare un controllo sulle proprietà strutturali39 e funzionali dei tessuti del PDL in condizioni di salute o di malattia. Queste scoperte suggeriscono che la periostina sia presente nei siti di interazione tra cellule e matrice, dove agisce come fattore adesivo per sostenere le forze meccaniche, incluse quelle occlusali.
La periostina è necessaria per la normale funzione parodontale?
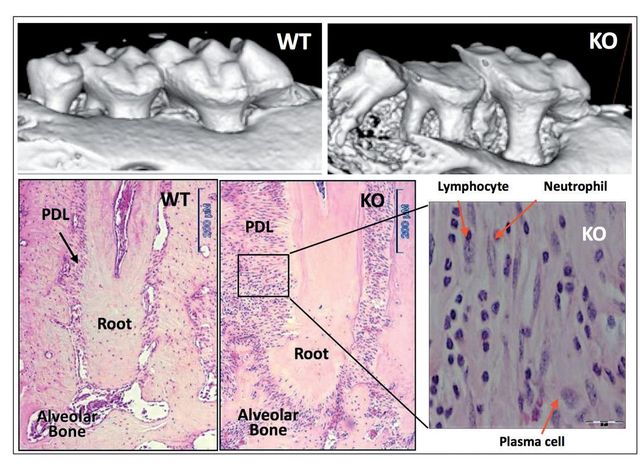
Abbiamo dimostrato inizialmente l’importante ruolo della periostina nell’integrità funzionale e strutturale del parodonto40. Gli animali deficitari di periostina mostrano chiaramente gravi deterioramenti alle strutture di supporto del dente40,41. Il nostro lavoro ha dimostrato che eliminando la periostina il parodonto si deteriora rapidamente nel tempo e non è più in grado di sostenere lo stimolo meccanico fisiologico, chiarendo quindi come sia necessaria questa molecola per la funzione del PDL e, di conseguenza, per l’integrità parodontale (Figura 3). Inoltre, abbiamo mostrato come la periostina sia necessaria durante la funzione occlusale e che in caso di topi con periostina KO, il legamento parodontale non sia in grado di sostenere il normale carico occlusale fisiologico, evento che causa quindi in questo caso uno stimolo traumatico per il parodonto. Mentre la letteratura suggerisce che i traumi occlusali primari portano a una risposta adattativa dove non si genera alcuna distruzione dei tessuti di sostegno, nel caso di periostina KO lo stimolo meccanico può essere classificato come un trauma secondario che, a causa della mancanza della suddetta proteina, genera un effetto nocivo nel parodonto. Questo porta a una grave perdita di osso alveolare, a una perdita severa di CAL e a un significativo aumento dell’ampiezza dello spazio del PDL.