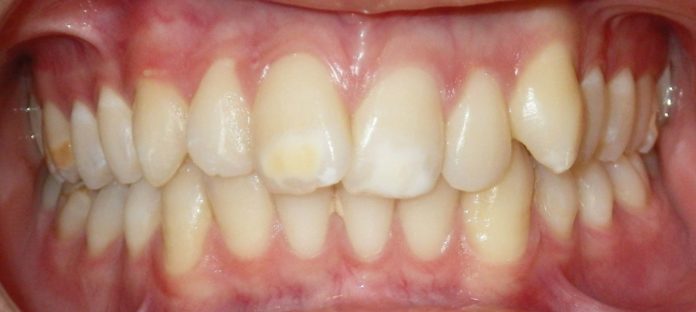
Una diagnosi precoce di queste alterazioni della struttura dentaria può aiutare a migliorare il risultato del trattamento e la qualità di vita dei pazienti affetti.
Le opzioni terapeutiche variano in funzione dei denti interessati, dell’entità di tessuto dentario coinvolto e della presenza o meno di sensibilità. L’approccio terapeutico viene scelto dall’odontoiatra anche in funzione della collaborazione del paziente e della estensione delle anomalie.
Una diagnosi precoce di queste alterazioni della struttura dentaria può aiutare a migliorare il risultato del trattamento e la qualità di vita dei pazienti affetti. Le opzioni terapeutiche variano in funzione dei denti interessati, dell’entità di tessu …
Questo contenuto è riservato agli abbonati al Dentista Moderno.
Abbonati e continua a leggere su DM Club, l'area premium del Dentista Moderno