Riassunto
Finalità del lavoro è individuare i criteri e stabilire gli schemi posologici per il trattamento antibiotico profilattico dei pazienti che si sottopongono a terapie odontoiatriche. Sono state valutate le categorie potenzialmente a rischio per l’insorgenza di infezioni conseguenti a batteriemia susseguenti a specifiche procedure. Sono stati allestiti appositi schemi posologici da attuarsi in base alla terapia preposta e alla patologia primaria.
Pur risultando ridotto rispetto a precedenti trattazioni il numero delle patologie e delle terapie da sottoporre a trattamento profilattico, viene rimarcata l’importanza della profilassi soprattutto perché viene a sostituire il trattamento terapeutico completo in molto trattamenti.
Summary
Antibiotic prophylaxis in dentistry
Aim of this study validate criteria and clinical protocol of antibiotic prophylaxis
in dentistry. We have found the illness condition and the pathologies that needs
antibiotic prophylaxis. We have found scheme posologici second of the primary
phatology and the proposed therapy.
Antibiotic prophylaxis reduce the risk of infection if is correctly used.
Nel corso degli ultimi anni sono state ripetutamente motivo d’indagine le modalità prescrittive dei chemioterapici. Questo interesse si è rivolto, oltre che all’identificazione di schemi terapeutici idonei, anche all’individuazione di molecole efficaci e al loro corretto e mirato utilizzo. Progressivamente ci si è resi conto che in determinate situazioni cliniche la somministrazione di piccole quantità di antibiotico pre-operatoriamente riduceva drasticamente l’insorgenza delle infezioni nel periodo post operatorio. Con il termine profilassi antibiotica si intende la somministrazione di antibiotici allo scopo di prevenire l’insorgenza di infezioni.
L’uso di antibiotici non ha finalità terapeutiche ma solo preventive.
In chirurgia per profilassi si intende la somministrazione di un farmaco prima che si verifichi la contaminazione batterica del campo operatorio e il successivo sviluppo di un’infezione del sito chirurgico.
La profilassi non ha lo scopo di sterilizzare i tessuti ma quello di ridurne la carica
microbica in modo che possa essere controllata dalle difese dell’ospite.
È importante sottolineare il fatto che la profilassi si aggiunge a un buona tecnica chirurgica, ma non la sostituisce.
Affinché si possa ridurre l’incidenza delle infezioni del sito chirurgico è importante che si considerino tre punti fondamentali:
- la scelta dell’antibiotico;
- le modalità di somministrazione;
- in quali interventi la terapia è efficace.
Il razionale della somministrazione profilattica è impedire che un’eventuale batteriemia sostenuta da germi endogeni si trasformi in una malattia infettiva locale o sistemica.
Per tale motivo la profilassi differisce in maniera sostanziale, nella posologia e durata, dalla terapia la cui finalità è la cura di un’infezione in atto3. I vantaggi della profilassi sono innumerevoli; infatti oltre a ridurre la quantità di antibiotico somministrata, la durata del trattamento e il costo economico dello stesso, diminuisce notevolmente anche le probabilità di insorgenza delle resistenze4. È somministrata in un breve lasso di tempo e si avvale di dosaggi più elevati per assicurare la presenza del farmaco in circolo e nel sito operatorio con concentrazioni 3-4 volte superiori alla Minima Concentrazione Inibente (MIC) definendo per MIC la più bassa concentrazione di farmaco in grado di bloccare lo sviluppo batterico rilevabile2.
L’uso empirico della profilassi/terapia antibiotica è di comune riscontro nell’aneddotica odontoiatrica soprattutto in quelle situazioni che determinano sanguinamento è stato rilevato come l’odontoiatra sia responsabile della prescrizione di circa il 10% di tutti i chemioterapici29 e spesso un uso improprio dell’antibioticoterapia più che essere indotto dall’implementazione di linee guida è determinato dai principi di una medicina “difensiva” che sempre più spesso albergano all’interno della categoria.
È altresì utile ricordare come la sola assenza di infezione in atto permette una corretta efficacia del principio profilattico. Attualmente la profilassi interessa solo le specie batteriche e non quelle virali; il motivo è da ricercarsi nella totale mancanza di indicazioni odontoiatriche per queste ultime.
La radicata credenza che un’infezione subclinica (soprattutto orale e a carico dei denti endodonticamente trattati) possa esitare in patologie sistemiche5 anche senza evidenze scientifiche ha condotto odontoiatri e medici generici all’utilizzo di terapie antibiotiche anche dove non espressamente indicate. La correlazione tra batteriemia ed endocardite, soprattutto in conseguenza di un intervento chirurgico intraorale, pur essendo a lungo descritta e caldeggiata6-7 non ha trovato ancora l’identificazione dei processi fisiopatologici.
Anche se da molti anni si provvede alla somministrazione di profilassi per l’endocardite, attualmente si è progressivamente assistito alla riduzione, oltre che della dose e del timing di trattamento, del numero di patologie cardiache che la richiedono. Scopo di questo lavoro è identificare l’attuale concezione di profilassi cercando di sviluppare utili indicazioni per una sua corretta applicazione clinica. In questo lavoro metteremo in luce in quali situazioni è efficace e specificatamente indicata.
Procedure chirurgiche che richiedono la profilassi
Gli interventi chirurgici vengono classificati in quattro tipologie:
- puliti;
- puliti-contaminati;
- contaminati (con flogosi acuta non purulenta);
- sporchi (flemmoni ascessualizzati).
Le procedure chirurgiche del cavo orale avvengono principalmente in ambiente che viene definito “pulito-contaminato”, la situazione in cui la profilassi ha maggior efficacia.
L’incidenza delle infezioni dopo terapia estrattiva è molto bassa, approssimativamente di circa l’1%8.
La batteriemia che insorge in seguito ad alcune terapie odontoiatriche ha una durata assai limitata e generalmente non supera i 15 minuti3, periodo comunque sufficiente a determinare una colonizzazione batterica. Considerando il timing di trattamento, gli schemi profilattici possono essere divisi in:
- ultra short prophilaxis, che consiste in un’unica somministrazione un’ora prima dell’intervento;
- short prophilaxis, che consiste in più somministrazioni: un’ora prima dell’intervento e ogni 8 ore dopo l’intervento fino alla copertura delle prime 24 ore.
Sotto il termine chirurgia dento-alveolare si raggruppano un nutrito gruppo di tecniche che possono essere eseguite sia dal dentista generico sia dallo specialista (parodontologo, chirurgo orale ecc.).
Possono essere interessati solo i tessuti molli (biopsia, gengivectomia ecc.) o anche quelli duri (inclusione dentarie ecc.).
Solitamente queste tecniche, se eseguite da mani esperte, prevedono un danno tessutale ridotto e dei tempi operativi che raramente superano i 60 minuti.
L’asportazione degli ottavi inclusi e il posizionamento di impianti sono le procedure che presentano il maggior rischio di infezioni e di possibili sequele.
Considerando i denti del giudizio, il principale problema è che spesso si confonde la normale infiammazione da trauma chirurgico con infezioni della ferita. Inoltre, spesso si confondono le alveoliti come infezioni batteriche e non per quello che realmente sono cioè problemi di guarigione conseguenti a un’aumentata attività fibrinolitica.
La definizione di infezione post chirurgica del sito estrattivo dovrebbe prevedere la presenza di cellulite (con fluttuazione, tensione e calore locale), fuoriuscita di pus dopo 72 ore dall’intervento, dolore e gonfiore che si prolungano dopo le 48 ore e persistente temperatura corporea superiore ai 38 °C28.
In chirurgia parodontale, in presenza di un sito altamente contaminato, la profilassi trova indicazione soprattutto nei pazienti immunodepressi e in presenza di presidi protesici9.
L’uso della profilassi preimplantare è stato a lungo controverso10.
Una recente review della Cochrane Library ha riconosciuto l’efficacia di una somministrazione di 2 g di amoxicillina 1 ora prima dell’intervento in condizioni standard.
Non risulta ancora chiara l’efficacia dell’antibioticoterapia post operatoria e l’antibiotico di prima scelta.
Si conclude con la raccomandazione di utilizzare una singola dose di profilassi antibiotica prima dell’inserimento delle fixture25.
Alcuni Autori ritengono29 che sia indicata in tutte le procedure in cui:
- si esegua l’impianto di fixture o biomateriale;
- l’infezione post operatoria può comportare conseguenze di particolare gravità;
- i pazienti abbiano una valutazione secondo la classificazione dell’American Society of Anesthesiologist (ASA) maggiore o uguale a 3.
Situazioni cliniche che richiedono la profilassi
Tradizionalmente in questa categoria si distinguono due tipi di profilassi:
- quella per l’endocardite batterica;
- quelle relative ad altre situazione cliniche potenzialmente patogene.
Ci sembra comunque indicato
suddividere il secondo gruppo in altri sottogruppi le cui condizioni convergono per affinità.
Endocardite batterica
L’endocardite è definita come uno stato infiammatorio, proliferativo ed essudativo dell’endocardio. L’incidenza è di 1-5 casi ogni 100.000 abitanti/anno26. È caratterizzata da vegetazioni di superficie causate dalla proliferazione batterica. Solitamente le valvole cardiache sono interessate.
Difetti congeniti o acquisiti possono predisporre l’insorgenza della patologia soprattutto se accompagnati da alterazione emodinamiche che provocano turbolenza del flusso intracardiaco. La profilassi trova indicazione se le procedure odontoiatriche coinvolgono i tessuti gengivali, ossei, la regione periapicale del dente o la manipolazione traumatica della mucosa orale. Recentemente l’American Heart Association (AHA) ha notevolmente ridotto le indicazioni profilattiche (tabella 2) identificando le condizioni che possono realmente indurre endocardite e conseguentemente minimizzando le possibili reazioni avverse imputabili a un indiscriminato uso dell’antibiotico (soprattutto quelle allergiche penicillina-correlate)28.
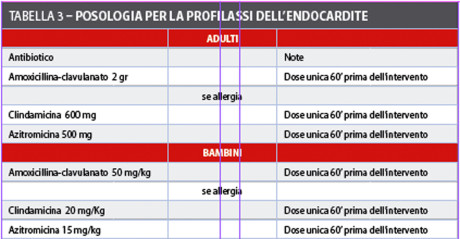
Il risultato è stato, oltre a un notevole decremento delle indicazioni, anche la riduzione della posologia necessaria il tutto accompagnato dall’uso di antibiotici di classi diverse per evitare reazioni allergiche crociate (tabella 3). Saltuariamente
possono verificarsi delle discordanze sulle indicazioni; in questi casi è doveroso ricordare che la valutazione del rapporto rischi/benefici è ad appannaggio dell’odontoiatra anche se la consultazione con il collega è doverosa al fine di ottenere una comune visione del problema.
Cateteri permanenti, shunt neurochirurgici e altri presidi
Solitamente la presenza di cateteri permanenti non impone la profilassi, a eccezione di quelli in prossimità del cuore destro.
Un significativo rischio di infezione dello stent dopo intervento percutaneo coronarico (PCI) si ha nelle prime due settimane dal posizionamento; successivamente uno strato epiteliale, ricoprendolo, riduce notevolmente questa eventualità.
I dispositivi sottocutanei per la somministrazione sistemica di farmaci per lunghi periodi inducono l’utilizzo della profilassi quando il paziente presenta una situazione immunitaria compromessa e non finalizzata alla presenza del catetere stesso.
Pur non essendo unanimemente condivisa1, in molti centri i pazienti emodializzati che presentano una fistola aterovenosa (sia autogena che con la presenza di una protesi vascolare) vengono preventivamente sottoposti a copertura antibiotica in quanto lo shunt, per sua natura, è particolarmente vulnerabile alle colonizzazioni batteriche. È altresì utile ricordare la possibilità di una latente immunodepressione a carico di questi pazienti soprattutto se da lunga data sono stati sottoposti a emodialisi.
Nella dialisi peritoneale, invece, non viene richiesto alcun tipo di profilassi.
I pazienti con idrocefalo possono presentare due tipi di derivazione per il drenaggio del liquido cefalorachidiano in eccesso: la derivazione ventricolo atriale e quella ventricolo peritoneale. Le infezioni sono più frequenti nelle prime due settimane dopo il posizionamento. La letteratura suggerisce che in seguito a trattamenti odontoiatrici risultano più esposte le derivazioni ventricolo atriali nelle quali la profilasi trova indicazione11.
Per le altre tipologie di presidi protesici (quali defibrillatori, pacemaker ecc.) non ci sono evidenze che supportano l’utilizzo routinario di antibiotico profilassi12.
Particolare attenzione meritano le protesi articolari (soprattutto d’anca); infatti sia per la rarità sia per i patogeni interessati (sporadicamente gli streptococchi orali) l’odontoiatra tende a non somministrare la profilassi. Tuttavia non è di infrequente riscontro imbattersi in indicazioni profilattiche suggerite dal collega ortopedico. Fattori che possono indurne l’utilizzo sono la concomitante presenza di immunosoppressione, infiammazione cronica del presidio e certezza di indurre una elevata batteriemia27.
Pazienti immunocompromessi
I pazienti immunosoppressi rappresentano una categoria eterogenea che mostra un rischio elevato di sviluppare, in seguito a batteriemia, una progressiva infezione sistemica13,14. Di seguito verranno analizzate le varie situazioni cliniche che determinando una riduzione delle difese immunitarie possono necessitare di profilasi. Durante il trattamento chemioterapico si è rilevata una particolare sensibilità alle infezioni. Per questi pazienti la profilassi è raccomandata in tutte le pratiche che, determinando sanguinamento, inducono batteriemia.
Nei pazienti sieropositivi in trattamento con retro virali abitualmente la profilassi non è indicata. Ovviamente nel caso che il clinico lo ritenesse opportuno, soprattutto in presenza di infezioni sistemiche conclamate, la somministrazione profilattica è raccomandata.
Altra importante categoria da considerare è rappresentata dai diabetici. Questi, soprattutto se insulino-dipendenti, mostrano una maggior suscettibilità alle infezioni16 anche a causa di una frequente e concomitante disfunzione leucocitaria. La copertura antibiotica più che essere determinata dalla tipologia d’intervento o dall’eventuale insulino-dipendenza viene suggerita dalla capacità di controllo del livello glicemico (valutabile attraverso il valore dell’emoglobina glicata). Frequenti e quantitativamente significativi sbalzi impongono oltre a un attento monitoraggio anche un’adeguata profilassi15. Non ci sono dati certi circa l’utilità di una somministrazione nei pazienti tossicodipendenti. La loro elevata tendenza a sviluppare endocardite non è stata necessariamente correlata a una possibile batteriemia di origine odontoiatrica17. Similmente non è stata dimostrata una maggior suscettibilità infettiva in seguito a trattamenti odontoiatrici nei pazienti sottoposti a splenectomia18,19.
La profilassi in età pediatrica
Alcune significative differenze vanno considerate prima di un trattamento antibiotico in età pediatrica:
- i giovani pazienti tendono a non avere una pregressa anamnesi farmacologica paventando la possibilità di allergie o reazioni avverse;
- la notevole percentuale di acqua nei tessuti e l’estesa componente spongiosa dell’osso facilitano la diffusione delle infezioni;
- la difficoltà al mantenimento di una corretta igiene orale associata a una dieta ricca di carboidrati aumenta il rischio di batteriemia;
- le frequenti infezioni che interessano l’anello di Waldeyer con conseguente antibioticoterapia aumentano la probabilità di resistenze.
Considerando ciò la profilassi viene indicata in ogni intervento chirurgico, soprattutto se si sospetta la presenza di un’alta carica microbica.
Le indicazione si possono applicare ai seguenti casi:
- pazienti immunodepressi compresi quelli in chemio-radioterapia20. Questi criteri vanno, inoltre, applicati ai seguenti casi: infezione da HIV, immunodeficienze, neutropenie, immunosoppressioni, anemia, splenectomia, uso abituale di steroidi, lupus eritematoso, diabete e trapianti d’organo21;
- pazienti con problematiche cardiache associabili a endocardite. Oltre alle raccomandazioni dell’AHA e in accordo con questa, l’American Accademy of Pediatric Dentistry (AAPD) ha aggiunto i pazienti con storia di assunzione di farmaci per via endovenosa (soprattutto se associata ad anomalie cardiache)22 e i bambini affetti da sindromi (di Down, di Marfan ecc.) in cui sono frequenti alterazioni cardiache spesso misconosciute23,24;
- pazienti con shunt, cateteri permanenti o con presidi. Si utilizzano le stesse indicazioni per la persona adulta;
- casi di auto-trapianto dentale.
Non mancano tuttavia Autori30 che in seguito al riscontro, dopo il posizionamento della matrice o della diga di gomma, di una batteriemia paragonabile a quella post estrattiva caldeggiano un riesame delle linee guida fin qui adottate.
Schemi profilattici
L’identificazioni di schemi posologici per la somministrazione trova un razionale nella pratica operativa e la rilevazione di possibili insuccessi potrebbero portare a eventuali modifiche. Durante la somministrazione antibiotica a scopo profilattico il livello plasmatico dovrebbe essere più elevato rispetto a quello utilizzato per fini terapeutici. In considerazione di ciò la dose raccomandata è solitamente il doppio di quella terapeutica.
Di seguito vengono elencati gli schemi normalmente utilizzati considerando sia le vie di somministrazione sia le alternative in caso di allergia (tabella 4).
Conclusioni
Scopo della profilassi è prevenire l’infezione della ferita chirurgica con la creazione di uno stato di resistenza ai microrganismi attraverso la concentrazione ematica di antibiotico che evita la disseminazione e la proliferazione dei batteri dal loro punto di entrata rappresentato dalla ferita chirurgica.
A tutt’oggi non esistono studi clinici affidabili per quantità e qualità che possano validare protocolli di profilassi antibiotica31.
Il rischio di contaminazione della ferita chirurgica aumenta con il tempo di esposizione e con la complessità dell’intervento ed è ridotto da una buona tecnica o dal buon stato di salute del paziente.
Il collegamento tra procedure odontoiatriche ed endocardite batterica rimane
controverso; tuttavia anche una corretta somministrazione profilattica non esclude completamente la possibile insorgenza della patologia.
Bisogna considerare che non tutte le procedure odontoiatriche inducono batteriemia (come la conservativa e la protesi) non motivando un uso indiscriminato della stessa.
Fondamentale risulta l’individuazione delle procedure chirurgiche che ne possano beneficiare sia localmente sia per la concomitante batteriemia.
È sempre utile ricordare i possibili effetti nocivi dell’antibioticoterapia che se infrequenti possono risultare importanti (reazioni allergiche).
Quest’ultima eventualità e tanto più significativa se si considera che il luogo di somministrazione è, dato la tempistica, il nostro ambulatorio.
Allo stesso tempo l’adozione di posizioni difensivistiche – intese come l’indiscriminato uso della terapia antibiotica a lungo termine – non trova motivazioni e nel lungo periodo può determinare l’insorgenza di resistenze.
Corrispondenza
Lorenzo Damia
Tel . 02.20240373 – 347.0482143
Fax 02/20240373
lorenzodamia@katamail.com