Riassunto
L’atrofia della cresta alveolare, in senso sia verticale sia orizzontale, è l’esito della perdita di elementi dentali dovuta a estrazioni, carie, traumi o motivi parodontali. In caso di riassorbimento estremo, l’inserimento di impianti, secondo i protocolli attuali è possibile nel caso in cui vengano ristabiliti i corretti volumi ossei mediante il ricorso a tecniche di aumento della cresta atrofica effettuata sia con osso autologo sia con biomateriali. Scopo del presente lavoro è illustrare un caso clinico di riassorbimento dell’osso alveolare di 1.1. per grave parodontopatia.
La correzione dell’atrofia è stata realizzata prelevando un blocco di osso dal trigono retromolare, mediante chirurgia piezoelettrica (Easy Surgery® Biosaf) e innestato al sito ricevente con l’ausilio di una vite da osteosintesi. Una volta trascorsi i normali tempi di guarigione, si è proceduto all’inserimento di un impianto a superficie SLA e, dopo due mesi, alla sua protesizzazione.
Questa tecnica ha reso possibile il recupero dell’elemento, oltre che dal punto di vista funzionale anche da quello estetico, con effetti positivi anche sul supporto osseo degli elementi adiacenti come dimostrato dal controllo radiografico a due anni.
Summary
Vertical augmentation of alveolar ridge with autologous bone in aesthetic zone
Alveolar ridge atrophy, both in vertical and horizontal sense, is the loss of teeth due to extractions, decay, trauma or parodontal reasons. In case of extremely resorption,
dental implants, according to actual protocols, is possible when correct bone volumes are re-established through augmentation ridge atrophy techniques made with autologous bone or biomaterials.
Aim of this work is to show a clinical report of alveolar bone resorption of central incisor for high degree of parodontal disease. The correction of atrophy as been realized taking a block section from retromolar area through piezoelectrical surgery (Easy Surgery® Biosaf) and grafted in the receiving site with osteosynthesis screw. As healing time passed, a dental implant SLA surface as been implanted and after two months, to prosthesis.
This technique has made possible the recovery of the site from both functional and aesthetic point of view, with positive effects even on adjacent teeth bone.
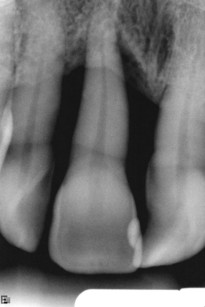
Le cause che portano all’atrofia ossea sono molteplici. La perdita di elementi dentali per parodontopatia, per il grave riassorbimento osseo che ne può derivare, costituisce un ostacolo alla riabilitazione delle edentulie totali o parziali mediante inserimento di impianti, dato che la condizione primaria e indispensabile è la disponibilità ossea.
Attualmente, le procedure per la rigenerazione ossea guidata (GBR, guided bone regeneration) in chirurgia orale prevedono l’utilizzo di materiali da innesto classificabili come autologhi (tessuto osseo prelevato dallo stesso individuo), omologhi (tessuto osseo prelevato da un individuo della stessa specie, ma di patrimonio genetico diverso) o eterologhi (di origine animale o di sintesi)1-5.
Nella letteratura internazionale, numerosi sono gli studi che hanno indagato la scelta del materiale da innesto più idoneo e molti autori sono concordi nel considerare l’osso autologo fresco spongioso e corticale il materiale di scelta per le sue proprietà osteogenetiche, osteoconduttive e moderatamente osteoinduttive.
La capacità osteoinduttiva è potenzialmente attiva perché la proteina morfogenetica ossea (BMP, bone morphogenetic protein) è presente in minime quantità nell’osso spongioso (di solito è contenuta in maggior quantità nell’osso corticale) e si esprime solo dopo esposizione della proteina da parte degli osteoclasti.
Gli innesti cortico-spongiosi autologhi vengono rapidamente rivascolarizzati e, inoltre, sono privi di immunogenicità e del rischio di infezioni virali6,7.
Il prelievo di osso autologo è associato a problematiche quali: l’esposizione di una seconda sede chirurgica (intra o extraorale) con aumento dei tempi operatori, complicanze intraoperatorie e della morbilità post-chirurgica e, inoltre, le quantità prelevabili sono spesso limitate8,9.
Di contro, l’uso di materiali eterologhi presenta diversi vantaggi quali: l’assenza di un sito chirurgico donatore, la riduzione
del rischio di lesioni neurologiche e/o vascolari e la diminuzione della morbilità post-operatoria3.
Con l’innesto di osso autologo è possibile ottenere un elevato grado di predicibilità associato a una ridotta morbilità e tempi brevi di guarigione10.
La quantità necessaria di materiale da innesto determina l’area di prelievo.

Quali siti donatori sono disponibili le regioni del mascellare inferiore e superiore, la calotta cranica, la costola, la cresta iliaca e la tibia. I siti di prelievo intraorale preferiti sono: la zona retromolare, il tuber, la sinfisi mentoniera, le zone edentule, il processo coronide, il toro palatino o mandibolare e la zona zigomatica11-14.
La sinfisi è un sito donatore facilmente accessibile, fornisce una buona quantità di osso, ma sono frequenti gli esiti di tipo neurosensoriale transitori o permanenti15-18.
La zona retromolare, in mancanza del terzo molare, offre una buona quantità di osso, è facilmente accessibile e non ha effetti collaterali di tipo estetico.
Studiando radiograficamente il decorso del canale mandibolare è difficile causarne la lesione, con esiti clinici ottimali.
Paragonato a quello della cresta iliaca, l’osso mandibolare mostra poco riassorbimento19,20 e il periodo di guarigione, di solito, è di 6-9 mesi21.
Comunque, un periodo di guarigione di quattro mesi, secondo gli studi clinici, è sufficiente per l’inserimento di impianti22.
Un importante presupposto per il successo dell’innesto è l’intimo contatto tra superficie dell’impianto e tessuto osseo, facilmente ottenibile con adeguati dispositivi che aumentano la ritenzione meccanica (osteosintesi con viti) e con una buona vascolarizzazione del sito. Anche la tecnica di prelievo risulta importante.
Viene presentato e discusso un caso clinico di riabilitazione implantare preceduta da rialzo verticale di cresta mediante l’impiego di osso autologo, con due anni di follow-up dal carico protesico, prelevato con dispositivo piezoelettrico (Easy Surgery® Biosaf), nella zona dell’incisivo superiore destro, dove l’innesto e l’impianto hanno consentito il recupero estetico e funzionale della zona edentula.
Caso clinico
È giunta alla nostra osservazione una paziente di 46 anni in buone condizioni di salute generale. Riferisce una storia di parodontopatia e, da alcuni anni, di mobilità dell’elemento 1.1.
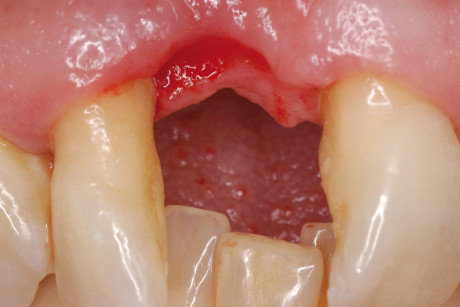
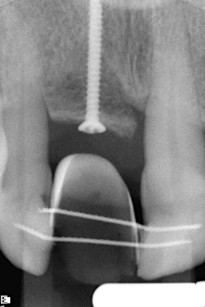
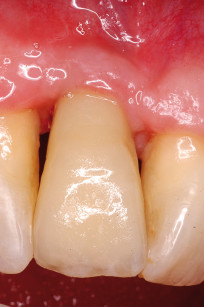
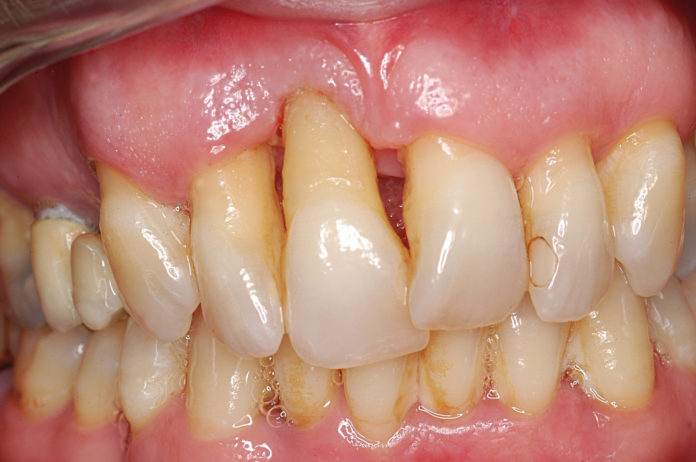
All’esame obiettivo intraorale si reperta, in corrispondenza di molti elementi, la presenza di tasche e recessioni. In corrispondenza di 1.1 (figura 1) si evidenzia una grave recessione, confermata dalla radiografia endorale. All’esame con Periotest, il PTV (Perio Test Value) di 1.1 è + 30 e si conferma la mobilità di grado 3. Per un elemento con parodonto integro il PTV è di solito compreso tra – 8 e + 9 (grado 0)7.
Prima delle fasi chirurgiche sono state effettuate sedute di scaling e root planing su tutti e quattro i quadranti. È stato, inoltre, fatto leggere e firmare il consenso informato.
Prima fase chirurgica
Previa assunzione di terapia antibiotica con amoxicilllina + acido clavulanico (1 g ogni 12 ore per 3 giorni), si è preceduto solamente all’estrazione dell’incisivo compromesso.
È stata praticata anestesia plessica con articaina 1:200.000, estratto l’elemento, sottoposti a curettage gli elementi prossimali al difetto e suturati i lembi.
La decisione di non effettuare subito l’innesto, ma aspettare 15 giorni, si è resa indispensabile per permettere la normale guarigione dei tessuti molli, necessari poi alla completa copertura dell’innesto (figura 2).
Seconda fase chirurgica
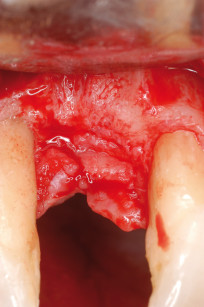
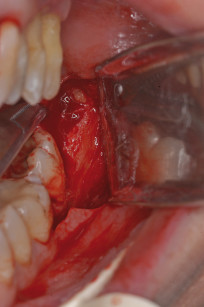
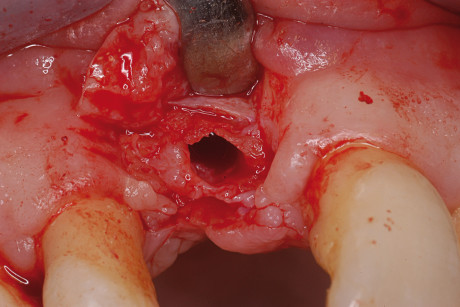
Trascorso tale periodo, è stato eseguito l’intervento di prelievo di osso autologo e innesto. Un’ora prima è stata prescritta terapia antibiotica con amoxicillina + acido clavulanico (l g ogni 12 ore per 6 giorni). Eseguito un lembo a tutto spessore con incisione sul versante palatino a circa 5 mm dal centro della cresta e a bisello interno ed esposto il letto ricevente (figura 3), sono state valutate le dimensioni del sito (circa 1 cm x 7 mm x 1 cm di altezza). Si è, quindi, proceduto all’esposizione del sito donatore in corrispondenza della zona retromolare e prelevato con dispositivo piezoelettrico (Easy Surgery® Biosaf) un blocco di adeguate dimensioni (figura 4).
La scelta di prelevare osso membranoso piuttosto che osso endocondrale offre evidenti vantaggi, grazie alle migliori proprietà biologiche di rivascolarizzazione e resistenza al riassorbimento dell’osso membranoso23. Il vantaggio della chirurgia piezoelettrica è data dal taglio micrometrico, dall’assenza di sanguinamento che, se presente, limita la visibilità del campo operatorio, grazie all’effetto cavitazionale, senza compromettere la vitalità dell’innesto24. Eseguito il foro di ingresso per la vite da osteosintesi (14 x 2 mm), si è proceduto all’adattamento dell’innesto al sito ricevente (figura 5) e unito saldamente a quest’ultimo previa cruentazione delle pareti ossee per consentire un maggior apporto di sangue, ricco di cellule totipotenti e di fattori di crescita (figura 6).
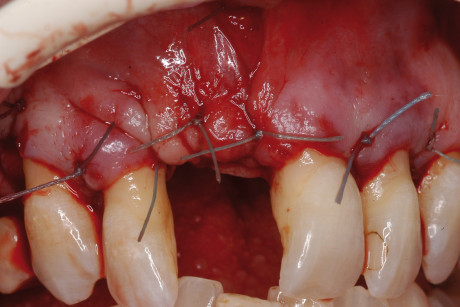
La stabilizzazione va effettuata con il lato trabecolare rivolto verso l’osso ricevente onde prevenire il riassorbimento dell’innesto e favorire una più rapida vascolarizzazione. In ultimo, sono stati accuratamente passivizzati i lembi, a coprire in modo totale l’innesto e posizionati i punti di sutura staccati in poliammide (Biopol) (figura 7).
Nel post-intervento è stato somministrato Betametasone 4 mg e.v. ed è stata prescritta una terapia analgesica (Ibuprofene 600 mg ogni 12 ore per 6 giorni e clorexidina 0,20%, sciacqui 3 volte al dì per 7 giorni).
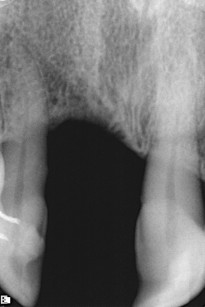
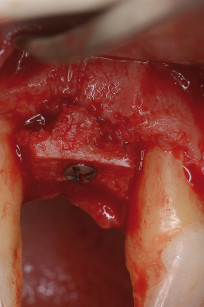
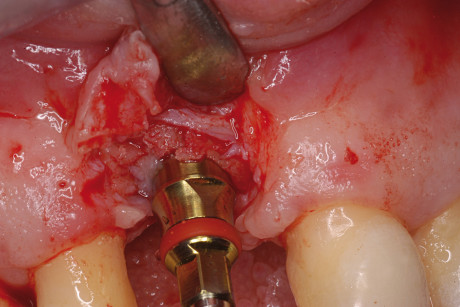
A distanza di 10 giorni sono state rimosse le suture, senza esiti locali di nessun tipo. Nel periodo di guarigione non si è avuta esposizione dell’innesto e la radiografia di controllo ha confermato l’adattamento al sito ricevente. Dopo quattro mesi è stato effettuato il rientro chirurgico. Previa somministrazione di terapia antibiotica è stato eseguito il lembo a tutto spesso ed esposta la vite da osteosintesi (figura 8).
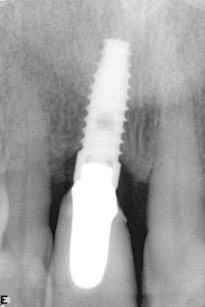
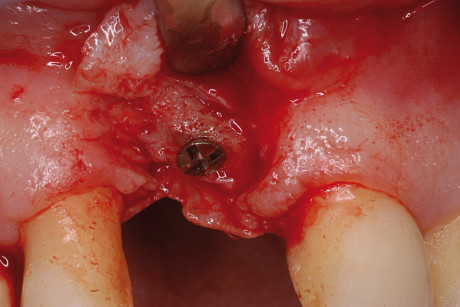
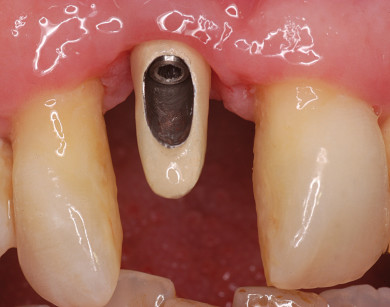
Dalla sua sporgenza si può evidenziare il minimo riassorbimento dell’innesto. La vite è stata quindi rimossa e lo stesso foro è stato ampliato (figura 9) ed è stato inserito l’impianto a superficie SLA da 4 x 13 mm. Dopo 60 giorni è stato protesizzato con un moncone e una corona provvisoria (figura 10) e condizionata la guarigione dei tessuti molli.
A distanza di ulteriori 60 giorni è stata effettuata la riabilitazione protesica definitiva con un moncone ceramizzato e con la tecnica dello switch-platform (figura 11) e una corona in ceramica integrale Empress 2 (figura 12).
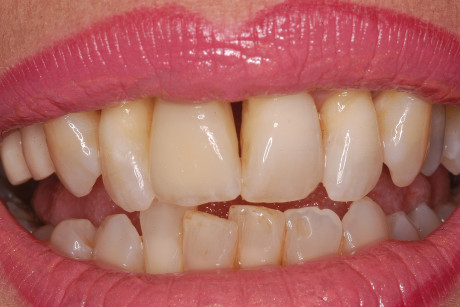
Il vantaggio offerto dallo switch-platform consiste nella miglior preservazione dell’osso crestale23. La corona in ceramica integrale, grazie all’assenza del metallo, garantisce una più elevata resa estetica, con un aspetto del dente protesico del tutto simile a quello del dente naturale (figura 13).
A otto mesi, epoca della protesizzazione definitiva, è stato valutato il PTV di 1.2, + 12 e il PTV di 2.1, + 10, a dimostrazione della miglior stabilità degli elementi adiacenti al difetto rispetto al controllo iniziale. A distanza di due anni dalla protesizzazione è stato eseguito il controllo radiografico (figura 14), che ha evidenziato l’ottimale adattamento dell’impianto e l’integrazione dell’innesto osseo, utile anche alla stabilizzazione degli elementi adiacenti, come dimostrato dalla misurazione con il Periotest che dava un PTV + 8 di 1.2 e il PTV + 6 di 2.1.
Discussione e conclusioni
Come conseguenza di estrazioni, sia per motivi parodontali sia per carie o traumi, l’esito è l’atrofia della cresta alveolare, in senso sia verticale sia orizzontale.
In caso di riassorbimento estremo, inserire gli impianti, secondo i protocolli attuali, non è sempre possibile. In queste situazioni l’unica possibilità è fare ricorso a tecniche di aumento della cresta atrofica e, tra i materiali proposti, l’osso autologo è il materiale di scelta per le proprietà osteogenetiche, osteoconduttive e osteoinduttive, anche se è necessario un secondo sito di intervento per il prelievo.
Il caso clinico proposto riguarda proprio il riassorbimento dell’osso alveolare di 1.1. per grave parodontopatia.
La scelta del trigono retromolare per il prelievo è stata effettuata in quanto, per la riabilitazione del dente singolo, è un metodo attendibile per il minimo effetto e il minimo rischio di complicanze6.
Il prelievo dell’innesto dalla zona retromolare effettuato con la chirurgia piezoelettrica (Easy Surgery® Biosaf) ha certamente contribuito alla buona riuscita della procedura di prelievo, in quanto il taglio micrometrico e l’assenza di sanguinamento, grazie all’effetto cavitazionale, danno una migliore visibilità senza compromettere la vitalità dell’innesto24-25, con un’eccellente guarigione del secondo sito chirurgico. L’innesto effettuato ha avuto, a distanza di quattro mesi, un riassorbimento minimo, valutabile dall’esposizione della vite da osteosintesi, e ha consentito l’inserimento di un impianto di dimensioni adeguate per diametro e lunghezza.
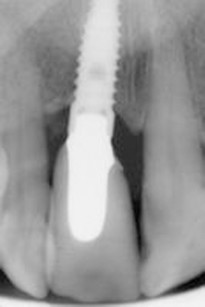
Questo ha favorito il ripristino, anche estetico, della zona edentula. L’importanza del fattore estetico viene raramente incluso nelle valutazioni. Infatti, la maggior parte degli articoli considerano rilevante solo la sopravvivenza dell’impianto9. Il ricorso a tecniche quali il moncone ceramizzato switch platform e la corona in ceramica integrale, hanno reso possibile un’estetica eccellente, in una zona così delicata da questo punto di vista, ma è anche importante la rigenerazione ossea in corrispondenza degli elementi vicini che ne ha favorito la stabilizzazione, requisito necessario al loro recupero e mantenimento, come evidenziato dal controllo radiografico, eseguito due anni dopo la protesizzazione, che ha evidenziato l’adattamento ottimale dell’impianto e l’integrazione dell’innesto osseo, utile anche alla stabilizzazione degli elementi adiacenti, come dimostrato dalla misurazione con il Periotest.
Ringraziamenti
Si vuole ringraziare il Laboratorio Odontotecnico P3 di Ivano Paolantoni e Massimiliano Pezzotti
per il valido contributo fornito.
Corrispondenza
dottor Bruno Marcelli
Via Sulpicio Rufo 14 – 00174 Roma
b.marcelli@libero.it
• Bruno Marcelli1
• Alessia Delli Carpini
• Maurizio Procaccini1
1 Università Politecnica delle Marche, Istituto di Scienze Odontostomatologiche, Direttore professor Maurizio Procaccini
2. Labanca M, Leonida A, Rodella FL. Biomateriali naturali o di sintesi in odontoiatria: scienza ed etica come criteri per la loro scelta. Implantologia 2008;1:9-23.
3. Misch CE, Dietsh F. Bone grafting materials
in implant dentistry. Implant Dent 1993;2:
158-167.
4. Hollinger JO, Brekke J, Gruskin E, Lee D. Role of bone substitutes. Clin Orthop 1996;324:55-65.
5. Moghadam HG, Sándor GK, Holmes HH, Clokie CM. Histomorphometric evaluation of bone regeneration using allogeneic and alloplastic bone substitutes. J Oral Maxillofac Surg 2004;62:202-213.
6. Buckwalter JA, Glimcher MJ, Cooper RR. Bone biology. Part 1: structure, blood supply, cells, matrix and mineralization. J Bone & Joint Surg 1995;77A:1256-75.
7. Lukas D: Periotest: a dynamic procedure for the diagnosis of the human periodontium. Clin Phys Physiol Meas 1990;11:65-75.
8. Jovanovic SA, Schenk RK, Orsini M, Kenney EB. Supracrestal bone formation around dental implants: an experimental dog study. Int J Oral Maxillofac Implants 1995;10:23-31.
9. Albrektsson T, Zarb G, Worthington P, Eriksson AR. The long-term efficacy of currently used dental implants: a review and proposed criteria of success. Int J Oral Maxillofac Impl 1986;1:11-25.
10. Simion M, Trisi P, Piattelli A. Vertical ridge augmentation using a membrane technique associated with osseointegrated implants. Int J Period Rest Dent 1994;14:497-511.
11. Proussaef P, Lozada J, Kleinman A, Rohrer MD. The use of ramus autogenous block grafts for vertical alveolar ridge augmentation and implant placement: a pilot study. Int J Oral Maxillofac Implants 2002;17:238-48.
12. Neukam M. Anatomic site evaluation of the zygomatic bone for dental implant placement. Clin Oral Implants Res 2003;14:72-79.
13. Nkenke M, Radespiel-Troger M, Wiltfang J, Schultze-Mosgau S, Winkler G, Neukam FW. Morbidity of harvesting of retromolar grafts: a prospective study. Clin Oral Implants Res 2002;13:514-21.
14. Nkenke M, Schultze-Mosgau S, Radespiel-Troger M, Kloss F, Neukam FW. Morbidity of harvesting of chin grafts: a prospective study. Clin Oral Implants Res 2002;12:495-502.
15. Joshi A. An investigation of post-operative morbidity following chin graft surgery. Br Dent J 2004 Feb;194(4):215-218.
16. Von Arx T, Häfliger J, Chappuis V. Neurosensory disturbances following bone harvesting in the symphysis: a prospective clinical study. Clin Oral Implant Res 2005;16(4):432-9.
17. Cordaro L, Rossini C, Mijiritsky E. Fracture and displacement of lingual cortical plate of mandibular symphysis following bone harvesting: case report. Implant Dent 2004;13(3):202-6.
18. Chiriac G, Herten M, Schwarz F, Rothamel D, Becker J. Autogenous bone chips: influence of a new piezoelectric device (Piezosurgery) on chip morphology, cell viability and differentiation. J Clin Periodontol 2005 Sep;32(9):994-9. 19. Lundgren S, Moy P, Johansson C, Nilsson H. Augmentation of the maxillary sinus floor with particulate mandible: a histologic and histomorphometric study. Int J Oral Maxillofac Impl 1996;11:760-766.
20. Listrom RD, Symington JS. Osseointegrated dental implants in conjunction with bone grafts. Int J Oral Maxillofac Surg 1988;17:116-118.
21. Misch CM, Misch C, Resnik RR, Ismail YH. Reconstruction of maxillary alveolar defects with mandibular symphysis grafts for dental implants: a preliminary procedural report. Int J Oral Maxillofac Impl 1992;7:360-6.
22. Kusiak JF, Zins JE, Whitaker LA. The early revascularization of membranous bone. Plast Reconstr Surg 1985;76:510-4.
23. Hansen-Algenstaedt N, Joscheck C, Wolfram L, et al. Sequential changes in vessel formation and microvascular function during bone repair. Acta Ortoph 2006 Jun;77(3):429-39.
24. Belser UC, Schmid B, Higginbottom F, Buser D. Outcome analysis of implant restorations located in the anterior maxilla: a review of the recent literature. Int J Oral Maxillofac Impl 2004;19(Suppl):30-42.
25. Sacco R. Innesto a interposizione: revisione della letteratura e casistica clinica come alternativa nel trattamento delle atrofie mandibolo-mascellari. Dent Mod 2008;3:28-45.





[…] Il Dentista Moderno (Aumento verticale di cresta mediante innesto autologo in zona estetica). […]